
- •1.Кинематика материальной точки. Системы отсчета. Траектория, перемещение, путь, средняя путевая и средняя скорость по перемещению.
- •2. Мгновенная скорость. Путь, как интеграл.
- •3. Равномерное и равнопеременное движения. Координатное и графическое представления.
- •4. Криволинейное движение. Нормальное и тангенциальное ускорение.
- •5. Движение точки по окружности. Угловые перемещение, скорость, ускорение. Связь между линейными и угловыми характеристиками.
- •6. Динамика материальной точки. Сила и движение. Инерциальные системы отсчета и первый закон Ньютона.
- •7. Фундаментальные взаимодействия. Силы различной природы (упругие, гравитационные, трения), второй закон Ньютона. Третий закон Ньютона.
- •8. Закон всемирного тяготения. Сила тяжести и вес тела.
- •9. Силы сухого и вязкого трения. Движение по наклонной плоскости.
- •10.Упругое тело. Силы и деформации при растяжении. Относительное удлинение. Напряжение. Закон Гука.
- •11. Импульс системы материальных точек. Уравнение движения центра масс. Импульс и его связь с силой. Столкновения и импульс силы. Закон сохранения импульса.
- •12. Работа, совершаемая постоянной и переменной силой. Мощность.
- •13. Кинетическая энергия и связь энергии и работы.
- •14. Потенциальные и непотенциальные поля. Консервативные и диссипативные силы. Потенциальная энергия.
- •15. Закон всемирного тяготения. Поле тяготения, его напряженность и потенциальная энергия гравитационного взаимодействия.
- •16. Работа по перемещению тела в поле тяготения.
- •17. Механическая энергия и её сохранение.
- •18. Соударение тел. Абсолютно упругий и неупругий удары.
- •19. Динамика вращательного движения. Момент силы и момент инерции. Основной закон механики вращательного движения абсолютно твердого тела.
- •20. Вычисление момента инерции. Примеры. Теорема Штейнера.
- •21. Момент импульса и его сохранение. Гироскопические явления.
- •22. Кинетическая энергия вращающегося твердого тела.
- •24. Математический маятник.
- •25. Физический маятник. Приведенная длина. Свойство оборотности.
- •26. Энергия колебательного движения.
- •27. Векторная диаграмма. Сложение параллельных колебаний одинаковой частоты.
- •28. Биения
- •29. Сложение взаимно перпендикулярных колебаний. Фигуры Лиссажу.
- •30. Статистическая физика (мкт) и термодинамика. Состояние термодинамической системы. Равновесное, неравновесное состояния. Термодинамические параметры. Процесс. Основные положения мкт.
- •31. Температура в термодинамике. Термометры. Температурные шкалы. Идеальный газ. Уравнение состояния идеального газа.
- •32. Давление газа на стенку сосуда. Закон идеального газа в мкт.
- •33. Температура в мкт(31 вопрос). Средняя энергия молекул. Среднеквадратичная скорость молекул.
- •34. Число степеней свободы механической системы. Число степеней свободы молекул. Закон равнораспределения энергии по степеням свободы молекулы.
- •35. Работа, совершаемая газом при изменениях его объема. Графическое представление работы. Работа в изотермическом процессе.
- •37.Первое начало тд. Применение первого начала к различным изопроцессам.
- •38. Теплоемкость идеального газа. Уравнение Майера.
- •39. Уравнение адиабаты идеального газа.
- •40. Политропические процессы.
- •41. Второе начало тд. Тепловые двигатели и холодильники. Формулировка Клаузиуса.
- •42. Двигатель Карно. Кпд двигателя Карно. Теорема Карно.
- •43. Энтропия.
- •44. Энтропия и второе начало тд.
- •45. Энтропия как количественная мера беспорядка в системе. Статистическая интерпретация энтропии. Микро и микросостояния системы.
- •46. Распределение молекул газа по скоростям. Распределение Максвелла.
- •47. Барометрическая формула. Распределение Больцмана.
- •48. Свободные затухающие колебания. Характеристики затухания: коэффициент затухания, время, релаксация, декремент затухания, добротность колебательной системы.
- •49. Электрический заряд. Закон Кулона. Электростатическое поле (эсп). Напряженность эсп. Принцип суперпозиции. Силовые линии эсп.
39. Уравнение адиабаты идеального газа.
Для
0%98%D0%B4%D0%B5%D0%B0%D0%BB%D1%8C%D0%BD%D1%8B%D0%B9_%D0%B3%D0%B0%D0%B7"идеальных
газов,
чью теплоёмкость можно считать постоянной,
в случае
0%9A%D0%B2%D0%B0%D0%B7%D0%B8%D1%81%D1%82%D0%B0%D1%82%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B8%D0%B9_%D0%BF%D1%80%D0%BE%D1%86%D0%B5%D1%81%D1%81"квазистатического
процесса
адиабата имеет простейший вид и
определяется уравнением[
где:
V — его 0%9E%D0%B1%D1%8A%D1%91%D0%BC"объём,
 —
0%9F%D0%BE%D0%BA%D0%B0%D0%B7%D0%B0%D1%82%D0%B5%D0%BB%D1%8C_%D0%B0%D0%B4%D0%B8%D0%B0%D0%B1%D0%B0%D1%82%D1%8B"показатель
адиабаты,
и
—
0%A2%D0%B5%D0%BF%D0%BB%D0%BE%D1%91%D0%BC%D0%BA%D0%BE%D1%81%D1%82%D1%8C"теплоёмкости
газа соответственно при постоянном
давлении и постоянном объёме.
—
0%9F%D0%BE%D0%BA%D0%B0%D0%B7%D0%B0%D1%82%D0%B5%D0%BB%D1%8C_%D0%B0%D0%B4%D0%B8%D0%B0%D0%B1%D0%B0%D1%82%D1%8B"показатель
адиабаты,
и
—
0%A2%D0%B5%D0%BF%D0%BB%D0%BE%D1%91%D0%BC%D0%BA%D0%BE%D1%81%D1%82%D1%8C"теплоёмкости
газа соответственно при постоянном
давлении и постоянном объёме.
С учётом 0%A3%D1%80%D0%B0%D0%B2%D0%BD%D0%B5%D0%BD%D0%B8%D0%B5_%D1%81%D0%BE%D1%81%D1%82%D0%BE%D1%8F%D0%BD%D0%B8%D1%8F_%D0%B8%D0%B4%D0%B5%D0%B0%D0%BB%D1%8C%D0%BD%D0%BE%D0%B3%D0%BE_%D0%B3%D0%B0%D0%B7%D0%B0"уравнения состояния идеального газа уравнение адиабаты может быть преобразовано к виду:
 ,
,
где T — 0%90%D0%B1%D1%81%D0%BE%D0%BB%D1%8E%D1%82%D0%BD%D0%B0%D1%8F_%D1%82%D0%B5%D0%BC%D0%BF%D0%B5%D1%80%D0%B0%D1%82%D1%83%D1%80%D0%B0"абсолютная температура газа. Или к виду:

Поскольку Kвсегда больше 1, из последнего уравнения следует, что при адиабатическом сжатии (то есть при уменьшении V) газ нагревается (T возрастает), а при расширении — охлаждается, что всегда верно и для реальных газов. Нагревание при сжатии больше для того газа, у которого больше коэффициент K.
40. Политропические процессы.
Политропический
процесс, политропный
процесс, изменение состояния физической
системы, при котором сохраняется
постоянной её
0%BA%D0%BD%D0%B8%D0%B3%D0%B8/%D0%91%D0%A1%D0%AD/%D0%A2%D0%B5%D0%BF%D0%BB%D0%BE%D1%91%D0%BC%D0%BA%D0%BE%D1%81%D1%82%D1%8C/"теплоёмкость
(С).
Кривая на термодинамических диаграммах,
изображающая П. п., называется
0%BA%D0%BD%D0%B8%D0%B3%D0%B8/%D0%91%D0%A1%D0%AD/%D0%9F%D0%BE%D0%BB%D0%B8%D1%82%D1%80%D0%BE%D0%BF%D0%B0/"политропой.
Простейшим примером обратимого П. п.
может служить П. п. с
0%BA%D0%BD%D0%B8%D0%B3%D0%B8/%D0%91%D0%A1%D0%AD/%D0%98%D0%B4%D0%B5%D0%B0%D0%BB%D1%8C%D0%BD%D1%8B%D0%B9%20%D0%B3%D0%B0%D0%B7/"идеальным
газом,
определяемый уравнением pVn
=const,
где р
— давление, V
—
объем газа,
 показатель
политропы (Cp
и Cv
— теплоёмкости
газа соответственно при постоянном
давлении и объёме). Используя
0%BA%D0%BD%D0%B8%D0%B3%D0%B8/%D0%91%D0%A1%D0%AD/%D0%A3%D1%80%D0%B0%D0%B2%D0%BD%D0%B5%D0%BD%D0%B8%D0%B5%20%D1%81%D0%BE%D1%81%D1%82%D0%BE%D1%8F%D0%BD%D0%B8%D1%8F/"уравнение
состояния
идеального газа, уравнение политропы
можно записать в ином виде:
показатель
политропы (Cp
и Cv
— теплоёмкости
газа соответственно при постоянном
давлении и объёме). Используя
0%BA%D0%BD%D0%B8%D0%B3%D0%B8/%D0%91%D0%A1%D0%AD/%D0%A3%D1%80%D0%B0%D0%B2%D0%BD%D0%B5%D0%BD%D0%B8%D0%B5%20%D1%81%D0%BE%D1%81%D1%82%D0%BE%D1%8F%D0%BD%D0%B8%D1%8F/"уравнение
состояния
идеального газа, уравнение политропы
можно записать в ином виде:
 const
или
const
или
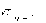 const
(здесь Т
— абсолютная
температура).уравнение П. п. идеального
газа включает, как частные случаи,
уравнения:
0%BA%D0%BD%D0%B8%D0%B3%D0%B8/%D0%91%D0%A1%D0%AD/%D0%90%D0%B4%D0%B8%D0%B0%D0%B1%D0%B0%D1%82%D0%B0/"адиабаты
(С =0,
n =Cp/Cv,
это отношение теплоёмкостей обозначают
g),
0%BA%D0%BD%D0%B8%D0%B3%D0%B8/%D0%91%D0%A1%D0%AD/%D0%98%D0%B7%D0%BE%D0%B1%D0%B0%D1%80%D0%B0/"изобары
(С =
Ср,
n =
0),
0%BA%D0%BD%D0%B8%D0%B3%D0%B8/%D0%91%D0%A1%D0%AD/%D0%98%D0%B7%D0%BE%D1%85%D0%BE%D1%80%D0%B0/"изохоры
(С = Cv,
n =
¥) и
0%BA%D0%BD%D0%B8%D0%B3%D0%B8/%D0%91%D0%A1%D0%AD/%D0%98%D0%B7%D0%BE%D1%82%D0%B5%D1%80%D0%BC%D1%8B/"изотермы
(С = ¥, n
=
1). РаботаАидеального
газа в П. п. против внешнего давления
определяется по формуле
const
(здесь Т
— абсолютная
температура).уравнение П. п. идеального
газа включает, как частные случаи,
уравнения:
0%BA%D0%BD%D0%B8%D0%B3%D0%B8/%D0%91%D0%A1%D0%AD/%D0%90%D0%B4%D0%B8%D0%B0%D0%B1%D0%B0%D1%82%D0%B0/"адиабаты
(С =0,
n =Cp/Cv,
это отношение теплоёмкостей обозначают
g),
0%BA%D0%BD%D0%B8%D0%B3%D0%B8/%D0%91%D0%A1%D0%AD/%D0%98%D0%B7%D0%BE%D0%B1%D0%B0%D1%80%D0%B0/"изобары
(С =
Ср,
n =
0),
0%BA%D0%BD%D0%B8%D0%B3%D0%B8/%D0%91%D0%A1%D0%AD/%D0%98%D0%B7%D0%BE%D1%85%D0%BE%D1%80%D0%B0/"изохоры
(С = Cv,
n =
¥) и
0%BA%D0%BD%D0%B8%D0%B3%D0%B8/%D0%91%D0%A1%D0%AD/%D0%98%D0%B7%D0%BE%D1%82%D0%B5%D1%80%D0%BC%D1%8B/"изотермы
(С = ¥, n
=
1). РаботаАидеального
газа в П. п. против внешнего давления
определяется по формуле
 ,
где индексами 1 и 2 обозначены начальное
и конечное состояния газа. Понятием П.
п. широко пользуются в технической
термодинамике при исследовании рабочих
циклов тепловых двигателей.
,
где индексами 1 и 2 обозначены начальное
и конечное состояния газа. Понятием П.
п. широко пользуются в технической
термодинамике при исследовании рабочих
циклов тепловых двигателей.
