
- •Раздел 5. Окислительно-восстановительные и электрохимические процессы
- •5.1 Электродные потенциалы и гальванический элемент Механизм возникновения электродных потенциалов и определение их величин
- •Уравнение Нернста
- •Гальванические элементы. Химические источники тока
- •5.2 Электролиз
- •Последовательность электродных процессов
- •Законы электролиза
- •5.3. Коррозия и защита металлов
- •Химическая коррозия
- •Электрохимическая коррозия
- •Факторы, влияющие на скорость электрохимической коррозии
- •Защита металлов от коррозии
- •Защита металлов на стадии проектирования
- •Защита от коррозии на стадии изготовления
- •Защита от коррозии на стадии эксплуатации
- •Защита путём уменьшения агрессивности среды
- •Заключение
Защита металлов от коррозии
Защита металлов от коррозионного разрушения состоит из целого комплекса мероприятий по увеличению работоспособности и надёжности изделий из металлов.
Часть этих мер закладывается ещё при проектирования, часть ─ в процессе изготовления, а остальные меры должны быть приняты при эксплуатации конструкций и изделий из металлов. Основные мероприятия по защите металлов от коррозии представлены на рис.5.17.
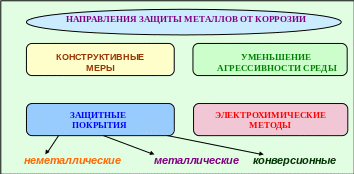
Рис. 5.17 ─ Схема основных направлений защиты металлов от коррозии
Защита металлов на стадии проектирования
При проектировании изделий и конструкций должен быть предусмотрен выбор соответствующего металла или сплава, что определяется не только экономической целесообразностью, но и возможностью обеспечения коррозионной защиты. Детали, подвергающиеся усиленному коррозионному воздействию, изготовляются из легированных (нержавеющих) сталей или из благородных (Au, Ag, Pt) металлов. Конструктор должен предусмотреть рациональные формы частей металлических изделий, допускающих быструю очистку от грязи. Конструкция, по возможности, не должна иметь мест скопления влаги, которая является возбудителем коррозии.
Защита от коррозии на стадии изготовления
В процессе изготовления конструкций и изделий их защищают от коррозии путём нанесения покрытий, изолирующих металл от окружающей среды. Для различных условий коррозии и эксплуатации изолирующие плёнки на поверхности металлов создают различными путями. Защитные покрытия подразделяются на неметаллические, металлические, конверсионные.


Гальванические покрытия наносятся электрохимическим путём. Защищаемое изделие погружают в электролит и подключают к отрицательному полюсу источника постоянного тока, т.е. делают катодом. Анод изготовляют, чаще всего, из того металла, которым хотят покрыть изделие.
В зависимости от электрохимической активности защищаемого металла и защитного слоя различают анодные и катодные покрытия. Например, покрытие железа (стали) цинком будет анодным, потому что при нарушении целостности покрытия и при наличии влаги начинает работать коррозионный элемент, в котором цинк будет анодом.
Покрытие никелем стали будет катодным покрытием, т.к. при нарушении его целостности в коррозионном элементе никель будет катодом, а сталь анодом, т.е. корродировать будет сталь. Поэтому к катодным покрытиям предъявляют более жёсткие требования в отношении их толщины, сплошности и прочности сцепления с защищаемым металлом (рис. 5.18).
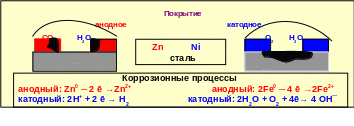
Рис. 5.18 ─ Защитные свойства гальванических покрытий
Конверсионные защитные плёнки представляют собой те или иные химические соединения, образуемые металлом. Чаще всего это оксиды. Оксидные защитные плёнки могут быть получены прямым путём в растворах окислителей. Примером может служить воронение стали, которое ведётся в горячем щелочном растворе (NaOH + NaNO2 + NaNO3).В результате обработки на поверхности изделия образуется плотная, прочная плёнка оксидов железа, предохраняющая его от коррозии. Защитные свойства оксидного слоя могут быть улучшены при наполнении его красителями или минеральным маслом.
Процесс получения оксидных плёнок электрохимическим путём называется анодированием. Таким путём защищяют от коррозии сплавы на основе алюминия.
Фосфатные защитные плёнки применяют как грунт под окраску. Фосфатирование металлической поверхности представляет собой процесс осаждения нерастворимых фосфатов этого металла.
