
- •Ковалентная связь
- •0,6 Для элементов вплоть до неона; 0,75 для элементов вплоть до аргона; 0,75 для элементов вплоть до криптона и 0,8 для элементов вплоть до ксенона.
- •Образование связи
- •Образование связи по донорно-акцепторному механизму
- •Виды ковалентной связи
- •Примеры веществ с ковалентной связью
- •Комплексные соединения
- •Номенклатура
- •Изомерия координационных соединений
- •Пространственная (геометрическая) изомерия
- •Применение
- •Характерные кристаллические решётки
Применение
Комплексные соединения имеют важное значение для живых организмов, так гемоглобин крови образует комплекс с кислородом для доставки его к клеткам, хлорофилл находящийся в растениях является комплексом.
Комплексные соединения находят широкое применение в различных отраслях промышленности. Химические методы извлечения металлов из руд связаны с образованием КС. Например, для отделения золота от породы руду обрабатывают раствором цианида натрия в присутствии кислорода. Метод извлечения золота из руд с помощью растворов цианидов был предложен в 1843 г. русским инженером П. Багратионом. Для получения чистых железа, никеля, кобальта используют термическое разложение карбонилов металлов. Эти соединения — летучие жидкости, легко разлагающиеся с выделением соответствующих металлов.
Широкое применение комплексные соединения получили в аналитической химии в качестве индикаторов.
Многие КС обладают каталитической активностью, поэтому их широко используют в неорганическом и органическом синтезах. Таким образом, с использованием комплексных соединений связана возможность получения многообразных химических продуктов: лаков, красок, металлов, фотоматериалов, катализаторов, надёжных средств для переработки и консервирования пищи и т. д.
Комплесные соединения цианидов имеют важное значение в гальванопластике, так как из обычной соли бывает невозможно получить настолько прочное покрытие как при использовании комплексов.
Если вместо равновесия в реакциях образования комплексов рассматривать обратный процесс – реакции диссоциации комплексов (или реакции обмена лигандов на молекулы растворителя), то соответствующие константы будут носить название ступенчатых констант нестойкости комплексов:
[ML] M + L; K1(нест) = [M] ´ [L] / [ML]
[ML2] [ML] + L ; K2(нест) = [ML] ´ [L] / [ML2]
…….
[MLn] [ML(n-1)] + L; Kn(нест) = [ML(n-1)] ´ [L] / [MLn];
и общих (суммарных) констант нестойкости комплексов:
[ML] M + L; b1(нест) = [M] ´ [L] / [ML]
[ML2] M + 2 L; b2(нест) = [M] ´ [L]2 / [ML2]
[ML3] M + 3 L; b3(нест) = [M] ´ [L]3 / [ML3]
…….
[MLn] M + n L; bn(нест) = [M] ´ [L]n / [MLn]
Ступенчатые и общие константы образования и нестойкости комплексов соотносятся друг с другом как обратные величины:
bn(обр) = 1 / b n(нест); Kn(обр) = 1 / Kn(нест),
поэтому для сравнения прочности комплексов могут использоваться справочные данные как по значениям констант образования, так и констант нестойкости.
Ступенчатое комплексообразование можно проиллюстрировать примером взаимодействия иона Hg2+ (как комплексообразователя) с ионами Cl- (как лигандом):
Hg2+ + Cl- [HgCl]+; K1(обр) = 1,85 . 105
[HgCl]+ + Cl- [HgCl2]; K2(обр) = 3,2 . 107
[HgCl2] + Cl- [HgCl3]- ; K3(обр) = 14
[HgCl3]- + Cl- [HgCl4]2- ; K4(обр) = 10
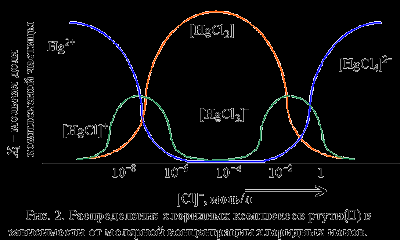
Чем больше концентрация хлоридных ионов, тем с большим координационным числом образуется комплексное соединение. Как только будет достигнуто максимально возможное для данного комплексообразователя координационное число, образование новых комплексных соединений приостанавливается, и при дальнейшем увеличении концентрации лиганда наблюдается постепенное исчезновение в растворе комплексных частиц с меньшими координационными числами.
Из рис. 2 видно, что уже при концентрации хлорид-ионов, равной 1 . 10-5 моль/л, в растворе полностью исчезают катионы Hg2+ и образуются преимущественно нейтральные частицы [HgCl2]. При концентрации хлорид-ионов около 0,1 моль/л в растворе присутствуют комплексы [HgCl2], [HgCl3]- и [HgCl4]2- .
При концентрации ионов Cl- свыше 1 моль/л в растворе присутствуют только тетрахлоромеркурат(II)-ионы [HgCl4]2- , которые довольно легко диссоциируют, отщепляя хлоридный лиганд, но обладают достаточно высокой полной константой образования:
b4(обр) = K1(обр) ´ K2(обр) ´ K3(обр) ´ K4(обр) =
= (1,85 . 105) ´ (3,2 . 107) ´14 ´10 = 8,3 . 1014
Таким образом, полная константа образования дает возможность судить об отсутствии склонности комплекса к полной диссоциации, а ступенчатая константа образования свидетельствует об устойчивости отдельных форм комплексных ионов или нейтральных комплексов.
Как правило, ступенчатые константы образования уменьшаются по мере возрастания числа лигандов. Например, взаимодействие такого комплексообразователя, как ион Cd2+, с молекулами аммиака, выполняющими функции лиганда, протекает поэтапно, с постепенным уменьшением значения ступенчатой константы образования:
Cd2+ + NH3 [Cd(NH3)]2+ ; K1(обр) = 450
[Cd(NH3)]2+ + NH3 [Cd(NH3)2]2+ ; K2(обр) = 126
[Cd(NH3)2]2+ + NH3 [Cd(NH3)3]2+ ; K3(обр) = 27,5
[Cd(NH3)3]2+ + NH3 [Cd(NH3)4]2+ ; K4(обр) = 8,5
[Cd(NH3)4]2+ + NH3 [Cd(NH3)5]2+ ; K5(обр) = 0,47
[Cd(NH3)5]2+ + NH3 [Cd(NH3)6]2+ ; K6(обр) = 0,02
Однако бывают и исключения, например, уже указанные выше хлоридные комплексы ртути(II).
Среди причин закономерного уменьшения значений ступенчатых констант образования с увеличением числа лигандов прежде всего выделяют возрастание пространственных затруднений в размещении вокруг комплексообразователя все большего числа лигандов и электростатическое отталкивание одноименно заряженных лигандов.
Металлическая связь
Металлическая связь — это одновременное существование положительно заряженных атомов и свободного электронного газа.
Механизм металлической связи
Во всех узлах кристаллической решётки расположены положительные ионы металла. Между ними беспорядочно, подобно молекулам газа, движутся валентные электроны, отцепившиеся от атомов при образовании ионов. Эти электроны играют роль цемента, удерживая вместе положительные ионы; в противном случае решётка распалась бы под действием сил отталкивания между ионами. Вместе с тем и электроны удерживаются ионами в пределах кристаллической решётки и не могут её покинуть. Силы связи не локализованы и не направлены. Поэтому в большинстве случаев проявляются высокие координационные числа (например, 12 или 8).
Так, щелочные металлы кристаллизуются в кубической объёмно-центрированной решётке, и каждый положительно заряженный ион щелочного металла имеет в кристалле по восемь ближайших соседей – положительно заряженных ионов щелочного металла (рис.1). Кулоновское отталкивание одноимённо-заряженных частиц (ионов) компенсируется электростатическим притяжением к электронам связывающих звеньев, имеющих форму искажённого сплющенного октаэдра – квадратной бипирамиды, высота которой и рёбра базиса равны величине постоянной трансляционной решётке aw кристалла щелочного металла (рис.2).
Связывающие электроны становятся общими для системы из шести положительных ионов щелочных металлов и удерживают последние от кулоновского отталкивания.
Величина постоянной трансляцонной решётки aw кристалла щелочного металла значительно превышает длину ковалентной связи молекулы щелочного металла, поэтому принято считать, что электроны в металле находятся в свободном состоянии:
Щёлочный металл Li Na K Rb Cs
Постоянная решётка aw,Å [1] 3,5021 4,2820 5,247 5,69 6,084
Длина ковалентной связи, Me2, Å [2] 2,67 3,08 3,92 4,10 4,30
Математическое построение, связанное со свойствами свободных электронов в металле, обычно отождествляют с «поверхностью Ферми», которую следует рассматривать как геометрическое место, где пребывают электроны, обеспечивая основное свойство металла – проводить электрический ток. Таким образом, электрический ток в металлах – это движение сорванных с орбитального радиуса электронов в поле положительно заряженных ионов, находящихся в узлах кристаллической решётки металла. Выход и вход свободных электронов в связывающее звено кристалла осуществляется через точки «0», равноудалённые от положительных ионов атомов.
Свободное движение электронов в металле подтверждено в 1916 году опытом Толмена и Стюарта по резкому торможению быстро вращающейся катушки с проводом – свободные электроны продолжали двигаться по инерции, в результате чего гальванометр регистрировал импульс электрического тока. Свободное движение электронов в металле обусловливает высокую теплопроводность металла и склонность металлов к термоэлектронной эмиссии, происходящей при умеренной температуре.
Колебания ионов кристаллической решётки создаёт сопротивление движению электронов по металлу, сопровождающееся разогревом металла. В настоящее время важнейшим признаком металлов считается отрицательный температурный коэффициент электрической проводимости, то есть понижение проводимости с ростом температуры. С понижением температуры электросопротивление металлов уменьшается, вследствие уменьшения колебаний ионов в кристаллической решётке. В процессе исследования свойств материи при низких температурах Камерлинг-Оннес открывает явление сверхпроводимости. В 1911 году ему удаётся обнаружить уменьшение электросопротивления ртути при температуре кипения жидкого гелия (4,2 К) до нуля. В 1913 году Камерлинг-Оннесу присуждается Нобелевская премия по физике со следующей формулировкой: «За исследование свойств веществ при низких температурах, которые привели к производству жидкого гелия.»
Однако теория сверхпроводимости была создана позднее. В её основе лежит концепция куперовской электронной пары – коррелированного состояния связывающих электронов с противоположными спинамии и импульсами, и, следовательно, сверхпроводимость можно рассматривать как сверхтекучесть электронного газа, состоящего из куперовских пар электронов, через ионную кристаллическую решётку. В 1972 году авторам теории БКШ – Бардину, Куперу и Шрифферу присуждена Нобелевская премия по физике “За создание теории сверхпроводимости, обычно называемой БКШ-теорией».
