
- •1) Електронна будова атома. Електронні, атомні та молекулярні орбіталі. Принципи заповнення електронами атомних орбіталей.
- •1. Міжмолекулярні взаємодії – сильні і слабкі. Хімічний зв’язок. Хімічні пе ретворення – перебудова електронних орбіталей зі зміною і характером заповнення їх електронами.
- •3. Хімічні перетворення – перебудова електронних орбіталей зі зміною і характером заповнення їх електронами. Навести приклади.
- •1. Хімічні сполуки елементів і їх хімічні реакції. Класифікації.
- •3.Атом силіцію. Гібридизація орбіталей. Утворення sp3 -. Sp2 – та sp – гібридизованих орбіталей.
- •3)Органічні речовини і матеріали у поліграфічному виробництві.
- •Існування ізомерів називають явищем ізомерії
- •Історія відкриття
- •Основні типи хімічних реакцій
- •3. Насичені одноосновні карбонові кислоти
- •Фізичні властивості карбонових кислот.
- •Біологічна дія.
- •Добування карбонових кислот.
- •Хімічні властивості карбонових кислот (на прикладі оцтової кислоти).
- •Застосування карбонових кислот.
3. Насичені одноосновні карбонові кислоти
Карбонові
кислоти —
це органічні сполуки, до складу молекул
яких входить карбоксильна
функціональна група:
–![]() Насичені
одноосновні карбонові кислоти містять
одну карбоксильну групу й ординарні
карбон-карбонові зв’язки.
У результаті
взаємного впливу атомів у карбоксильній
групі:
— зв’язок С=О міцніший, ніж в
альдегідній групі;
— зв’язок O–H
менш міцний, ніж у спиртах;
— атом
Гідрогену більш рухливий і
реакційноздатний.
Міжнародні
систематичні назви карбонових кислот
утворюються від назв відповідних
вуглеводнів із додаванням закінчення -ова і
слова кислота.
Наприклад,
метанова кислота.
Загальна формула
насичених одноосновних карбонових
кислот
Насичені
одноосновні карбонові кислоти містять
одну карбоксильну групу й ординарні
карбон-карбонові зв’язки.
У результаті
взаємного впливу атомів у карбоксильній
групі:
— зв’язок С=О міцніший, ніж в
альдегідній групі;
— зв’язок O–H
менш міцний, ніж у спиртах;
— атом
Гідрогену більш рухливий і
реакційноздатний.
Міжнародні
систематичні назви карбонових кислот
утворюються від назв відповідних
вуглеводнів із додаванням закінчення -ова і
слова кислота.
Наприклад,
метанова кислота.
Загальна формула
насичених одноосновних карбонових
кислот
![]() або
або ![]() .
Представники
гомологічного ряду насичених одноосновних
карбонових кислот
.
Представники
гомологічного ряду насичених одноосновних
карбонових кислот
Формула |
Назва за міжнародною систематичною номенклатурою |
Тривіальна назва |
НСООН |
Метанова кислота |
Мурашина кислота |
|
Етанова кислота |
Оцтова кислота |
|
Пропанова кислота |
Пропіонова кислота |
|
Бутанова кислота |
Масляна кислота |
|
Пентанова кислота |
Валеріанова кислота |
Ізомерія
карбонових кислот зумовлена зміною
будови карбонового скелета. Ізомери
утворюються у кислот з більш ніж чотирма
атомами Карбону, починаючи з бутанової
кислоти. Нумерація атомів Карбону
починається з Карбону, що входить до
складу карбоксильної групи. Наприклад:
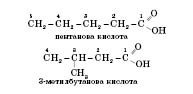
Фізичні властивості карбонових кислот.
Мурашина
кислота —
безбарвна рідина з різким запахом,
температура плавлення ![]() ,
кипіння
,
кипіння ![]() .
Розчиняється у воді в будь-яких
кількостях.
Оцтова
кислота —
за кімнатної температури безбарвна
рідина з різким характерним запахом.
За температури нижчої за
.
Розчиняється у воді в будь-яких
кількостях.
Оцтова
кислота —
за кімнатної температури безбарвна
рідина з різким характерним запахом.
За температури нижчої за ![]() (температура
плавлення) кристалізується і стає схожою
на лід, тому її називають«крижаною»
оцтовою кислотою.
Температура кипіння
(температура
плавлення) кристалізується і стає схожою
на лід, тому її називають«крижаною»
оцтовою кислотою.
Температура кипіння ![]() .
Розчиняється у воді в будь-яких кількостях:
3—9%-й розчин називається оцтом, 70—80%-й
розчин — оцтовою
есенцією.
.
Розчиняється у воді в будь-яких кількостях:
3—9%-й розчин називається оцтом, 70—80%-й
розчин — оцтовою
есенцією.
Біологічна дія.
Кислоти викликають хімічні опіки на шкірі. Мурашина кислота міститься у виділеннях залоз мурах, а також у деяких рослинах (наприклад у листі кропиви).
Добування карбонових кислот.
Загальний
спосіб добування карбонових кислот —
окиснення альдегідів або спиртів із
гідроксигрупою біля першого атома
Карбону:
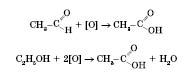
Хімічні властивості карбонових кислот (на прикладі оцтової кислоти).
Властивості,
подібні до властивостей неорганічних
кислот:
1)
Дисоціація у водних розчинах:
![]() Кислотний
залишок називається ацетат-іоном.
2)
Взаємодія з основами:
Кислотний
залишок називається ацетат-іоном.
2)
Взаємодія з основами:
![]() 3)
Взаємодія з основними оксидами:
3)
Взаємодія з основними оксидами:
![]() 4)
Взаємодія з солями слабкіших
кислот:
4)
Взаємодія з солями слабкіших
кислот:
![]() Властивості,
характерні для карбонових кислот:
5)
Взаємодія з галогенами:
Властивості,
характерні для карбонових кислот:
5)
Взаємодія з галогенами:
![]() Одержана
хлороцтова кислота сильніша за оцтову.
6)
Взаємодія зі спиртами:
Одержана
хлороцтова кислота сильніша за оцтову.
6)
Взаємодія зі спиртами:
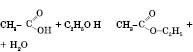 Утворюються складні
естери.
Цей естер називається етилацетат,
або етиловий
естер оцтової кислоти.
Утворюються складні
естери.
Цей естер називається етилацетат,
або етиловий
естер оцтової кислоти.
Застосування карбонових кислот.
Мурашина кислота застосовується як протрава для фарбування шерсті, консервант фруктових соків і силосу, використовується для дезінфекції місткостей у харчовій промисловості, у хімічних синтезах. Оцтова кислота застосовується для добування пластмас, барвників, ліків, штучних волокон, кіноплівки в хімічних синтезах. Вона використовується як приправа до їжі, для консервації овочів. Солі оцтової кислоти використовують для фарбування тканин, а також для боротьби зі шкідниками сільського господарства.
