
- •Химические свойства кислот и оснований.
- •Номенклатура и химические свойства солей.
- •Комплексные соединения: номенклатура, состав и химические свойства.
- •Ионообменные реакции с участием осадков и газов.
- •5. Ионообменные реакции с участием слабых электролитов и комплексных ионов.
- •Степень окисления. Окислительно-восстановительные реакции.
- •Гидролиз соли, образованной сильной кислотой и слабым основанием. Степень гидролиза
- •Гидролиз соли, образованной слабой кислотой и сильным основанием.
- •Гидролиз соли, образованной слабой кислотой и слабым основанием.
- •Случаи полного гидролиза.
- •Термохимия. Тепловой эффект реакции. Термохимические уравнения. Закон Гесса.
- •Термохимия. Энтальпия образования реагента. Вычисление теплового эффекта.
- •Химическая термодинамика. Функции процесса и состояния. Энтропия. Энергия Гиббса.
- •Химическая термодинамика. Определение направления протекания реакциипо изменению её энергии Гиббса. Энтальпия образования реагента.
- •Химическое равновесие. Константа равновесия гомогенных и гетерогенных реакций.
- •Химическое равновесие. Принцип ЛеШателье. Смещение равновесия при изменении температуры.
- •Химическое равновесие. Принцип ЛеШателье. Смешение равновесия при изменении общего давления.
- •Химическое равновесие. Принцип ЛеШателье. Смещение равновесия
- •Равновесия в растворах электролитов. Сильные и слабые электролиты.
- •Равновесия в растворах электролитов. Степень иконстанта диссоциации слабого электролита.
- •Равновесия в растворах электролитов. Ионное произведение воды. Водородный показатель.
- •Равновесия в растворах электролитов. Произведение растворимости.
- •Равновесия в растворах электролитов. Константы нестойкости комплексного иона.
- •Химическая кинетика. Зависимость скорости реакции от температуры.
- •Химическая кинетика. Зависимость скорости реакции от концентрации реагирующих веществ. Молекулярность и порядок реакции. Лимитирующая стадия реакции.
- •26 Химическая кинетика применительно к гетерогенным системам.
- •Химическая кинетика. Гомогенный и гетерогенный катализ. Автокатализ.
- •Электрохимия. Уравнение Нернста. Потенциал металлического электрода.
- •Электрохимия. Водородный электрод и ряд напряжений.
- •Электрохимия. Уравнение Нернста.
- •31. Электрохимия. Гальванический элемент.
Электрохимия. Водородный электрод и ряд напряжений.
Электрохимия – естественнонаучная дисциплина, которая изучает физико-химические свойства ионных растворов и расплавов, а также явления, которые протекают на границе раздела фаз с участием заряженных частиц.
Стандартный водоро́дныйэлектро́д — электрод, использующийся в качестве электрода сравнения при различных электрохимических измерениях и в гальванических элементах. Водородный электрод (ВЭ) представляет собой пластинку или проволоку из металла, хорошо поглощающего газообразный водород (обычно используют платину или палладий), насыщенную водородом (при атмосферном давлении) и погруженную в водный раствор, содержащийионы водорода. Потенциал пластины зависит[уточнить] от концентрации ионов Н+ в растворе. Электрод является эталоном, относительно которого ведется отсчет электродного потенциала определяемой химической реакции. При давлении водорода 1 атм., концентрации протонов в растворе 1 моль/л и температуре 298 К потенциал ВЭ принимают равным 0 В. При сборке гальванического элемента из ВЭ и определяемого электрода, на поверхности платины обратимо протекает реакция:
2Н+ + 2e− = H2
то есть, происходит либо восстановление водорода, либо его окисление — это зависит от потенциала реакции, протекающей на определяемом электроде. Измеряя ЭДС гальванического электрода при стандартных условиях (см. выше) определяют стандартный электродный потенциал определяемой химической реакции.
ВЭ применяют для измерения стандартного электродного потенциала электрохимической реакции, для измерения концентрации (активности) водородных ионов, а также любых других ионов. Применяют ВЭ так же для определения произведения растворимости, для определения констант скорости некоторых электрохимических реакций.
[править]Устройство
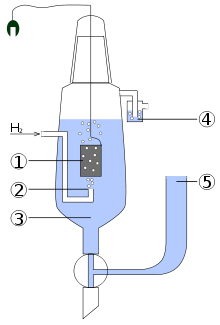

Схема стандартного водородного электрода:
Платиновый электрод.
Подводимый газообразный водород.
Раствор кислоты (обычно HCl), в котором концентрация H+ = 1 моль/л.
Водяной затвор, препятствующий попаданию кислорода воздуха.
Электролитический мост (состоящий из концентрированного р-ра KCl), позволяющий присоединить вторую половину гальванического элемента.
Электрохимический ряд активности (ряд напряжений, ряд стандартных электродных потенциалов) металлов — последовательность, в которой металлы расположены в порядке увеличения их стандартных электрохимических потенциалов φ0, отвечающих полуреакции восстановления катиона металла Men+: Men+ + nē → Me
Li→Rb→K→Ba→Sr→Ca→Na→Mg→Al→Mn→Zn→Cr→Fe→Cd→Co→Ni→Sn→Pb→H→Sb→Bi→Cu→Hg→Ag→Pd→Pt→Au |
Ряд напряжений характеризует сравнительную активность металлов в окислительно-восстановительных реакциях в водных растворах.
Электрохимия. Уравнение Нернста.
Потенциал окислительно-восстановительного электрода.
Электрохимия – естественнонаучная дисциплина, которая изучает физико-химические свойства ионных растворов и расплавов, а также явления, которые протекают на границе раздела фаз с участием заряженных частиц.
Уравнение Нернста — уравнение, связывающее окислительно-восстановительный потенциал системы с активностями веществ, входящих в электрохимическое уравнение, и стандартными электродными потенциалами окислительно-восстановительных пар.
Вывод уравнения Нернста
,
где
— электродный потенциал, — стандартный электродный потенциал, измеряется в вольтах;
— универсальная газовая постоянная, равная 8.31 Дж/(моль·K);
— абсолютная температура;
— постоянная Фарадея, равная 96485,35 Кл·моль−1;
— число моль электронов, участвующих в процессе;
и — активности соответственно окисленной и восстановленной форм вещества, участвующего в полуреакции.
Если в формулу Нернста подставить числовые значения констант и и перейти от натуральных логарифмов к десятичным, то при получим
Окислительно-восстановительный потенциал (редокс-потенциал от англ. redox — reduction-oxidationreaction, Eh или Eh) — мера способности химического вещества присоединять электроны (восстанавливаться[1]). Окислительно-восстановительный потенциал выражают в милливольтах (мВ). Примером окислительно-восстановительного электрода: Pt/Fe3+,Fe2+ Окислительно-восстановительный потенциал определяют как электрический потенциал, устанавливающийся при погружении платины или золота (инертный электрод) в окислительно-восстановительную среду, то есть в раствор, содержащий как восстановленное соединение (Ared), так и окисленное соединение (Aox). Если полуреакцию восстановления представить уравнением:
Aox + n·e− → Ared,
то количественная зависимость окислительно-восстановительного потенциала от концентрации (точнее активностей) реагирующих веществ выражается уравнением Нернста.
Окислительно-восстановительный потенциал определяют электрохимическими методами с использованием стеклянного электрода с red-ox функцией[2] и выражают в милливольтах (мВ) относительно стандартного водородного электродав стандартных условиях.
