
- •1. Происхождение и смысл понятия «Синергетика».
- •2.Отличие подходов в кибернетике и синергетике.
- •3. Что такое Диссипативная структура?
- •4. Что такое Фрактал?
- •5. Принцип порядка Больцмана.
- •6. Два принципа асимметрии природы на примерах преобразования энергии.
- •7 Соотношение взаимности Онсагера
- •8 Теорема о минимуме производства энтропии и вытекающие из нее выводы
- •9. Критерий эволюции.
- •10. Соотношение, связывающее условия термодинамической устойчивости с кинетикой химических реакций.
- •11. Упрощенный механизм образования шестигранных ячеек в модели Бенара.
- •12. Примеры решения задач нелинейной теплопроводности и их практическое применение (значение)
- •13. Составляющие энтропии в реакции окисления железа
- •14. Составляющие энтропии в реакции диссоциации
- •15 Реакция Белоусова-Жаботинского
- •16 Объяснение механизма самоорганизации мартеновской ванны
- •17. Схема механизма колебательности в металлургическом реакторе-осцилляторе.
- •18. Принцип наименьшего принуждения.
- •19 Принцип подчинения
- •20 Примеры микроосцилляторов в металлургии
- •21. Соотношение для критического размера диффузионной области
- •22 Отклонение от равновесия и бифуркации
- •23 Роль флуктуации в механизме самоорганизации
- •2 4 Уравнение динамики популяций, живущих за счет общего ресурса
- •25. Уравнение Ланжевена
- •26. Уравнение популяций типа хищник-жетва
14. Составляющие энтропии в реакции диссоциации
![]() ,
,
Нужна энергия для разрыва связи A<-->A. Не создастся новых связей, отсутствует уменьшение энергии. Если реакция протекает в направлении от чистого соединения А2 к А, то к исходному веществу необходимо подводить энергию. Тогда продукты реакции обладают большей энергией, чем исходное вещество. Энергия рассеивается и вкладывается в хаос.
Протекание
реакции
 2A
вносит в хаос следующие вклады:
2A
вносит в хаос следующие вклады:
• уменьшается рассеивание энергии, т.к. тепловое движение частиц гасится, а энергия использ. для разрушения связи А-А
• происходит увеличение числа частиц в том же объеме давление газа растёт, либо (при P=const) увеличится объем продукты реакции и энергия рассеиваются, энтропия растёт;
• Молекула А2 заменяется на две А и т.к. они по-разному запасают энергию, то их энтропии отличаются. Изменение энтропии может быть + и -, в зав. от специфики хим. соединений. • Если в смеси есть и А и А2, то энтропия выше, т.к. кол-во перестановок молекул больше. Максимум когда 50% А и 50% А2.


Т.о., реакции могут порождать хаос экзотермически, другие эндотермически. В последнем случае неупорядоченность понижается, а взятая извне энергия идет на увеличение хаоса внутри самой системы.
15 Реакция Белоусова-Жаботинского

![]()

16 Объяснение механизма самоорганизации мартеновской ванны
Если взглянуть на некоторые факты (существенное изменение положения максимума зависимости скорость обезуглероживания – содержание углерода при изменении температуры металла, синхронное изменение активности кислорода и температуры во времени и другие) с позиций, что мартеновская ванна обладает свойствами самоорганизации, то момент начала самораскипания можно сопоставить с созреванием условий неравновесного неустойчивого состояния (повышение окисленности шлака и металла, температуры, снижение вязкости шлака), при наличии которых достаточно даже случайной флуктуации, чтобы началось самопроизвольное ускорение процесса обезуглероживания, а затем движение системы к равновесию за счет быстрого расходования ранее накопленных в шлаке ресурсов оксида железа. Самоускорение реакции обезуглероживания обусловливается положительной обратной связью – выделением газообразного продукта реакции, возрастанием работы перемешивания и межфазной поверхности.
Далее наши объяснения механизма в определенной степени солидаризируются с приведенными в работе [18], за исключением несколько преувеличенной роли содержания углерода. По мере уваривания шлака и его гомогенизации уменьшается поверхность для зарождения пузырьков в подшлаковом слое (прекращается поверхностное кипение). Для достаточно интенсивного перехода в нижние слои металла и обеспечения зарождения и роста пузырей на подине должен возрасти градиент концентрации кислорода в металле по отношению к равновесному по реакции D[O] = [O] – [O]pn, а также градиент концентраций кислорода (оксидов железа) в шлаке по отношению к равновесному между шлаком и металлом:
 шлака; L FeO и a FeO
– коэффициент распределения и активность
FeO в шлаке.
шлака; L FeO и a FeO
– коэффициент распределения и активность
FeO в шлаке.
Этот процесс, наряду
с ранее накопленным потенциалом оксидов
железа в шлаке (за счет присадок в
предыдущий период), способствует
нарастанию неравновесного состояния.
В то же время с ростом температуры
металла и степени гомогенизации шлака
создаются более благоприятные условия
для переноса кислорода из шлака в металл,
а также для кинетики реакции
обезуглероживания в локальном объеме
(флуктуации), что приводит к повышению
коэффициентов массоотдачи
![]() в уравнениях турбулентной диффузии
в уравнениях турбулентной диффузии
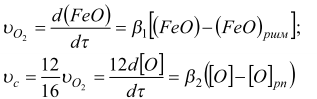
и реакционной поверхности в уравнениях кинетики, что, в свою очередь, ведет к повышению величины υ с и т.д. до тех пор, пока процесс самоускорения не будет уравновешен отрицательными обратными связями: экранирующее действие выделяющегося оксида углерода над ванной, разбавление потенциала кислорода газовой фазы печи, а также уменьшение ресурсов FеО в шлаки.
Влияние же на
уменьшение скорости обезуглероживания
содержания углерода, а через него
накопления кислорода в металле и шлаке,
существенно сказывается, по-видимому,
лишь при содержании углерода ниже
0,3%, когда жидкая ванна в результате
наступающего вслед за самоускорением
замедления процесса обезуглероживания
(исчерпание ранее накопленного
потенциала оксидов железа в шлаке)
переходит в состояние, близкое к
термодинамическому равновесию, а
значение величины
![]() становится
существенным (здесь m – величина, обратная
константе равновесия;
становится
существенным (здесь m – величина, обратная
константе равновесия;
![]() – парциальное давление СО в пузырьках).
– парциальное давление СО в пузырьках).
Таким образом, так
называемая критическая концентрация
углерода, при которой происходит
уменьшение скорости обезуглероживания,
вероятно, соответствует моменту
перехода ванны от неравновесного к
равновесному состоянию. При этом
влияние на этот процесс содержания
углерода является не причинно-следственным,
а опосредствованным (линейная корреляция
содержания углерода и в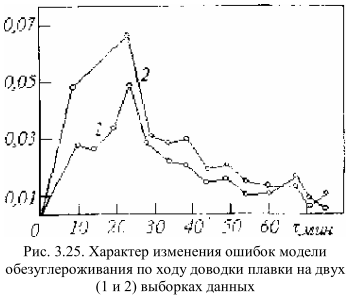 ремени
при С > 0,3 %).
ремени
при С > 0,3 %).
Это подтверждается характером графиков зависимости скорости обезуглероживания от времени с момента начала чистого кипения, которая практически повторяет аналогичную зависимость от содержания углерода, синхронным изменением во времени графиков температуры металла и активности кислорода, «плаванием» максимума зависимости υ с от С в пределах от 0,2 до 0,45 % С при изменении перегрева металла над температурой плавления от 50 до 100 °С [19], изменением момента вскипания ванны при даче присадок. Интересные результаты ч этом плане получены при проверке адекватности статической модели обезуглероживания, основанной на балансе кислорода в газовой фазе и ванне мартеновской печи. Как видно из рис. 3.25, на 20-30 минутах от начала чистого кипения наблюдается весьма характерный и хорошо воспроизводящийся от выборки к выборке «горб» на графике зависимости ошибки модели по времени, что можно объяснить, повидимому, созреванием к этому моменту условий для самораскипания ванны. Если сопоставить временную координату со среднестатистическим содержанием углерода, то оказывается, что этому моменту соответствует значение содержания углерода порядка 0,4%.
Влияние на самораскипание ванны состояния системы шлак – металл и управляющих воздействий, наносимых в предыдущие моменты времени, можно проиллюстрировать приведенными ниже результатами наших исследований по определению вероятности момента вскипания мартеновской ванны. Суть их сводится к анализу выборки только тех плавок, на которых зафиксировано интенсивное вскипание, в предположении, что именно на них наиболее ярко выражены условия, при которых это явление возникает. Наибольшее число плавок выборки приходится на интервал времени 25-30 минут от начала чистого кипения, т.е. в момент, к которому шлак достаточно хорошо уваривается. Эти плавки характеризуются содержанием FеО в шлаке не ниже 15 %, а распределение их вероятности с увеличением (FеО) характеризуется монотонно возрастающей зависимостью. Гистограмма распределения этих плавок по температуре охватывает практически весь температурный диапазон периода чистого кипения, но имеет явно выраженный экстремум с максимумом при 1575 – 1580 °С. Положительное влияние повышенной температуры на увеличение вероятности вскипания безусловно. Снижение же количества вскипаний при Т m > 1580 °С свидетельствует только о том, что это явление, а следовательно, и благоприятные для его возникновения условия создаются и реализуются несколько раньше. Аналогичный характер имеет кривая распределения в зависимости от [С], максимум которой приходится на значение 0,40 – 0,50 %.
