
- •Рівномірний рух
- •Розділи механіки:
- •I закон Ньютона:
- •Література:
- •Розподіл Больцмана.
- •Контрольні питання:
- •Література:
- •П ровідники
- •Контрольні питання:
- •Література:
- •Тема: Електромагнітна індукція. Самоіндукція. Рівняння Максвелла
- •Контрольні питання:
- •Контрольні питання:
- •Контрольні питання:
- •Тема: Електромагнітні коливання. Змінний струм. План:
- •Контрольні питання:
- •Тема: Дифракція хвиль. План:
- •Контрольні питання:
- •Тема: Поляризація світла План:
- •Контрольні питання:
- •Тема: Квантова фізика. Фотоефект. План:
- •Контрольні питання:
- •Тема: Рентгенівське випромінювання. Ефект Комптона. Закономірності випромінювання. План:
- •Контрольні питання:
- •Тема: Корпускулярно- хвильовий дуалізм. План:
- •Контрольні питання:
- •Література:
- •Тема: Атомне ядро План:
- •Контрольні питання:
Контрольні питання:
1. В чому полягають суперечності класичної фізики?
2. Що таке квант?
3. Як називають частинки світла?
4. Чому дорівнює енергія фотона червоного світла?
5. Яке явище називають фотоефектом? Види фотоефекта.
6. Сформулюйте закони зовнішнього фотоефекта. Поясніть їі закони, застосовуючи теорію Ейнштейна.
Література :
І.М. Кучерук, І.Т. Горбачук, П.П. Луцик Загальний курс фізики т.3, р.9, § 1 – 4.
Тема: Атомна фізика.
План:
1. Експериментальне обґрунтування основних квантових ідей.
2. Обгрунтування ідей квантування (дискретності): досліди Штерна і Герлаха, правило частот Бора. *
3. Лінійчастий спектр атомів і молекул.*
4. Принцип відповідності.*
5. Фотон.
1. У 1885р. швейцарським фізиком Бальмером була відкрита певна закономірність при спостереженні випромінювання атома водню. Він показав, що довжини хвиль 4-ох ліній видимої частини спектра можна подати за допомогою емпіричної формули
![]() ,
де
,
де
![]() =3645,6
=3645,6![]() м
м
![]()
У практичній спектроскопії частіше
користувалися хвильовим числом
![]() -кількістю
довжин хвиль на 1 см.
-кількістю
довжин хвиль на 1 см.
![]()
![]()
![]() - енергія іонізації атома водню.
- енергія іонізації атома водню.
![]() 10967734,5м
10967734,5м![]()
Сукупність спектральних ліній, які у своїй послідовності і в розподілі інтенсивності виявляють певну закономірність, називають спектральною серією.
У 1920р. Р.Вуд виявив 22 лінії серії Бальмера, тепер виявлено 37.
Формула Бальмера-Рідберга
![]()

2. Постулати Бора:
Атомна система може знаходитися в особливих стаціонарних станах, які характеризуються певним дискретним значенням енергії
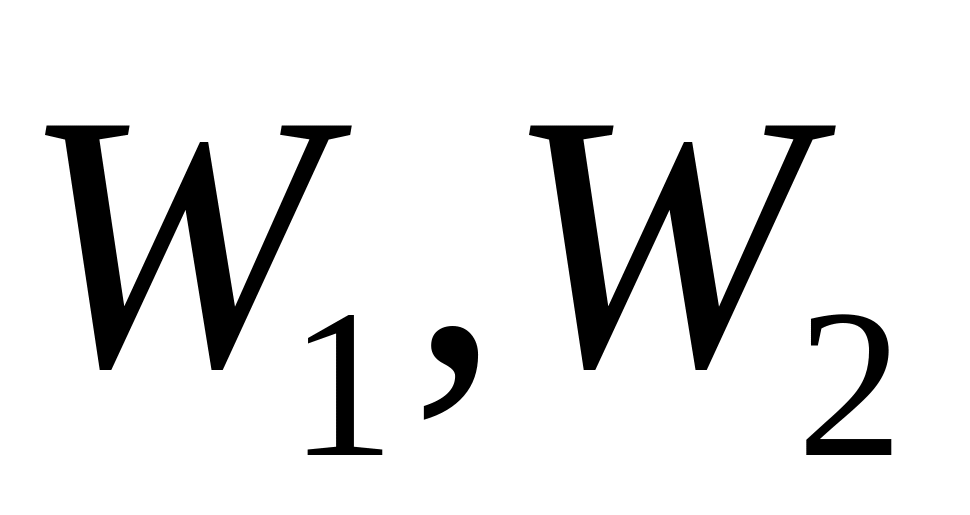 ,
….В стаціонарному стані атом не
випромінює.
,
….В стаціонарному стані атом не
випромінює.При переході із одного стаціонарного стану в інший атом випромінює або поглинає квант електромагнітної енергії.
![]()
Правило квантування
![]() :
:
Момент імпульса електрона може мати
тільки дискретні значення (
![]() =1,2,3,
…)
=1,2,3,
…)
3. Модель атома Бора
![]() (1)
(1)
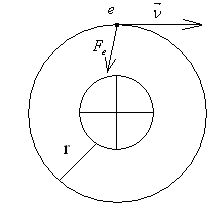
![]() (2)
(2)
![]() - радіус орбіти електрона
- радіус орбіти електрона
![]() м=0,53А
м=0,53А
![]()
![]()
![]()
![]()
![]()
![]()
![]()
Теорія Бора дала можливість з’ясувати фізичний зміст квантових чисел та виникнення спектральних ліній. Вона була перехідним етапом на шляху до створення сучасной теорії атомних явищ. Ця теорія може на якісному рівні пояснювати будову і випромінювання елементів першої групи таблиці Менделєєва.
4. Принцип відповідності
Створюючи свою теорію , Бор керувався
важливою ідеєю наступності в розвитку
фізичних теорій. Цю ідею він створював
стосовно співвідношення між його теорією
атома та класичною механікою і назвав
її принципом відповідності. Згідно
з принципом відповідності при досить
великих значеннях квантових чисел (![]() )
квантові співвідношення переходять у
класичні. За цим принципом будь-яка нова
теорія не заперечує попередню,основану
на експериментах, а включає її в себе і
вказує лише межі її застосування .
)
квантові співвідношення переходять у
класичні. За цим принципом будь-яка нова
теорія не заперечує попередню,основану
на експериментах, а включає її в себе і
вказує лише межі її застосування .
5. Досліди Франка і Герца (перевірка теорії Бора)
М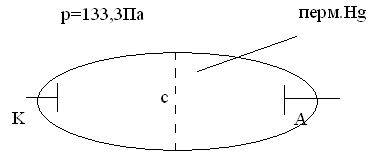 іж
катодом і анодом плавно змінюється
напруга. Між С і А
іж
катодом і анодом плавно змінюється
напруга. Між С і А
![]() .
Електрони, що випромінюються катодом,
прискорюються і створюють струм, що
реєструє чутливий гальванометр. У
досліді після першої різкої зміни струму
виникало
.
Електрони, що випромінюються катодом,
прискорюються і створюють струм, що
реєструє чутливий гальванометр. У
досліді після першої різкої зміни струму
виникало
![]() ртутних парів.
ртутних парів.
![]()
![]() сили струму повторюється при напругах
4,9В, 9,8В.
сили струму повторюється при напругах
4,9В, 9,8В.
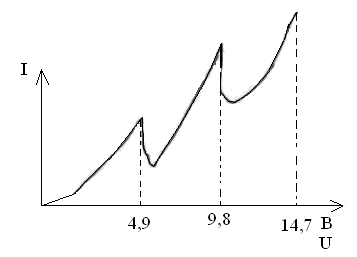
Висновок: за наявності дискретних рівнів атом може отримувати енергію тільки певними порціями.
6. Фотон – частинка світла.
![]()
![]()
![]()
Фотон -безмасова частина (маса спокою фотона=0)
Контрольні питання:
1. Що таке спектр? Види спектрів.
2. Сформулюйте постулати Бора.
3. Побудуйте модель атома Гідрогену, застосувавши теорію Бора.
4. Як ви розумієте принцип відповідності?
5. З якою метою були проведені досліди Франком та Герцем?
6. Які характеристики має фотон?
Література:
І.М. Кучерук, І.Т. Горбачук, П.П. Луцик Загальний курс фізики т.3, р.13, § 1 – 5.
