
- •1. Термодинамика. Метод и законы. Основные понятия и определения термодинамики.
- •Основные понятия и определения
- •2. Параметры состояния и уравнения состояния. Отличия между идеальным и реальным газом.
- •3. Термодинамическая и потенциальная работы."p-V" координаты.
- •4. Теплоемкость. Определение теплоемкости веществ.
- •5. Диаграмма фазовых состояний. Критические параметры.
- •7. Смеси идеальных и реальных газов
- •8. Математическое выражение первого начала термодинамики
- •10. Первое начало термодинамики в аналитической форме.
- •11. Первое начало термодинамики для идеальных газов.
- •12. Принцип существования энтропии идеального газа.
- •13. Процессы изменения состояния (изобара, изохора, изотерма и адиабата) в "p-V" и "t-s" координатах.
- •14. Политропа с постоянным и переменным показателем. Показатели политропы.
- •15. Работа в термодинамических процессах простых тел.
- •16. Теплообмен в термодинамических процессах простых тел
- •17. Процессы изменения состояния идеального газа
- •18. Работа и теплообмен в политропных процессах идеальных газов.
- •19.Круговые процессы. Кпд и холодильный коэффициент.
- •20. Обратимый цикл Карно. Кпд и холодильный коэффициент.
- •21. Математическое выражение второго начала термостатики.
- •22. Следствия второго начала термостатики. "t-s" координаты.
- •23. Математическое выражение второго начала термодинамики.
- •28. Истечение несжимаемых жидкостей
- •29. Особенности истечения сжимаемой жидкости. Кризис истечения.
- •31. Дросселирование. Эффект Джоуля-Томсона
28. Истечение несжимаемых жидкостей
Соотношения для определения удельной потенциальной работы несжимаемой жидкости в обратимых процессах истечения (1-2, 0-2) имеют следующий вид:
![]() ;
;
![]() .
.
С
учетом соотношений, теоретическая
линейная скорость истечения несжимаемой
жидкости в выходном сечении сопла (с2)
может быть определена из следующих
соотношений:
![]() ;
;
![]() .
.
Массовая
скорость потока несжимаемой жидкости
на выходе из сопла
![]()
29. Особенности истечения сжимаемой жидкости. Кризис истечения.
31. Дросселирование. Эффект Джоуля-Томсона
Эффект падения давления потока рабочего тела в процессе преодоления им (потоком) местного сопротивления называется дросселированием.
Уравнение первого начала термодинамики для потока по балансу рабочего тела
![]() примет
вид H2
- H1
= 0
или
примет
вид H2
- H1
= 0
или
![]() .
.
Это значит, что рассматриваемый процесс дросселирования является процессом изоэнтальпийным: энтальпия рабочего тела до дросселя численно равна энтальпии рабочего тела после дросселя. При течении внутри дросселя энтальпия газа или пара меняется.
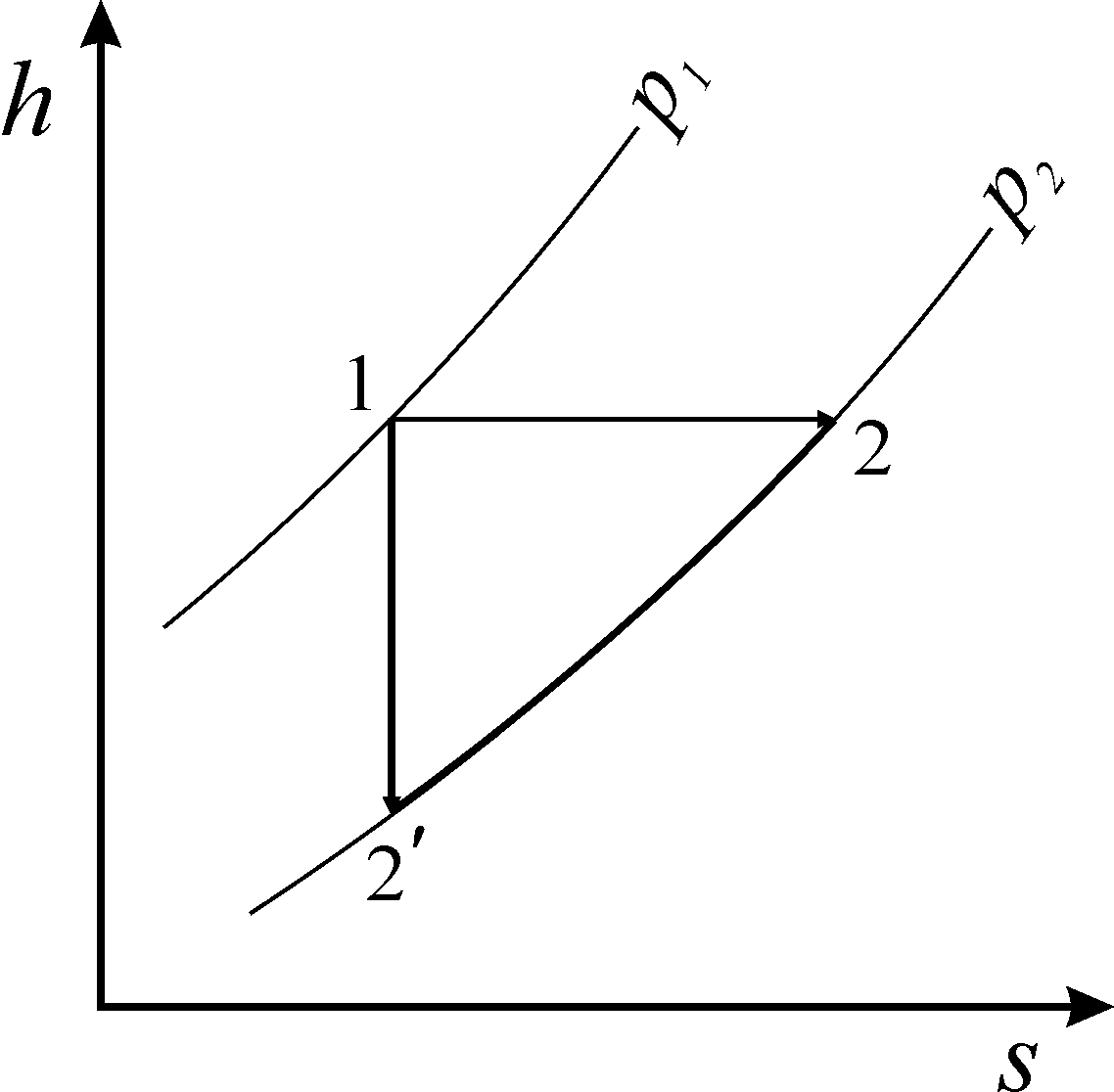
Рис. 26. Процесс дросселирования в h-s диаграмме
![]() .
.
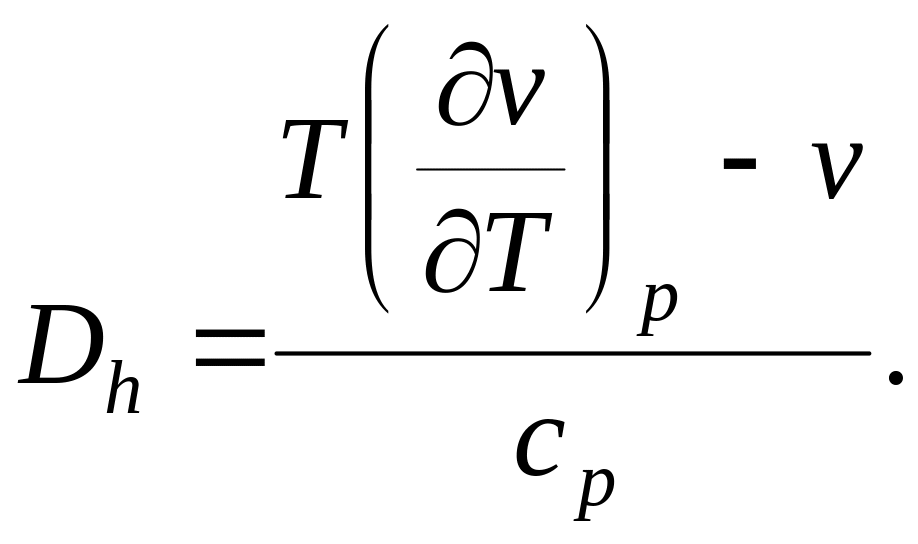
1. Дроссель–эффект положительный (Dh > 0), в этом случае процесс дросселирования сопровождается снижением температуры рабочего тела (dT<0);
2. Дроссель–эффект отрицательный (Dh < 0), в этом случае процесс дросселирования сопровождается повышением температуры рабочего тела (dT>0);
3. Дроссель–эффект равен нулю (Dh = 0), если в процессе дросселирования температура рабочего тела не изменяется. Нулевой дроссель-эффект наблюдается при дросселировании идеального газа.
