
- •1. Термодинамика. Метод и законы. Основные понятия и определения термодинамики.
- •Основные понятия и определения
- •2. Параметры состояния и уравнения состояния. Отличия между идеальным и реальным газом.
- •3. Термодинамическая и потенциальная работы."p-V" координаты.
- •4. Теплоемкость. Определение теплоемкости веществ.
- •5. Диаграмма фазовых состояний. Критические параметры.
- •7. Смеси идеальных и реальных газов
- •8. Математическое выражение первого начала термодинамики
- •10. Первое начало термодинамики в аналитической форме.
- •11. Первое начало термодинамики для идеальных газов.
- •12. Принцип существования энтропии идеального газа.
- •13. Процессы изменения состояния (изобара, изохора, изотерма и адиабата) в "p-V" и "t-s" координатах.
- •14. Политропа с постоянным и переменным показателем. Показатели политропы.
- •15. Работа в термодинамических процессах простых тел.
- •16. Теплообмен в термодинамических процессах простых тел
- •17. Процессы изменения состояния идеального газа
- •18. Работа и теплообмен в политропных процессах идеальных газов.
- •19.Круговые процессы. Кпд и холодильный коэффициент.
- •20. Обратимый цикл Карно. Кпд и холодильный коэффициент.
- •21. Математическое выражение второго начала термостатики.
- •22. Следствия второго начала термостатики. "t-s" координаты.
- •23. Математическое выражение второго начала термодинамики.
- •28. Истечение несжимаемых жидкостей
- •29. Особенности истечения сжимаемой жидкости. Кризис истечения.
- •31. Дросселирование. Эффект Джоуля-Томсона
10. Первое начало термодинамики в аналитической форме.
Изменения внутренней энергии и энтальпии простого тела, как функций состояния, в элементарных процессах являются полными дифференциалами и определяются соотношениями
![]() ;
;
![]() .
.
Для
изохорного процесса (![]() )
)
![]() ,
,
а
для изобарного процесса (
)
![]() .
.
![]() .
.
- первым началом термодинамики для простых тел в аналитической форме.
11. Первое начало термодинамики для идеальных газов.
Уравнение первого начала термодинамики для идеального газа по балансу рабочего тела в дифференциальной и интегральной формах:
![]() ;
;
![]() ..
..
12. Принцип существования энтропии идеального газа.
![]() .
.
Правая
часть уравнения представляет собой
сумму полных дифференциалов. Это значит,
что и соотношение
![]() есть полный дифференциал некоторой
функции состояния идеального газа
(s),
называемой удельной энтропией.
есть полный дифференциал некоторой
функции состояния идеального газа
(s),
называемой удельной энтропией.
Изменение удельной энтропии в элементарном процессе представляет собой полный дифференциал и определяется соотношением
![]() .
.
Из уравнения после интегрирования получим, что изменение удельной энтропии идеального газа в процессе (1-2) может быть найдено из соотношения
![]() =
=
![]() .
.
13. Процессы изменения состояния (изобара, изохора, изотерма и адиабата) в "p-V" и "t-s" координатах.
При изучении термодинамических процессов определяются:
1) закономерность изменения параметров состояния рабочего тела, то есть выводится уравнение процесса или дается его графическое изображение в координатах p-v, p-T, Т-s и т.д.;
2) параметры состояния системы в начальной и конечной точках процесса;
3) численные значения работы и теплообмена в процессе;
4) изменение значений внутренней энергии, энтальпии и энтропии рабочего тела.
Простейшие термодинамические процессы
Простейшими термодинамическими процессами обычно считают изобарный, изохорный и изопотенциальные процессы.
Удельная
термодинамическая и потенциальная
работы в изобарном
![]() ,
,
![]() .
.
Рис.
5. Простейшие термодинамические процессы:
1-2,
1-3
–
изобары; 1-4,
1-5
–
изохоры;
1-6,
1-7
–
изопотенциальные процессы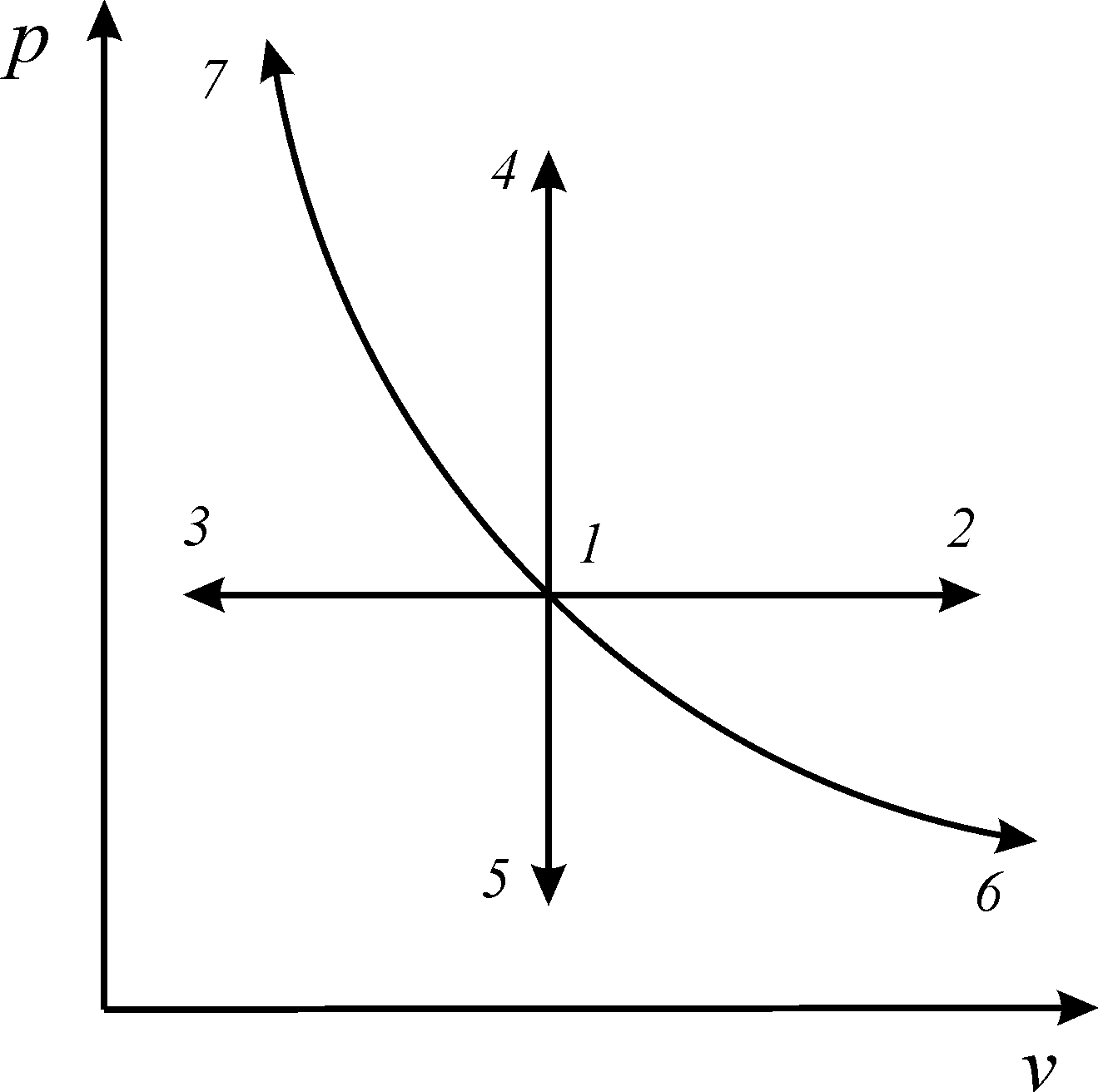
Количество теплоты, подведенной к рабочему телу или отведенной от него в изобарном процессе, определяется из выражения первого начала термодинамики
![]() .
.
Удельная термодинамическая и потенциальная работы в изохорном процессе
![]() ,
,
![]() .
.
Количество теплоты, подведенной к рабочему телу или отведенной от него в изохорном процессе, определяется из выражения первого начала термодинамики
![]() .
.
Удельная термодинамическая и потенциальная работы в изопотенциальном:
![]() =
=
![]() =
=
![]() ;
;
![]() =
=
![]() =
=
![]() =
=
![]() .
.
Количество теплоты, подведенной к рабочему телу или отведенной от него в изопотенциальном процессе определяется из выражения первого начала термодинамики по балансу рабочего тела
![]() .
.
