
- •1. Термодинамика. Метод и законы. Основные понятия и определения термодинамики.
- •Основные понятия и определения
- •2. Параметры состояния и уравнения состояния. Отличия между идеальным и реальным газом.
- •3. Термодинамическая и потенциальная работы."p-V" координаты.
- •4. Теплоемкость. Определение теплоемкости веществ.
- •5. Диаграмма фазовых состояний. Критические параметры.
- •7. Смеси идеальных и реальных газов
- •8. Математическое выражение первого начала термодинамики
- •10. Первое начало термодинамики в аналитической форме.
- •11. Первое начало термодинамики для идеальных газов.
- •12. Принцип существования энтропии идеального газа.
- •13. Процессы изменения состояния (изобара, изохора, изотерма и адиабата) в "p-V" и "t-s" координатах.
- •14. Политропа с постоянным и переменным показателем. Показатели политропы.
- •15. Работа в термодинамических процессах простых тел.
- •16. Теплообмен в термодинамических процессах простых тел
- •17. Процессы изменения состояния идеального газа
- •18. Работа и теплообмен в политропных процессах идеальных газов.
- •19.Круговые процессы. Кпд и холодильный коэффициент.
- •20. Обратимый цикл Карно. Кпд и холодильный коэффициент.
- •21. Математическое выражение второго начала термостатики.
- •22. Следствия второго начала термостатики. "t-s" координаты.
- •23. Математическое выражение второго начала термодинамики.
- •28. Истечение несжимаемых жидкостей
- •29. Особенности истечения сжимаемой жидкости. Кризис истечения.
- •31. Дросселирование. Эффект Джоуля-Томсона
2. Параметры состояния и уравнения состояния. Отличия между идеальным и реальным газом.
Параметры состояния
Параметры состояния - физические величины, характеризующие внутреннее состояние термодинамической системы. Параметры состояния термодинамической системы подразделяются на два класса: интенсивные и экстенсивные. Интенсивные свойства не зависят от массы системы, а экстенсивные - пропорциональны массе.
Термодинамическими параметрами состояния называются интенсивные параметры, характеризующие состояние системы.
К
термодинамическим параметрам состояния
относятся: удельный объем (![]() ),
давление (
),
давление (![]() )
и температура (
)
и температура (![]() ).
).
Удельный
объем (
)
- это объем единицы массы вещества, а
величина, обратная удельному объему,
называется плотностью вещества (![]() )
)
![]() ;
;
![]() ;
;
![]() ,
,
Объем
киломоля вещества или молярный объем
![]() связан с
удельным объемом следующим соотношением:
связан с
удельным объемом следующим соотношением:
![]() .
.
Абсолютное давление ( ) есть предел отношения нормальной составляющей силы к площади, на которую действует эта сила
p
=
![]()
![]() .
.
3. Термодинамическая и потенциальная работы."p-V" координаты.
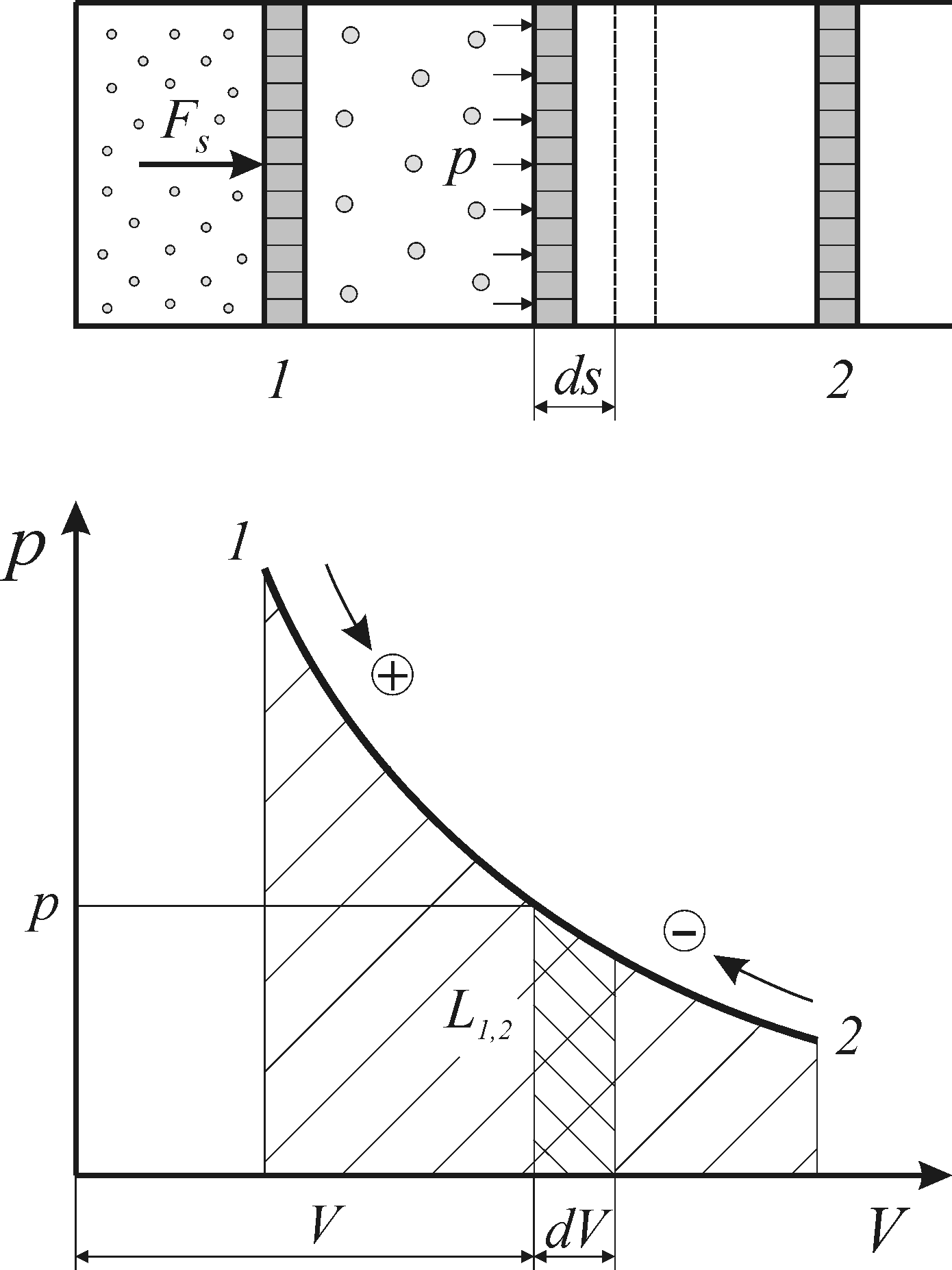
Рис. 1.Термодинамическая работа обратимого изменения объема
Термодинамическая работа
В простейшем случае элементарная работа простых тел определяется в зависимости от величины давления и изменения объема (рис. 1)
![]() ,
,
Удельная элементарная термодинамическая работа обратимого изменения объема
![]() .
.
В частном случае для изобарного процесса (p = idem)
L1,2
=
![]() =
=
![]() ;
l1,2
=
;
l1,2
=
![]() =
=
![]() .
.
Эффективная
работа реального процесса
![]() равна разности обратимой работы изменения
объема
равна разности обратимой работы изменения
объема
![]() и работы необратимых потерь
и работы необратимых потерь
![]()
![]() .
.
Потенциальная (техническая) работа
Потенциальной (технической) работой называется работа по перемещению сплошных масс (газа, пара или жидкости) из области одного давления (p1) в область другого давления (p2), т.е. потенциальная работа - это работа обратимого изменения давления.
Элементарная
потенциальная работа
простого тела
![]() .
.
Удельная
потенциальная работа
в элементарном процессе
![]() .
.
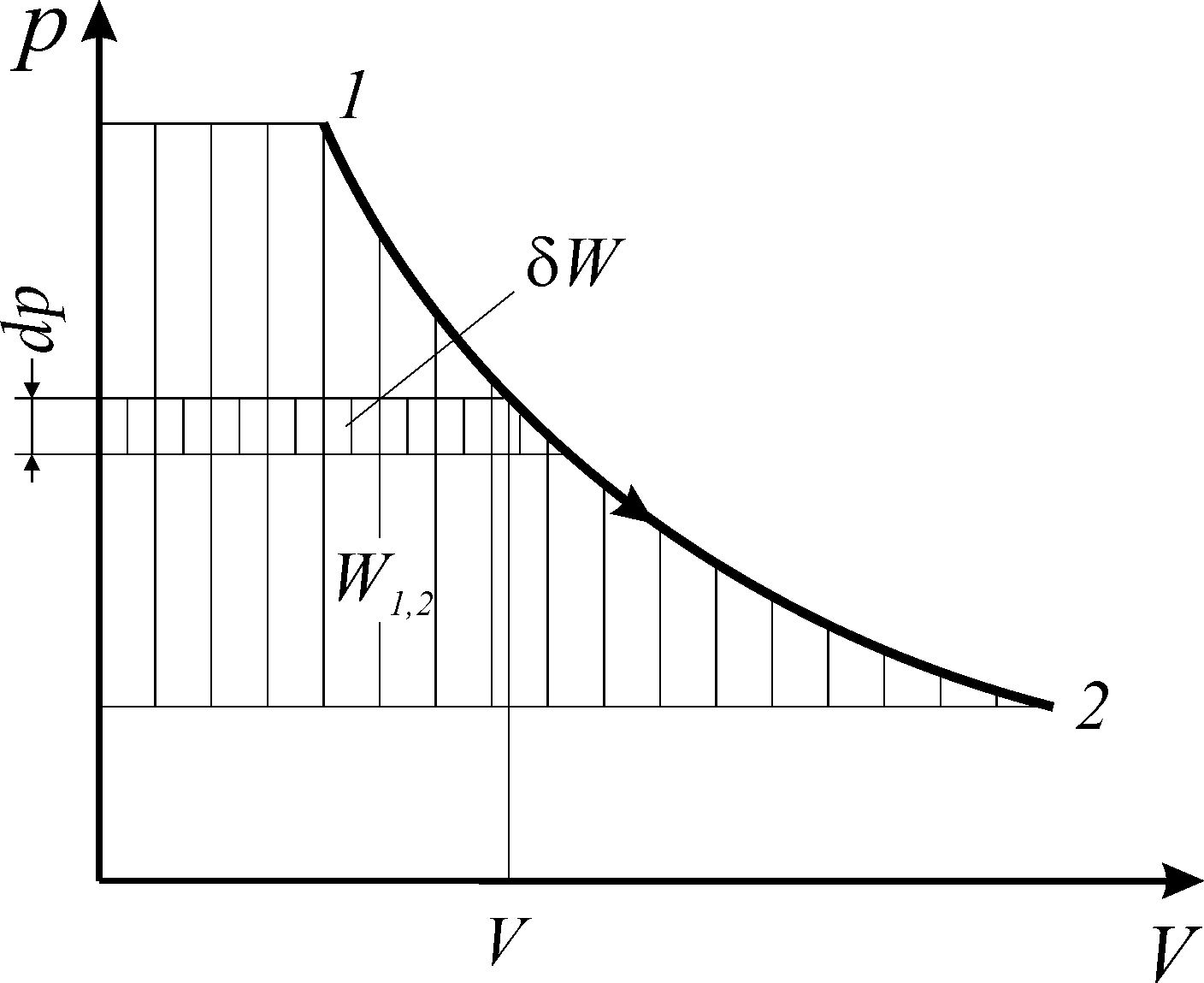
Рис. 2. Потенциальная работа обратимого изменения давления
Для изохорного процесса (v = idem)
![]() ;
;
![]() .
.
Потенциальная
работа в обратимом процессе (![]() )
есть сумма эффективной работы
)
есть сумма эффективной работы
![]() и необратимых потерь работы
и необратимых потерь работы
![]()
![]() =
=
![]() +
.
+
.
Эффективная
термодинамическая работа (
)
простого тела в замкнутом пространстве
и эффективная потенциальная работа (
)
потока непосредственно передаются
внешней системе (![]() или
или
![]() )
и используются для изменения энергии
внешнего положения тела (dEcz)
=
+ dEcz;
=
+
dEcz
.
)
и используются для изменения энергии
внешнего положения тела (dEcz)
=
+ dEcz;
=
+
dEcz
.
Уравнение распределения термодинамической и потенциальной:
![]() ;
;
![]() ,
,
