
- •Днк хромосом
- •Структурная организация хроматина
- •Уровни упаковки генетического материала
- •II. Хроматиновая фибрилла (соленоидный уровень) (супернуклеосомный)
- •III. Интерфазная хромонема (хроматидный или петлевой уровень организации)
- •IV. Метафазная хромосома
- •Реплицирующая молекула днк
- •Суть проблемы концевой недорепликации. А.М. Оловников 1971
- •Расположение буферных теломерных последовательностей на концах хромосом:
- •Удлинение теломер с помощью теломеразы.
- •IV. «Счетная»функция
- •1961 Год Леонард Хейфлик
1961 Год Леонард Хейфлик
Схема культивирования клеток по Хейфлику
Ткань- культура фибробластов человеческого эмбриона.
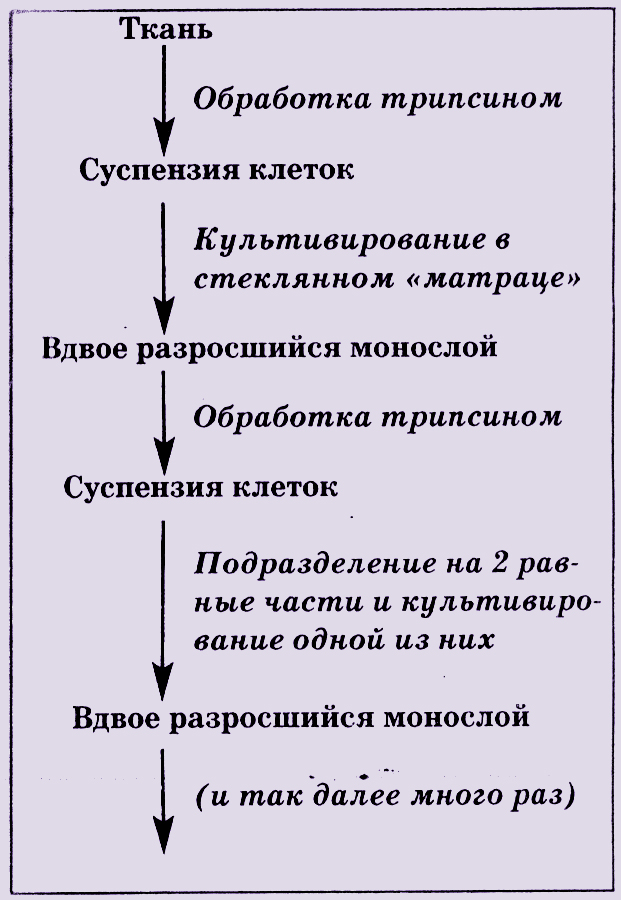
Линия делящихся соматических клеток вовсе не бессмертна;
Старение – это свойство самих клеток, причем оно даже запрограммировано в геноме клетки, поскольку наступает после определенного числа делений.
Это критическое число делений получило название Лимита Хейфлика
Дополнительные аргументы Хейфлика
Чем старше донор, тем меньше число делений. (Если получить фибробласты от взрослого человека, то число делений клетки до гибели оказывается 50)
«Память» о количестве прошедших делений сохраняется, если клетку подвергнуть глубокому замораживанию.
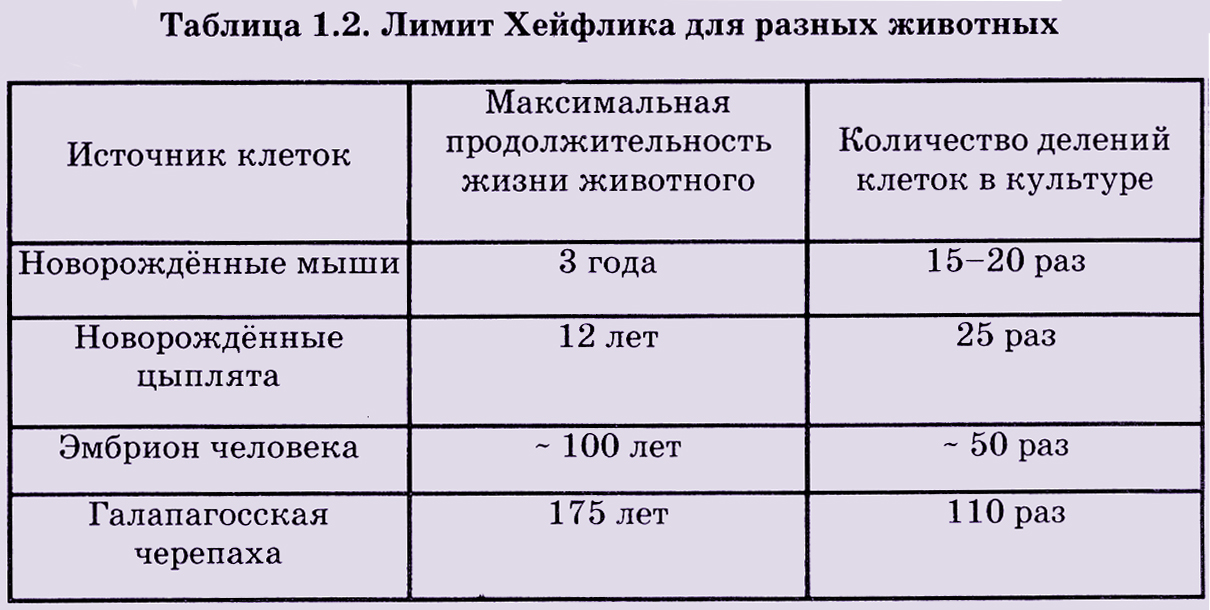
Показательная корреляция – между видовой продолжительностью жизни животного и количеством делений его клеток в культуре.
У клеток, вошедших в фазу III
а) замедляется и меняется морфология клетки,
б) меняются многие биохимические показатели – активности ферментов, интенсивность синтезов и т.д.
Чем больше живут животные данного вида, тем больше делений совершают выделенные из них клетки в in vitro т.е. 50 делений – это видовая характеристика лимита Хейфлика только для человека.
Теломерная теория старения (теория маргинотомии) А.М. Оловников
Предсказание о том, что должен присутствовать специальный механизм поддержания длины теломер.
*Подтверждено открытием теломеразы и альтернативного механизма (АLТ)
Э.Блэкберн
Э.Грайдер (1985)
Предсказание об укорочении теломер в соматических клетках.
** Подтверждено для многих делящихся клеток – в культуре и in vivo.
Предсказание о том, что в зрелых половых клетках, длина теломер не должна зависеть от возраста.
Предсказание о том, что именно укорочение теломер приводит к прекращению делений клеток в культуре.
***Подтверждено экспериментом, в котором лимит Хейфлика преодолен путем введения в клетки гена теломеразы (Джон Шейя; Вундринг Райт 1998)
Предсказание о наличии теломеразы в опухолевых клетках.
Вышесказанное не означает, что теломерная теории на самом деле полноценно описывает старение.
Критика теломерной теории старения
В
 большинстве клеток мышей высокая
активность теломеразы
большинстве клеток мышей высокая
активность теломеразы

 очень длинные теломерные
последовательности
очень длинные теломерные
последовательности
???
мало укорачиваются при делении, а лимит Хейфлика составляет здесь всего 20 делений
Клетки человека, зараженные вирусом ρV40 совершают 20-60 делений сверх лимита Хейфлика, укорочение теломер продолжается. Теломераза отсутствует.
В клетки молочной железы вводят ген теломеразы (TERT)
теломеры удлиняются
но не увеличивается лимит Хейфлика
В культуре эффект Хейфлика проявляется скачкообразно, in vivo – постепенно.
В итоге, остается совершенно неясным, каково же на самом деле предельно допустимое количество делений in vivo для клеток человека.
Предел Хейфлика (если он, действительно присутствует) для различных клеток может быть совершенно различным.
Лимит деления in vivo для различных клеток неизвестен.
Старение in vivo, скорее всего, не связано с приближением делящихся клеток к этому лимиту.
Старение соматических клеток не должно сводиться к выключению в них всего одного гена.
В организме имеется целая совокупность различных защитных систем:
система репарации ДНК,
система теломер и теломераза,
антиоксидантная система (обезвреживающая свободные радикалы)
система шаперонов, восстанавливающая третичную структуру белков при ее нарушении.
Если старение действительно запрограммировано, то программа, скорее всего, состоит в постепенном ослаблении деятельности вышеперечисленных защитных систем.
Таким образом, теломеры и теломераза всего лишь один из элементов единого и гораздо более сложного процесса.
