
- •Функции липидов
- •Роль желчных кислот
- •Гиперлипопротеинемия
- •Метаболизм кетоновых тел.
- •Жирные кислоты
- •Роль полиеновых вжк.
- •Липогенез.
- •Нейтральные жиры.
- •Сфинголипиды. Биологическая роль.
- •Перекисное окисление липидов.
- •Антиоксиданты.
- •Действие перекисей липидов на мембраны.
- •Действие перекиси липидов на белки.
- •Свободно – радикальное окисление.
- •Пол при опухолях.
- •Атеросклероз, ишемическая болезнь сердца (ибс), гипертоническая болезнь.
Липиды - вещества, обладающие общим свойством - нерастворимостью в воде, но существенно отличающиеся по структуре и функциям.
У человека, весом 70 кг содержится примерно 10-12 кг жира.

По физиологическому значению жиры делятся:
Структурные (протоплазматические) участвующие в построении мембран (2-3 кг), например: ФЛ, ХС, Сфинголипиды и др.
Резервные - откладывающийся в виде ТАГ в подкожно-жировой клетчатке, служащей формой депонирования энергии.
Бурый жир - имеющий значение в терморегуляции у грудных детей.
Функции липидов
Структурная.
Энергетическая.
Защитная (от повреждений)
Участие в теплорегуляции.
Образование Н2О (верблюды могут в пустыне обходиться без воды, благодаря жиру в своих горбах).
Растворители для жирорастворимых витаминов. (желчные кислоты)
Фосфолипиды осуществляют транспорт через мембрану.
Гликолипиды участвуют в иммунологических реакциях, в реакцих узнавания гормонов.
Ганглиозиды - связаны с явлениями долгосрочной памяти.
Сфингомиелины - в передаче нервного импульса.
С пищей ежедневно в организм поступает от 80 до 150г липидов, калорийность жира 9 ккал/моль по сравнению с 4,7 ккал/моль у углеводов.
У взрослого человека процесс переваривания и всасывания происходит в 12-перстной кишке при оптимальном рН=8 для действия ферментов.
У грудных детей основной пищей служит молоко, содержащее жиры в эмульгированном виде и переваривание липидов происходит в желудке, рН желудочного сока 5-5,5.
Жиры, проходя ЖКТ расщепляются до своих конечных продуктов.
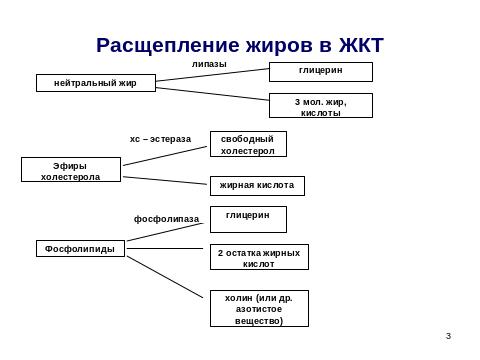
В процессе переваривания и всасывания принимают участие соли желчных кислот, синтезирующиеся в печени из ХС и при этом конъюгируются с таурином или глицином, образуя парные желчные кислоты, например, таурохолевую, гликохолевую.
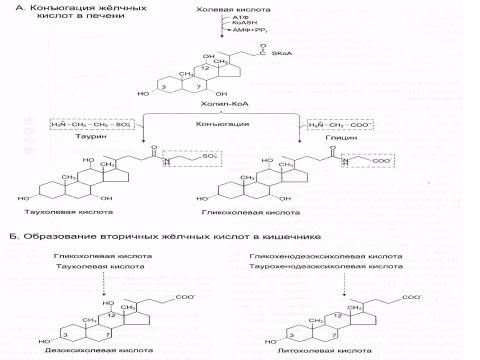
Роль желчных кислот
Эмульгируют жиры
Активируют панкреатическую липазу.
Участвуют во всасывании продуктов распада липидов.
После всасывания продуктов гидролиза жиров в стенке кишечника происходит ресинтез жиров: ТАГ, ЭХС, ФЛ.
Липиды в крови нерастворимы, поэтому для транспорта липидов кровью в организме образуются комплексы липидов с белками – липопротеины. Они имеют сходное строение (слайд).
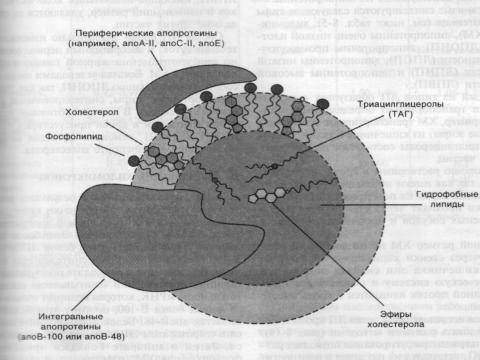
Апобелки – небольшие полипептиды, которые могут свободно переходить от одного ЛП к другому (А, В, С, Е). ЛП выполняют несколько функций:
Формируют структуру липопротеинов.
Взаимодействуют с R на поверхности клеток и т.о. определяют какими клетками будет захватываться данный тип ЛП.
Служат ферментами или активаторами ферментов, действ. на ЛП.
В организме человека синтезируются следующие формы: ХМ, ЛПНП, ЛПОНП, ЛПВП (слайд).
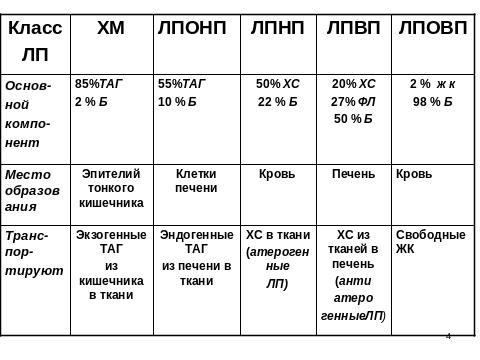
Гиперлипопротеинемия
Различают несколько типов.
Наиболее часто встречаются:
Первый тип: семейная хиломикронемия. У них повышен уровень ТАГ > 200мг/л и ХМ. Плазма крови напоминает молоко, образование ксантом в коже, сухожилиях, в сетчатке глаз.
Второй тип: семейная. Повышение ХС, ТАГ за счет увеличения ЛПНП, увеличена вероятность атеросклероза.
β-окисление – специфический путь катаболизма жирных кислот, при котором происходит отщепление по 2 углеродных атома в виде ацетил-КоА. называется так потому, что реакции окисления происходят у β-углеродного атома.
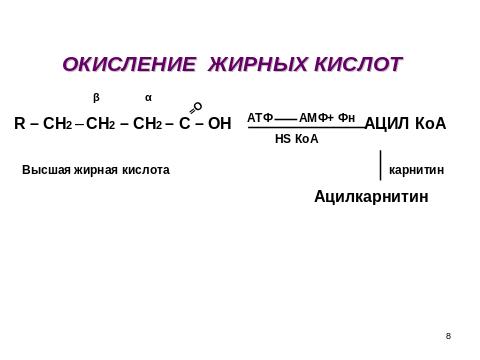
I этап – подготовительный, протекает в цитоплазме. В результате чего происходит активирование высшей жирной кислоты (ацил-КоА). Затем ацил-КоА соединяется с карнитином (слайд), с образованием ацил-карнитина, который транспортируется в митохондрию, где жирная кислота подвергается четырем превращениям за один цикл:
1. Дегидрирование
2. Гидратация
3. Второе дегидрирование
4. Тиолиз
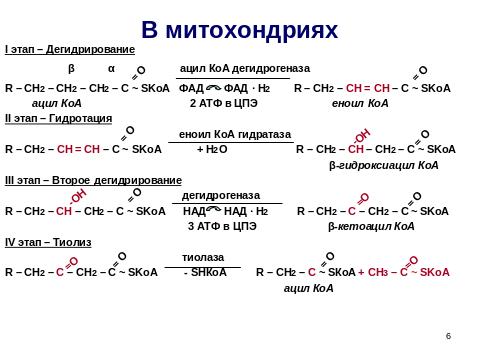

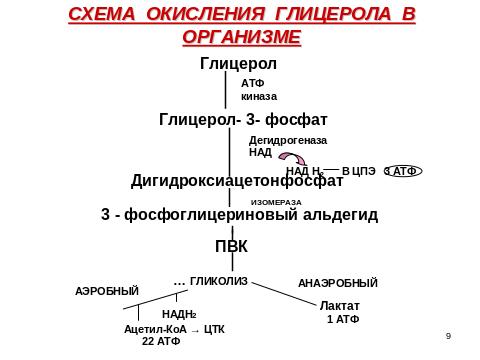
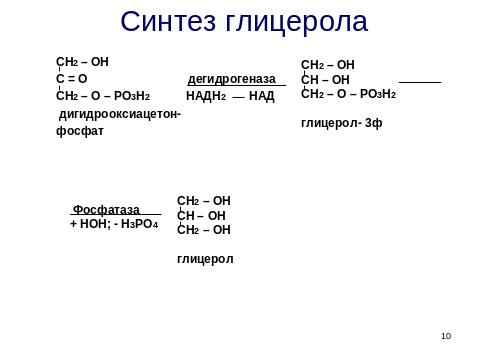
ОБМЕН ФОСФОЛИПИДОВ
К этому классу относятся фосфатидилэтаноламин, фосфатидилсерин, фосфатидилхолин (слайд).
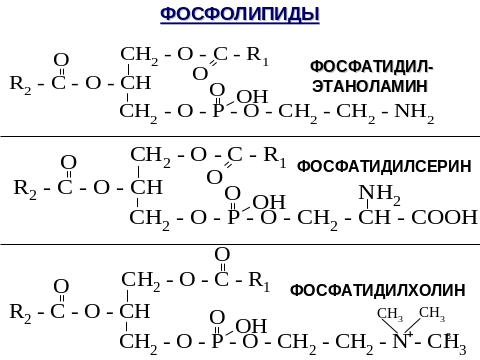
Биологическая роль.
Входят в состав в мембран, участвуя в их избирательной проницаемости.
Дипальмитоилфосфатидилхолин (до 80%), является компонентом сурфактанта, выстилающего альвеолы легких и препятствующей слипанию стенок альвеол во время вдоха (слайд).
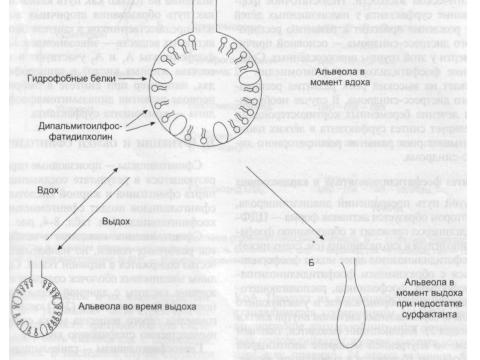
Фосфатидилэтаноламин и фосфатидилхолин мембран взаимодействует с ферментами, образуя комплексы, которые активируют факторы свертывания крови. Фосфатидилсерин активирует процессы фибринолиза, связываясь с другими ферментами.
Обладают липотропным действием, препятствуя отложению нейтрального жира в печени.
Продукты их распада участвуют в патогенезе бронхиальной астмы, атеросклероза.
Ф-серин влияет на освобождение гистамина.
Метаболизм любого класса веществ складывается из процесса распада и синтеза. Рассмотрим процесс распада фосфолипидов (слайд).
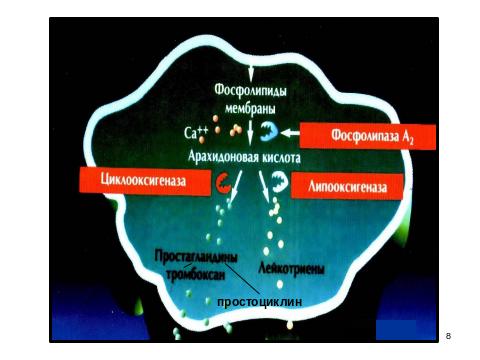
От фосфолипидов мембран под действием фосфолипазы А2, отщепляется арахидоновая кислота, которая используется для синтеза эйкозаноидов (напомнить о строении). Активация фосфолипаз происходит под действием различных факторов: гормонов, гистамина, цитокинов, в условиях гипоксии, иммунных воздействий и др.
В клетках имеется 2 основных пути превращения арахидоновой кислоты:
1 – циклооксигеназный, приводящий к синтезу простагландинов – предшественников тромбоксанов и простациклинов;
2 – липооксигеназный, заканчивающийся образованием лейкотриенов.
Простагландины
Влияют на сокращение гладких мышц.
Способствуют секреторной функции желудка.
Участвуют в воспалительных реакциях.
Модулируют действие гормонов.
Влияют на гемодинамику почек.
Автономно регулируют нервное возбуждение.
Простациклины – образуются в стенках кровеносных сосудов сердца, матки, слизистых желудка.
Расслабляют гладкую мускулатуру
Способствуют фибринолизу, и тем самым препятствует свертыванию крови.
Тромбоксаны являются антагонистами простациклинов, образуются в тромбоцитах, в мозге, способствуют свертыванию крови
вызывая агрегацию тромбоцитов
оказывают сосудосуживающее действие.
Накопление служит причиной тромбоза, атеросклероза
Лейкотриены в лейкоцитах, макрофагах.
Вызывают сокращение гладких мышц дыхательных путей
Стимулируют секрецию гликопротеинов, увеличивают количество слизи в дыхательных путях
Участвуют в аллергических и иммунологических реакциях.
Повышают проницаемость сосудов.
Затрудненное дыхание при бронхиальной астме связано с действием лейкотриенов. Ревматоидные артриты также обусловлены действием лейкотриенов.
Жировое перерождение (инфильтрация) печени.
Гепатоциты переполняются нейтральным жиром (ТАГ), разрушаются, образуются кисты, вокруг них разрастается соединительная ткань, развивается жировая дистрофия. Эта патология возникает вследствие нарушения синтеза фосфолипидов, связанный с недостатком липотропных фактров: метионина, полиеновых ненасыщенных жирных кислот, холина, В12, В15, фолиевой кислоты, липокаина (вырабатывается в ПЖЖ), поступающей только в составе пищи.
ФЛ входят в состав ЛПОНП, которые транспортируют эндогенные ТАГ из печени тканям. Следовательно, нарушение образования ЛПОНП приводит к нарушению их выведения и накопления в печени.
Метаболизм холестерола (слайд).
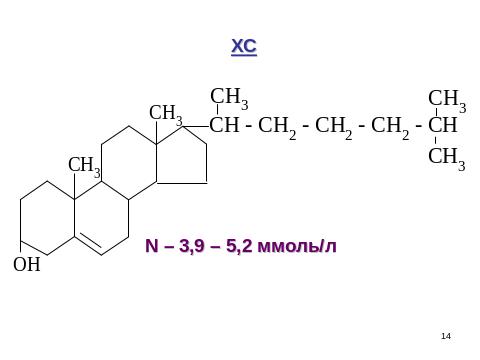
Холестерол – стероид, характерный только для животных организмов. 50% синтезируется в печени, 15-20% в тонком кишечнике, остальной – в коже, коре надпочечников, половых железах. В сутки синтезируется 1г холестерола. С пищей поступает 300-500мг.
N в крови = 3,9-5,2 ммоль/л
У новорожденных ХС – 1,3-2,6 ммоль/л
В 12-14 лет – достигает нормы.
Биологическая роль.
Входит в состав клеточных мембран, влияя на их свойства.
Субстрат для синтеза желчных кислот, стероидных гормонов, витамин Д3.
Поддерживает тургор кожи.
Реакция синтеза ХС происходит в цитолизе клеток, это один из самых длинных метаболических путей в организме человека, включает около 100 последовательных реакций.
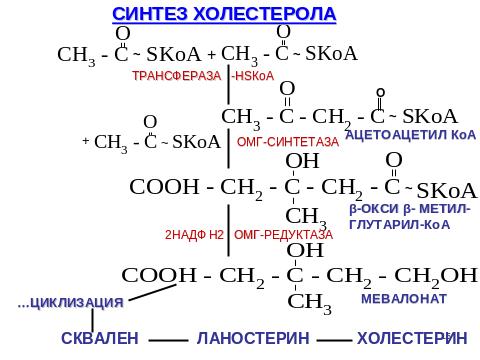
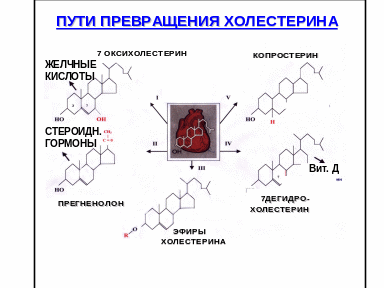
Основной путь превращения ХС – это его окисление. 80% от всего количества окисляется в печени в желчные кислоты, 3% в стероидные гормоны. При реакциях окисления в молекуле ХС появляются полярные группы, гидроксилы, карбоксилы, повышается его растворимость в воде, что способствует выведению из организма.
Второй путь превращения ХС в организме – это образование эфиров ХС (эстерификация). Эфиры ХС составляют около 10% от общего количества ХС в организме. При этом растворимость уменьшается и это приводит к накоплению в организме. У новорожденных относительно низкий коэффициент эстерификации по сравнению с более старшим возрастом детей = 0,58-1 ммоль/л, что связано с дефицитом полиненасыщенных жирных кислот.
Дегидрирование. В положении 7, 8 образуются двойные связи, что приводит к образованию 7-дегидрохолестерола (предшественника витамина Д3)
Выведение холестерола.
Чтобы поддерживать постоянный уровень его в организме необходимо выводить 1,5г в сутки. 1г в сутки окисляется в желчные кислоты, 200-300мг в сутки с калом в виде копростанола, 100мг со слущенным эпителием, 40 мг идет на синтез стероидных гормонов, с мочой 1-2мг в сутки.
Регуляция метаболизма холестерола.
Ключевую роль в регуляции метаболизма холестерина играют рецепторы ЛПНП. Впервые эти рецепторы были обнаружены на клетках кожи человека учеными Браун и Гольштейн в 1973г в Далласе (Техасском медицинском центре). За это открытие они получили нобелевскую премию по медицине в 1985г.
ЛПНП поставляют холестерин в различные клетки. Рецепторы, связывая белково-липидные комплексы ЛПНП не только обеспечивают клетки холестерином, но и снижают уровень ЛПНП в крови. Ясно, чем больше рецепторов ЛПН на поверхности клетки и чем эффективнее они взаимодействуют с ЛПН, тем быстрее холестерин удаляется из крови.
Происходит это в следующие этапы:
Рецепторы (по химической природе – гликопротеины) на плазматической мембране клеток узнают те ЛП, в состав которых входит апопротеин В-100 и связывается с ними.
Комплекс рецептор-ЛПНП проникает в клетку путем эндоцитоза, образуя пузырек-эндосому.
Эндосомы сливаются с лизосомами. Под действием ферментов лизосом белковая часть расщепляется до свободных аминокислот. Эфиры холестерина расщепляются кислой липазой до св. ХС.
Накапливающийся в клетках ХС оказывает тройное действие на метаболизм.
1. Тормозит синтез ХС самой клеткой, ингибируя по механизму обратной связи фермент ОмГ-редуктазу.
2. Индуцирует процесс образования эфиров ХС в цитоплазме клетки (активирует ЛХАТ) лецитинацетилхолестеролтрансфераза.
3. Избыток ХС по принципу обратной связи подавляет образование новых рецепторов ЛПНП. В результате количество рецепторов уменьшается и клетка начинает связывать меньше ЛПНП.
В регуляции синтеза рецепторов ЛПНП участвуют: инсулин, Т3, половые гормоны, которые увеличивают их количество, а глюкагон подавляет.
? эффекты инсулина и Т3 могут объяснить механизм гиперхолестеринемии, риск атеросклероза при сахарном диабете или при гипотиреозе.
Патология обмена ХС.
Гиперхолестеринемия – повышение уровня ХС в крови при норме 3,9-5,2 ммоль/л. Факторы риска:
Гиперкалорийное питание (избыточное поступление углеводов, жиров)
Гиподинамия
Курение
Сопутствующие заболевания (гипертоническая болезнь, сахарный диабет, гипотиреоз, ожирение)
Стресс (адреналин приведет к синтезу ацетилКоа → ХС).
Атеросклероз.
Заболевание, связанное с накоплением холестерола и его эфиров, в ЛПНП, в эндотелии сосудов (слайд).
Рассмотрим развитие атеросклеротической бляшки в клетках эндотелия кровеносных сосудов.

В области бляшки часто образуются тромбы, суживающие просвет сосуда, что приводит к острому нарушению кровообращения и развитию инфаркта миокарда, инсульта.

Желчнокаменная болезнь.
Патологический процесс, при котором в желчном пузыре образуются камни, основу которых составляет ХС. Выделения ХС в желчь должно сопровождаться пропорциональным выделением желчных кислот и ФЛ, удерживающих гидрофобные молекулы ХС в желчи в мицеллярном состоянии. Если эти пропорции нарушены, то ХС начинает осаждаться в желчном пузыре, образуя вязкий осадок, который постепенно становится твердым. Камни могут состоять не только из холестерола (белого цвета), но и из смеси ХС, билирубина, белков, кальция – смешанные (коричневого цвета).
Причины: гиперкалорийное питание, избыток ХС в пище, застой желчи, нарушение энтерогепатической циркуляции желчных кислот, а также их синтеза, инфекции желного пузыря.
