- •Введение
- •1. Физико-химические свойства аминокислот
- •1.1. Растворимость
- •1.2. Кислотно-основные свойства
- •1.3. Спектры поглощения аминокислот
- •1.4. Специфические реакции аминокислот
- •1.4.1. Образование комплексов с металлами
- •1.4.2. Реакции с азотистой кислотой
- •1.4.3. Окислительное дезаминирование
- •1.4.4. Переаминирование
- •1.4.7. Декарбоксилирование
- •1.4.8. Этерификация
- •2. Анализ аминокислот
- •2.1. Качественный анализ аминокислот
- •2.1.1. Цветные реакции на карбоновые аминокислоты
- •2.1.1.1. Нингидриновая реакция
- •2.1.1.6. Биуретовая реакция на пептидные связи
- •2.2. Количественный анализ
- •2.2.1. Идентификация аминокислот и определение их количества
- •Масс-спектрометрический анализ
- •Методы анализа с использованием изотопов
- •Ферментативные методы
- •Определение аминокислот формолтитрованием по Сьоренсону
- •2.2.2. Методы разделения Метод распределительной (радиальной) хроматографии на бумаге
- •Разделение смеси аминокислот методом распределительной хроматографии в тонком слое целлюлозы
- •Разделение аминокислот методом ионообменной колоночной хроматографии
- •Газовая хроматография
- •Литература
2.1. Качественный анализ аминокислот
2.1.1. Цветные реакции на карбоновые аминокислоты
2.1.1.1. Нингидриновая реакция
Принцип реакции. В результате взаимодействия α-аминокислоты с нингидрином (трикетогидриденгидратом) образуется окрашенное комплексное соединение.
При нагревании (до t 70 °С) α-аминокислоты окисляются нингидрином и подвергаются окислительному дезамиеированию с образованием аммиака и декарбоксилированию с образованием альдегида и СО2, а нингидрин восстанавливается

Восстановленный нингидрин, конденсируясь с аммиаком и окисленным нингидридом, образует соединение, которое, енолизируясь, переходит в окрашенную форму, имеющую сине-фиолетовый цвет.

В присутствии органических растворителей, на которых готовят раствор нингидрина (ацетон, этанол), возможно протекание побочной реакции с образованием соединения, содержащего в своем составе радикал (R) аминокислоты.
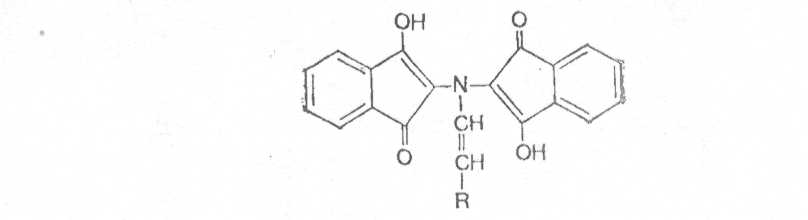
Наличие радикала аминокислоты в составе этого соединения обуславливает различную окраску (красную, желтую, голубую) соединений, возникающих при реакции аминокислот с нингидрином.
Реакция с нингидрином является специфической для аминокислот, содержащих α-аминогруппу, и характерна как для некоторых карбоновых, так и циклических аминокислот. В реакции глицина с нингидрином образуется комплексное соединение, имеющее сине-фиолетовую окраску [9, 10, 11].
2.1.1.2 Реакция с азотистой кислотой
Принцип реакции. В результате взаимодействия α-аминокислоты с азотистой кислотой, образуемой в реакции нитрита натрия с уксусной кислотой, происходит образование газообразного азота. Для глицина уравнение реакции имеет вид [10]:
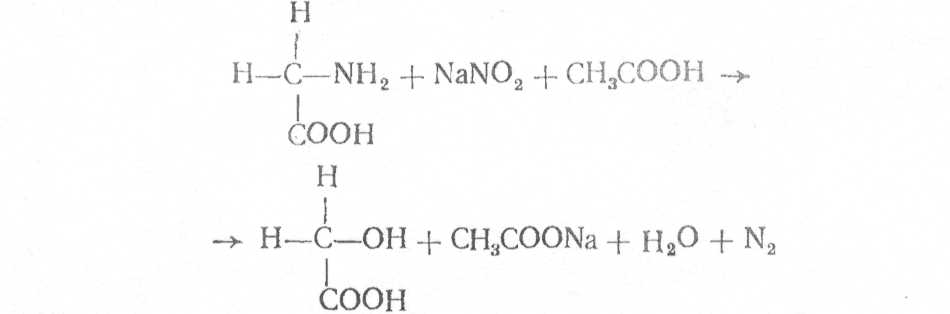
2.1.1.3. Образование комплексной соли меди
Принцип реакции. При нагревании аминокислоты с карбонатом меди (II) образуется комплексное соединение меди, имеющее синее окрашивание. В случае использования глицина уравнение реакции имеет вид [10]:
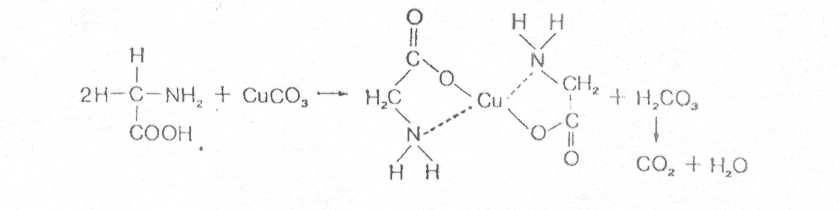
2.1.1.4. Реакция Сакагучи на аргинин
Принцип реакции. В реакции аргинина, содержащего гуанидиновую группировку, с гипобромитом происходит образование окисленной формы аргинина, которая при взаимодействии с α-нафтолом образует соединение красного цвета [9, 10, 11].

2.1.1.5. Реакция Фоля на «слабосвязанную» серу цистеина и цистина
Принцип реакции. При кипячении цистеина и цистина в щелочной среде от них легко отщепляется сера в виде сероводорода, который в щелочной среде образует сульфид натрия. Для цистеина уравнение реакции имеет вид [9, 10, 11]:
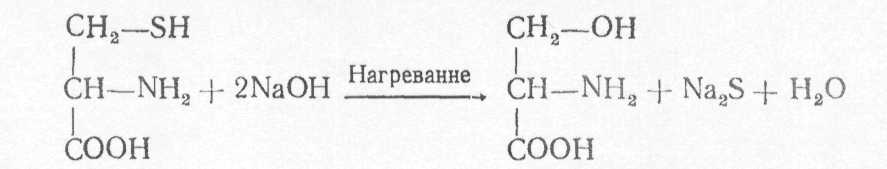
Образование сульфида натрия можно обнаружить с помощью ионов тяжелых металлов, например, ионов свинца, образующих с ионами серы нерастворимый сульфид свинца черного цвета. Для выявления сульфида серы можно использовать ацетат свинца, который при взаимодействии с гидроксидом натрия образует плюмбит натрия. В свою очередь плюмбит натрия, реагируя с сульфидом натрия, приводит к образованию сульфида свинца (бурый или черный осадок) [9 ,10].

2.1.1.6. Биуретовая реакция на пептидные связи
Принцип реакции. Аминокислоты, способные образовывать не менее двух пептидных связей (-CO-NH-), в щелочном растворе в присутствии сульфата меди (II) образуют комплексы с атомами меди, окрашенные в фиолетовый цвет.
Впервые реакция образования таких комплексных соединений меди была проведена для биурета, поэтому она и названа биуретовой.
Биурет, который может быть получен при нагревании мочевины до t 180 °С, не является аминокислотой, но имеет две пептидные связи
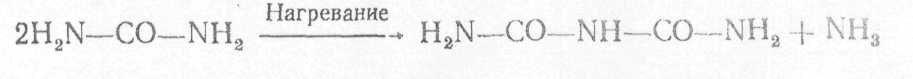
В щелочной среде биурет претерпевает енолизацию по схеме

Две молекулы енольной формы биурета взаимодействуют с гидроксидом меди (II) и образуют комплекс, в котором координационные связи образованы за счет электронных пар атомов азота иминных групп.
Гидроксид меди (II) для проведения биуретовой реакции получают, как правило, в результате реакции взаимодействия сульфата меди (II) с гидроксидом натрия (или калия):
![]()
Образование комплекса биурета с медью происходит по следующей схеме:
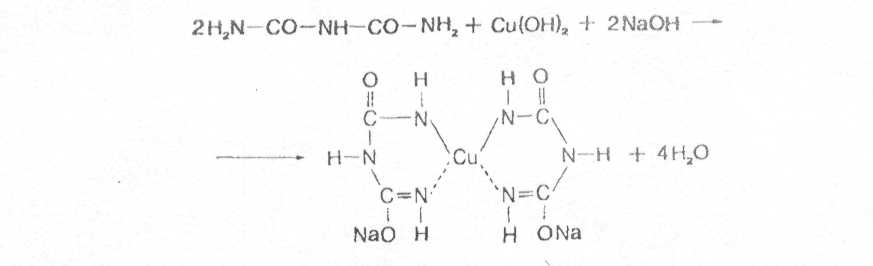
Подобный комплекс с медью могут создавать некоторые аминокислоты, у которых пептидные связи возникают за счет карбоксильной и аминогрупп. Примером такой аминокислоты может быть аспарагин [10, 11].
2.1.1.7. Цветная реакция на метионин (по Мак-Карти и Салливану)
Метионин в щелочном растворе реагирует с нитропруссида натрия с образованирем яркой красно-фиолетовой окраски [9].
2.1.1.8. Цветная реакция на глицин (реакция Циммермана)
Глицин в щелочном растворе реагирует с о-фталевым диальдегидом. Реакционная смесь немедленно окрашивается в ярко-зеленый цвет, затем выпадает зеленый осадок [9].
2.1.2. Цветные реакции на циклические аминокислоты
2.1.2.1. Ксантонротеиновая реакция
Принцип реакции. В ароматических аминокислотах, содержащих бензольные кольца (тирозин, триптофан, фенилаланин), под действием азотной кислоты происходит реакция нитрования бензольного кольца с образованием окрашенного в желтый цвет нитросоединения. Рассмотрим эту реакцию на примере тирозина [10, 11]:
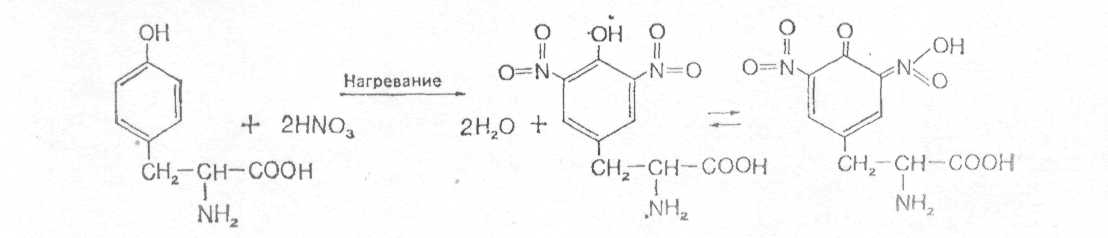
В реакции гидроксида натрия с хиноидной формой динитротирозина образуется натриевая соль динитротирозина, имеющая оранжевую окраску:
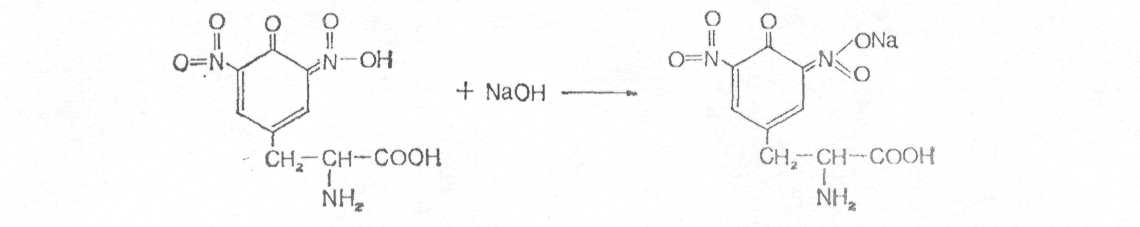
2.1.2.2. Реакция Милона на тирозин
Принцип реакции. В реакции ароматической аминокислоты тирозина, содержащей фенольное ядро с реактивом Милона (смесь нитратов и нитритов ртути (I) и (II), растворенных в концентрированной азотной кислоте) образуется ртутная соль тирозина, имеющая красную окраску [9, 10]:
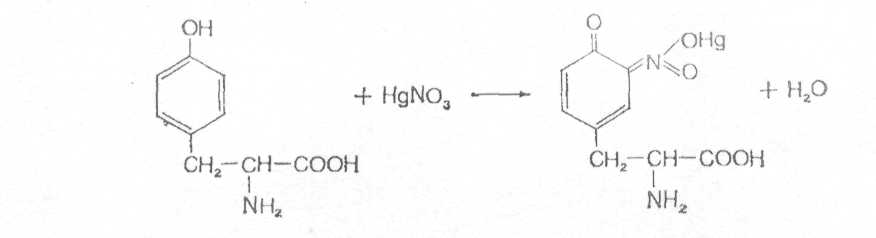
2.1.2.3. Реакция Адамкевича на триптофан
Принцип реакции. Триптофан в кислой среде вступает в реакцию с глиоксиловой кислотой (альдегидами), образуя при этом окрашенные в красно-фиолетовый цвет продукты конденсации [10, 11].
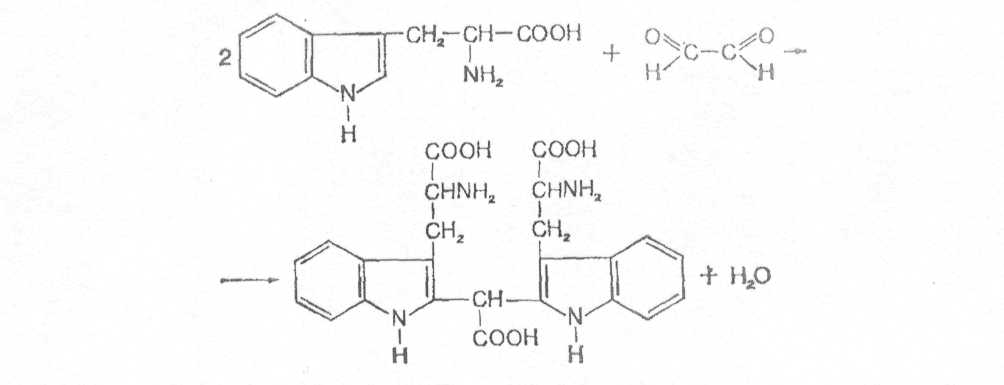
2.1.2.4. Реакция Вуазене на триптофан
Принцип метода. Триптофан, конденсируясь с формальдегидом, образует окрашенный продукт конденсации бис-2-триптофанилметан, который окисляется до бис-2-триптофанилкарбинола [10].
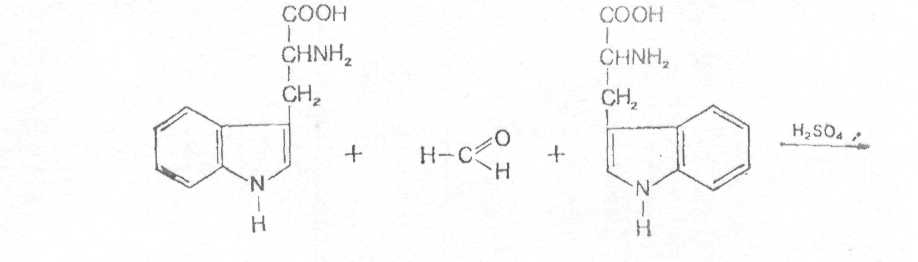
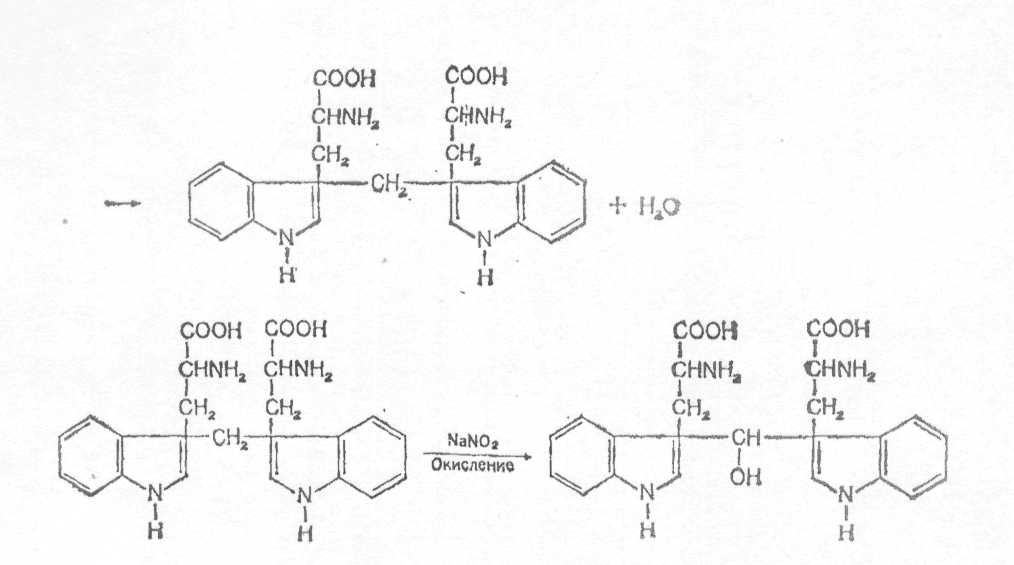
В присутствии минеральных кислот бис-2-триптофанилкарбинол образует соли, окрашенные в сине-фиолетовый цвет.
2.1.2.5. Реакция Паули на гистидин и тирозин
Принцип реакции. При взаимодействии сульфониловой кислоты в кислой среде с нитритом натрия (калия) происходит реакция диазотирования и образуется диазобензолсульфоновая кислота, которая в реакции с гистидином (или тирозином) образует комплексное соединение вишнево-красного цвета [9, 10, 11.
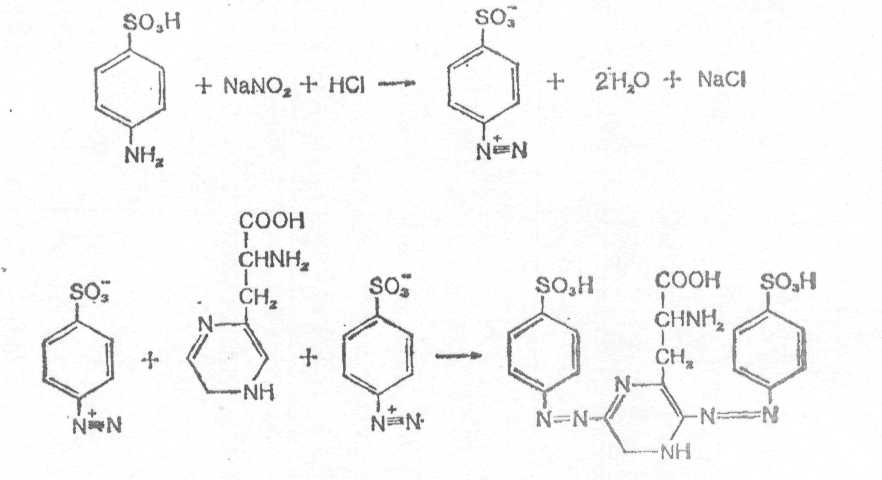
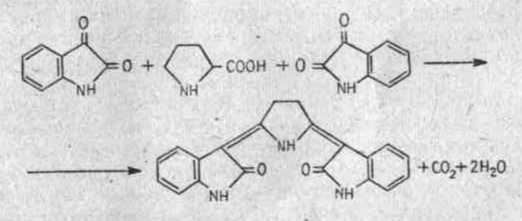
2.1.2.6. Цветные реакции на пролин.
Два наиболее распространенных реагента на присутствие аминокислот – нингидрин и изатин – взаимодействуют с аминокислотой пролином особым образом.
1) Цветная реакция пролина с нингидрином. Пролин реагирует с нингидрином при нагревании с образованием продукта конденсации пролина с нингидрином: ярко-желтой окраски [9]:

2) Цветная реакция пролина с изатином. Пролин в ледяной уксусной кислоте реагирует с изатином с образованием синего окрашивания [9].