
- •I.Теоретические вопросы требующие развернутого ответа
- •3.Основные типы кристаллических решеток металлов : оцк, гцк, гп.Их параметры.
- •5.Дефекты кристаллического строения реальных металлов : точечные , линейные , поверхностные и объемные.Их роль в формировании свойств металлов .
- •7.Кристаллизация металлов : несамопроизвольная кристаллизация , строение литого металла .Способы управления процессом кристаллизации.
- •8.Строение металлических сплавов .Понятия : сплав , термодинамическая система , компонент , фаза.
- •9.Твердые растворы замещения : определение , типы тр замещения , условия их образования , примеры.
- •10.Твердые растворы внедрения : условия образования , примеры.
- •11.Химические соединения : определение , условия образования , примеры.
- •12.Правило фаз Гиббса. Диаграмма состояния двухкомпонентных систем. Ликвидус и солидус.
- •15.Диаграмма фазового равновесия с нерастворимостью компонентов в твердом состоянии и эвтектикой. Типы образующихся структур.
- •Диаграмма состояния сплавов с отсутствием растворимости компонентов в компонентов в твердом состоянии (механические смеси)
- •16.Диаграмма состояния сплавов с ограниченной растворимостью компонентов в твердом состоянии и эвтектикой. Предельная растворимость , линия сольвус. Типы образующихся структур.
- •Диаграмма состояния сплавов с ограниченной растворимостью компонентов в твердом состоянии
- •17.Диаграмма состояния системы с образованием устойчивого химического соединения . Диаграмма состояния сплавов, компоненты которых образуют химические соединения.
- •18.Свойства железа , углерода , полиморфизм , критические точки .Взаимодействие железа с углеродом.
- •19.Фазы и структурные составляющие сплавов Fe-c (Fe3c) : определения , характеристики свойства.
- •20.Диаграмма фазового равновесия железо-углерод : реакции равновесия в системе. Диаграмма состояния железо—углерод (Fe—с)
- •24.Термическая обработка металлов и сплавов .Классификация видов термической обработки.
- •25.Способы отжига сталей : полный и неполный отжиг , нормализация.
- •26.Способы отжига сталей : гомогенизирующий , сфероидизирующий отжиг. Суть режимы.
- •28.Превращения , происходящие при нагреве сталей до аустенитного состояния. Понятие о китических точках сталей Ac1 , Ac3 , Acm , Ar1 , Ar3 ,Arm.
- •1. Превращение перлита в аустетит
- •29.Закалка сталей-полная и неполная . Понятие о критической скорости закалки .Закалка сталей на мартенсит.
- •30.Превращения происходящие при охлаждении сталей : промежуточное (бейнитное) превращение , особенности , структура. Бейнитное превращение Строение бейнита
- •Участок диаграммы состояния Fe — с
- •31.Превращения происходящие при отпуске закаленной стали. Низкий , средний и высокий отпуск : режимы, структура стали после отпуска.
- •32.Химико-термическая обработка . Общие закономерности хто.
- •Химико-термическая обработка стали
- •33.Цементация сталей : сущность , температурные режимы , структура после цементации.
- •35. Нитроцементация: сущность, температурные режимы, структура поверхности стали после нитроцементации.
- •36. Углеродистые стали. Влияние углерода и примесей на свойства стали.
- •38. Конструкционные углеродистые стали обыкновенного качества: классификация, маркировка, применение.
- •Стали конструкционные углеродистые обыкновенного качества
- •Стали группы а
- •Стали группы б
- •Стали группы в
- •Маркировка
- •Применение
- •39.Качественные конструкционные углеродистые стали : классификация , маркировка , применение.
- •40.Чугуны.Маркировка чугунов.
- •41. Классификация по назначению и маркировка легированных сталей. Примеры.
- •42.Легированные стали. Влияние легирующих элементов на структуру и свойства сталей. Карбиды в легированных сталях.
- •43.Легированные стали : подшипниковые стали : принцип легирования , маркировка , термообработка . Подшипниковые стали
- •44.Легированные стали : высокопрочные легированные стали : принципы легирования , термообработка.
- •45.Легированные стали : стали для строительных конструкций , принцип легирования , маркировка термообработка.
- •46.Легированные стали : улучшаемые стали , принцип легирования , маркировка , термообработка.
15.Диаграмма фазового равновесия с нерастворимостью компонентов в твердом состоянии и эвтектикой. Типы образующихся структур.
Диаграмма фазового равновесия с нерастворимость компонентов в твердом состоянии и эвтектикой. Типы образующихся структур.
Диаграмма состояния сплавов с отсутствием растворимости компонентов в компонентов в твердом состоянии (механические смеси)
Диаграмма состояния и кривые охлаждения типичных сплавов системы представлены на рис. 5.3.
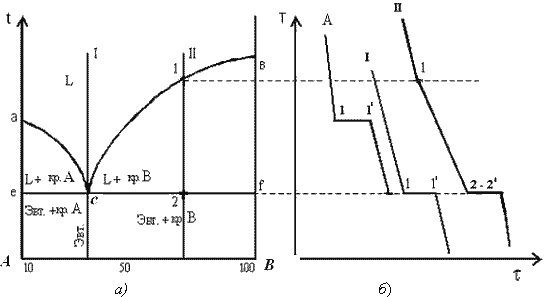
Рис. 5.3. Диаграмма состояния сплавов с отсутствием растворимости компонентов в твердом состоянии (а) и кривые охлаждения сплавов (б).
Проведем анализ диаграммы состояния.
1. Количество компонентов: К = 2 (компоненты А и В);
2. Число фаз: f = 3 (кристаллы компонента А, кристаллы компонента В, жидкая фаза).
3. Основные линии диаграммы:
линия ликвидус acb, состоит из двух ветвей, сходящихся в одной точке;
линия солидус ecf, параллельна оси концентраций стремится к осям компонентов, но не достигает их;
4.
Типовые сплавы системы.а) Чистые
компоненты, кристаллизуются при
постоянной температуре, на рис 5.3 б
показана кривая охлаждения компонента
А.б). Эвтектический
сплав –
сплав, соответствующий концентрации
компонентов в точке с (сплав I). Кривая
охлаждения этого сплава, аналогична
кривым охлаждения чистых металлов (рис.
5.3 б)Эвтектика
– мелкодисперсная механическая смесь
разнородных кристаллов, кристаллизующихся
одновременно при постоянной, самой
низкой для рассматриваемой системы,
температуре.При образовании сплавов
механических смесей эвтектика состоит
из кристаллов компонентов А и В: Эвт.
(кр. А + кр. В)Процесс
кристаллизации эвтектического сплава:
до точки 1 охлаждается сплав в жидком
состоянии. При температуре, соответствующей
точке 1, начинается одновременная
кристаллизация двух разнородных
компонентов. На кривой охлаждения
отмечается температурная остановка,
т.е. процесс идет при постоянной
температуре, так как согласно правилу
фаз в двухкомпонентной системе при
наличии трех фаз (жидкой и кристаллов
компонентов А и В) число степеней свободы
будет равно нулю
![]() .
В точке 1/
процесс кристаллизации завершается.
Ниже точки 1/
охлаждается сплав, состоящий из дисперсных
разнородных кристаллов компонентов А
и В.
.
В точке 1/
процесс кристаллизации завершается.
Ниже точки 1/
охлаждается сплав, состоящий из дисперсных
разнородных кристаллов компонентов А
и В.
16.Диаграмма состояния сплавов с ограниченной растворимостью компонентов в твердом состоянии и эвтектикой. Предельная растворимость , линия сольвус. Типы образующихся структур.
Диаграмма фазового равновесия ограниченной растворимостью компонентов в твердом состоянии и эвтектикой.
Диаграмма состояния сплавов с ограниченной растворимостью компонентов в твердом состоянии
Диаграмма
состояния и кривые охлаждения типичных
сплавов системы представлены на рис.5.5.
1. Количество компонентов: К = 2 (компоненты
А и В);2. Число фаз: f = 3 (жидкая фаза и
кристаллы твердых растворов
(раствор
компонента В в компоненте А) и
![]() (
раствор компонента А в компоненте В));
(
раствор компонента А в компоненте В));
3. Основные линии диаграммы:
линия ликвидус acb, состоит из двух ветвей, сходящихся в одной точке;
линия солидус аdcfb, состоит из трех участков;
dm – линия предельной концентрации компонента В в компоненте А;
fn – линия предельной концентрации компонента А в компоненте В.
4. Типовые сплавы системы. При концентрации компонентов, не превышающей предельных значений (на участках Аm и nВ), сплавы кристаллизуются аналогично сплавам твердым растворам с неограниченной растворимостью, см кривую охлаждения сплава I на рис. 5.5 б. При концентрации компонентов, превышающей предельные значения (на участке dcf), сплавы кристаллизуются аналогично сплавам механическим смесям, см. кривую охлаждения сплава II на рис. 5.5 б.
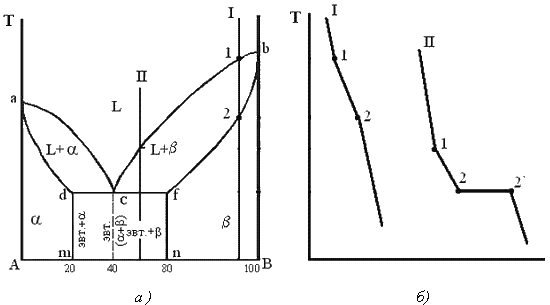
---------------------------Рис. 5.5 Диаграмма состояния сплавов с ограниченной растворимостью компонентов в твердом состоянии (а) и кривые охлаждения типичных сплавов (б).
Сплав с концентрацией компонентов, соответствующей точке с, является эвтектическим сплавом. Сплав состоит из мелкодисперсных кристаллов твердых растворов и , эвт. (кр. тв. р-ра + кр. тв. р-ра )
Кристаллы компонентов в чистом виде ни в одном из сплавов не присутствуют.
Сольвус -в диаграмме состояния, положение точек, представляющих температуру, при которой твердые фазы с переменным химическим составом сосуществуют с другими твердыми фазами, то есть показывающие пределы растворимости в твердом состоянии.
