
- •Номенклатура ферментов
- •Номенклатура окидоредуктаз
- •Номенклатура трансфераз
- •Номенклатура гидролаз
- •1). Гидролиз ацетилхолина:
- •Номенклатура лиаз (синтаз)
- •Номенклатура изомераз
- •1 ). Эпимеризация рибулозо-5-фосфата:
- •Номенклатура лигаз (синтетаз)
- •1). Карбоксилирование пирувата:
- •Написание уравнений ферментативных реакций исходя из названия фермента.
Лекция № 3
Классификация реакций, катализируемых ферментами.
Принципы классификации ферментов. Номенклатура ферментов: систематическая и тривиальная. Примеры важнейших ферментативных реакций, иллюстрирующие правила построения названий ферментов. Написание уравнений ферментативных реакций исходя из названия фермента.
Принципы классификации ферментов.
Особенностью классификации ферментов является то что, названия ферментам присваиваются не как обычно они даются органическим веществам по их формулам. При построении их названий их строение в настоящее время не учитывается, просто, потому, что это невозможно. Действительно, ферменты выделенные из разных организмов и катализирующие один и тот же процесс с одним и тем же субстратом могут различаться по своим физическим свойствам. Например амилаза Оптимум РН для действия фермента
поджелудочной железы 6,7-7,2
солода 4,4-4,5
слюны 6,5-6,8
Кроме того ситуация осложняется тем, что для ферментов, являющихся сложными белками (см. часть I, стр. 67, 68), характерно существование изоферментов. Изоферменты – это ферменты, катализирующие одну и ту же реакцию, но отличающиеся друг от друга по строению и физико-химическим свойствам.
Специфическим признаком, отличающим один фермент от другого, является лишь катализируемая ферментами химическая реакция. Этот классификационный признак и положен в основу систематической классификации ферментов, которая утверждена Комиссией по ферментам Международного биохимического союза (IUBМВ) в 1961 году. Вместе с этим продолжают применяться и тривиальные (рабочие) названия, которые, как правило, короче и поэтому более употребительны.
Систематическая классификация учитывает реакционную и субстратную специфичность ферментов. Все ферменты включены в «Каталог ферментов» под своим классификационным номером (КФ), состоящим из четырех цифр. Первая цифра КФ указывает на принадлежность фермента к одному из шести главных классов, в зависимости от типа реакции. Внутри каждого класса ферменты подразделяются на подклассы в зависимости от типа субстрата (вторая цифра КФ), а подклассы в свою очередь подразделяются на подподклассы в зависимости от типа кофермента, реагента или особенностей реакции (третья цифра КФ). Четвертая цифра указывает порядковый номер фермента в пределах данного подподкласса.
Итак, все ферменты разделяют на следующие 6 классов в зависимости от типа реакции:
Оксидоредуктазы, катализирующие окислительно-восстанови-тельные реакции.
Трансферазы, катализирующие реакции межмолекулярного переноса различных химических групп и остатков.
Гидролазы, катализирующие реакции гидролиза внутри-молекулярных связей.
Лиазы (синтазы), катализирующие расщепление или образование связи без участия окисления или гидролиза
Изомеразы, катализирующие реакции изомеризации.
Лигазы (синтетазы), катализирующие реакции присоединения, сопряженные с разрывом макроэргической связи в АТФ или ГТФ, ЦТФ, УТФ, ТТФ.
Внутри каждого класса ферменты разделяются на подклассы в зависимости от типа субстрата, с которым они взаимодействуют. Например, оксидоредуктазы (класс 1) подразделяют на подклассы в зависимости от типа субстрата, например, действующие на:
1.1. CH-OH группу доноров;
1.2. альдегидную или кетонную группу доноров;
1.3. CH-СH группу доноров;
1.4. CH-NH2 группу доноров; и др. подробнее см в пособии «Номенклатура ферментов»
Трансферазы (класс 2) разделяют на подклассы в зависимости от природы переносимой группы на переносящие:
2.1. одноуглеродные фрагменты;
2.2. альдегидные и кетоостатки;
2.3. ацильные группы; и др.
Гидролазы (класс 3) делятся на подклассы по типу гидролизуемой связи на катализирующие гидролиз:
3.1. сложных эфиров;
3.2. О-гликозидов;
3.3. простых эфиров;
3.4. пептидов; и др.
Лиазы (класс 4) делят на подклассы в зависимости от природы разрываемой связи на:
4.1. углерод-углерод лиазы;
4.2. углерод-кислород лиазы;
4.3. углерод-азот лиазы; и др.
Изомеразы (синтазы) (класс 5) делятся по типу изомеризации на:
5.1. рацемазы и эпимеразы;
5.2. цис-транс изомеразы; и др.
Лигазы (синтетазы) (класс 6) в зависимости от типа образующейся связи делятся на катализирующие образование связи:
6.1. углерод-кислород;
6.2. углерод-сера;
6.3. углерод-азот; и др.
Подклассы в свою очередь разделяют на подподклассы, детализирующие природу катализируемой реакции.
Номенклатура ферментов
Правила, которыми руководствуются при установлении систематического названия фермента и его четырехзначного кода можно уяснить при рассмотрении конкретных примеров ферментативных реакций.
Большинство официальных тривиальных названий, принятых в 1992 году IUBМВ, дает некоторую информацию о природе субстратов и характере катализируемых реакций. Такие названия ферментов обычно имеют окончание -«аза». Наряду с этим официально утверждены исторически сложившиеся названия, главным образом, для гидролаз, которые не подчиняются правилам построения ни систематических, ни тривиальных названий, например: ренин, трипсин, папаин и др.
Рассмотрим ряд примеров построения названий ферментов разных классов..
Номенклатура окидоредуктаз
Структура систематического названия оксидоредуктаз такова: название субстрата – донора электронов (восстановителя): название акцептора электронов (окислителя) – название класса (оксидоредуктаза.). Таким образом, приступая к построению названия фермента необходимо:
установить субстрат;
установить акцептор электронов.
Поскольку многие окислительно-восстановительные реакции обратимы, а прямую и обратную реакцию катализирует один и тот же фермент, то условлено, что в качестве субстрата для построения названия фермента выбирается метаболит, являющийся донором электронов, т.е. субстрат, подвергающийся окислению.
Тривиальные названия оксидоредуктаз имеют следующую структуру: приставка - название субстрата, корень – название группы оксидоредуктаз. Наиболее распространенные группы оксидоредуктаз следующие:
1. Дегидрогеназы – оксидоредуктазы, катализирующие дегидрирование субстрата с использованием в качестве акцептора водорода любых молекул кроме кислорода.
2. Если перенос водорода от молекулы донора трудно доказуем, то такие оксидоредектазы называют редуктазами.
3. Оксидазы – оксидоредуктазы, катализирующие окисление субстратов с молекулярным кислородом в качестве акцептора электронов без включения кислорода в молекулу субстрата.
4. Монооксигеназы – оксидоредуктазы, катализирующие внедрение одного атома кислорода в молекулу субстрата с молекулярным кислородом в качестве донора кислорода.
5. Диоксигеназы – оксидоредуктазы, катализирующие внедрение 2 атомов кислорода в молекулу субстрата с молекулярным кислородом в качестве донора кислорода.
6. Пероксидазы – оксидоредуктазы, катализирующие реакции с пероксидом водорода в качестве акцептора электронов.
Рассмотрим ряд примеров.
1). Восстановление пирувата до лактата:
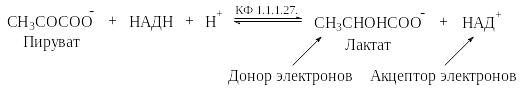
В рассматриваемом примере донор электронов - лактат. Акцептором электронов, т.е. окислителем выступает НАД+.

Систематическое название фермента КФ 1.1.1.27. – лактат:НАД+-оксидоредуктаза, тривиальное – лактатдегидрогеназа.
2). Окислительное декарбоксилирование пирувата:
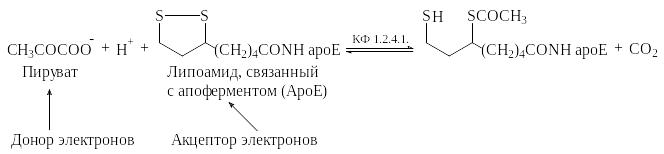
Фермент, катализирующий окислительное декарбоксилирование пирувата, имеет код КФ 1.2.4.1.

Систематическое название этого фермента – пируват:липоамид-оксидоредуктаза, тривиальное – пируватдегидрогеназа.
3). Окисление α-аминокислот кислородом без включения в их молекулы атомов кислорода из молекулы кислорода, например:
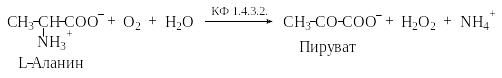
Кислород в молекуле пирувата появляется из молекулы воды после быстрого неферментативного гидролиза первоначально образующейся 2-имино-пропионовой кислоты.
Систематическое название этого фермента – L-аланин:кислород-оксидоредуктаза, тривиальное – L-аланиноксидаза.
4). Окисление цистеина кислородом с включением в молекулу цистеина обоих атомов кислорода:

Систематическое название фермента КФ 1.13.11.20.– цистеин:кислород-оксидоредуктаза, тривиальное – цистеиндиоксигеназа.
