
- •.Рух і його форми. Енергія та її види. Предмет термодинаміки. Робочі тіла. Поняття про ідеальні та реальні гази. Мета введення поняття про ідеальний газ
- •Ентальпія. Потенційна енергія тиску. Їх фізичний зміст.
- •Теплота і робота. Їх фізичний зміст та обчислення. Робота розширення та стиснення. Позитивний і негативний напрямок теплоти і роботи. Термодинамічна система та її типи.
- •Перший закон термодинаміки, його зміст, основні формулювання. Принципи еквівалентності енергії. Математичний вираз першого закону термодинаміки в різних формах
- •Вільна і зв’язана енергія робочого тіла. Поняття про енергію. Енергія Гельмгольца і енергія Гіббса. Їх фізичний зміст і математичні залежності. Енергетична модель робочого тіла.
- •Термодинамічний стан. Параметри стану. Термодинамічний метод. Екстенсивні та інтенсивні параметри стану. Питомі та мольні термодинамічні величини. Рівноважні та нерівноважні стани.
- •Чотири загальні властивості параметрів стану.
- •Термодинамічні потенціали. Чотири потенціали Гіббса. Диференційні рівняння термодинамічних потенціалів.
- •Теплоємність системи (робочого тіла). Питома теплоємність, фізичний зміст, одиниці виміру, залежність між питомими теплоємностями. Залежність теплоємності газу від температури.
- •Середня та дійсна теплоємність. Визначення середньої теплоємності газу при криволінійній та прямолінійній залежності її від температури
- •Середня уявна молекулярна маса, газова постійна. Густина та питомий об’єм суміші ідеальних газів, парціальних тиск компонентів сумішей ідеальних газів, співвідношення для їх знаходження.
- •Властивості реальних газів. Рівняння Ван Дер Ваальса для 1 кг газу. Внутрішній молекулярний тиск газу. Зміст константи в рівнянні Ван Дер Ваальса.
- •Термодинамічний процес. Рівноважний та нерівноважний процес. Графічний метод дослідження процесу. Прямий і зворотній процеси.
- •Оборотний та необоротний процеси. Умови проходження оборотних процесів. Облік незворотності в дійсних процесах.
- •Визначення значень зміни внутрішньої енергії, ентальпії та ентропії робочого тіла при зміні його стану.
- •Графічний метод вивчення термодинамічних процесів. Pv та ts –діаграми та їх властивості.
- •Ентропія робочого тіла. Фізичний зміст. Розмірність. Математичний вираз.
- •Характеристики термодинамічного процесу. Теплота і робота. Властивості їх диференціалів. Графічне зображення для розімкнутих та кругових процесів.
- •Характеристики термодинамічного процесу. Коефіцієнт перетворення енергії в процесаі (кпе). Коефіцієнт використання термодинамічного потенціалу в процесі (квп).
- •Ізохорний процес в ідеальних газах
- •Ізобарний процес в ідеальних газах
- •Політропний процес в ідеальних газах. Залежність для зміни параметрів стану робочого тіла
- •Обчислення роботи. Значення політропи для основних термодинамічних процесів. Визначення показника ступеня політропи.
- •Другий закон термодинаміки, його зміст та основні формулювання. Умови перетворення теплоти в роботу в безперервно діючому тепловому двигуні.
- •Кругові процеси чи цикли. Цикли прямі та зворотні, оборотні та необоротні. Термічний ккд циклу.
- •Прямий оборотний цикл Карно. Зображення циклу на pv та ts –діаграмах: вивести вираз для термічного ккд циклу. Аналіз циклу на основі виразу термічного ккд.
- •Зворотний оборотний цикл Карно. Холодильний коефіцієнт.
- •Теорема Карно.
- •Узагальнений (регенеративний цикл) Карно та його ккд. Необоротний цикл Карно та його ккд.
- •Властивості оборотного циклу. Перший та другий інтеграл Клаузіуса.
- •Зміна ентропії ізольованої кінцевої системи при оборотних на необоротних процесах. Математичний вираз другого закону термодинаміки. Принцип зростання ентропії.
- •Ексергія теплоти та фізичний зміст ентропії. Рівняння Гюі-Стодоли. Визначення зміни ексергії в основних термодинамічних процесах. Ексергетичний ккд.
- •Водяна пара як реальний газ.
- •Ентропія води, вологої та сухої, насиченої та перегрітої пари. Їх знаходження.
- •Знаходження питомого об’єму та густини вологої насиченої пари. Знаходження ентальпії та внутрішньої енергії вологої насиченої перегрітої пари.
- •Hs діаграма водяної пари, її побудова та застосування. Визначення параметрів стану вологої насиченої, сухої насиченої та перегрітої пари на hs діаграмі.
- •Ізобарний процес зміни стану водяної пари. Зображення процесу на pv, hs та ts діаграмах. Визначення роботи зміни внутрішньої енергії та параметрів стану пари.
- •Адіабатний процес зміни стану водяної пари. Зображення процесу на pv, hs та ts діаграмах. Визначення роботи зміни об’єму та параметрів стану.
- •Рівняння першого закону термодинаміки для потоку, фізичний зміст кожного члена рівняння, різні форми рівняння.
- •Швидкість витоку ідеального газу при адіабатному процесі. Рівняння для його визначення та аналізу. Швидкість витоку водяної пари та її визначення.
- •Секундна витрата ідеального газу при витоку. Рівняння для визначення та його аналіз. Гіпотеза Сен-Венана. Критичне відношення тисків при витоку ідеальних газів, рівняння для його визначення.
- •Вибір профілю сопла в залежності від критичного відношення тисків. Виток газу через комбіноване сопло. Розрахунок комбінованого сопла.
- •Витоки водяної пари та його особливості. Визначення швидкості водяної пари при різних умовах. Виток газів та пари при наявності тертя.
- •Дослідження дроселювання водяної пари різних станів по hs діаграмі.
- •Термодинамічні основи роботи поршневого компресора. Зображення роботи одноступінчатого компресора на pv діаграмі при ізотермічному, адіабатному та політропному стиску газу.
- •Робочий процес багатоступінчастого поршневого компресора. Зображення теоретичного робочого процесу триступінчастого компресора на pv та ts –діаграмах.
- •Що призвело до появи двигунів внутрішнього згорання(двз). На які групи діляться поршневі двз та яке паливо в них використовується? Індикаторна діаграма двз. Термодинамічний метод вивчення двз.
- •Причини виникнення двз зі змішаним згоранням палива. Теоретичний цикл цих двигунів. Зображення циклу в pv та ts –діаграмах, характеристики циклу, термічний ккд циклу, аналіз ккд циклу.
- •Принципова схема паросилової установки, що працює по циклу Ренкіна. Зображення циклу в pv та ts –діаграмах.
- •Вплив початкових та кінцевих параметрів пари на ккд циклу паросилової установки. Дати аналіз з використанням hs –діаграми. Відносний внутрішній ккд циклу.
- •Принципова схема паросилової установки, що працює по теплофікаційному циклу. Зображення циклу в pv та ts –діаграмах. Коефіцієнт використання теплоти циклі, порівняння з конденсаційним циклом.
- •Цикл газотурбінної установки(гту). Переваги гту перед двз. Термічний ккд гту.
- •Вологе повітря. Визначення. Абсолютна та відносна вологість, вологоємність. Точка роси. Hd –діаграма вологого повітря. Основні процеси вологого повітря в hd –діаграмі.
- •Відмінність паротурбінної установки від двз. Цикл Карно для насиченої пари.
- •Цикл паротурбінної установки з проміжним перегрівом пари. Економічність проміжного перегріву пари. Термічний ккд циклу, факти, які впливають на його величину.
- •Регенеративний цикл паросилової установки. Ціль використання. Ефективність застосування циклу. Питома витрата пари для регенеративного циклу.
- •Цикл теплового насосу. Доцільність використання теплового насосу. Опалювальний коефіцієнт. Його визначення. Переваги використання теплового насосу.
- •Цикл теплового насосу. Призначення та область застосування теплових насосів. Опалювальний коефіцієнт та його визначення
Зміна ентропії ізольованої кінцевої системи при оборотних на необоротних процесах. Математичний вираз другого закону термодинаміки. Принцип зростання ентропії.
Другий закон вивчає напрямок та глибину протікання термодинамічних процесів. Важлива задача полягає також у дослідженні необоротності протікання термодинамічних процесів. Розглянемо ізольовану термодинамічну систему.
, , , ; .
Так як це ізольована система, то немає теплообміну з навколишнім середовищем. Таким чином:
. (1)
Розглянемо ізольовану термодинамічну систему, коли в ній протікає необоротний процес – під час наявності тертя, на подолання якого необхідні витрати енергії. Система ізольована, тому ззовні енергія не поступає.
Кількість енергії ізольованої системи не змінюється. dH=0
Тоді ми беремо термодинамічну тотожність, що дає: TdS=dH-Vdp; dH=0; .
Тертя в необоротному процесі долається за рахунок наявної роботи, і в цьому випадку:
TdS>0 T>0 dS>0 (2)
Об’єднаємо перший і другий вирази:
dS≥0 (3)
Вираз (3) зображує принцип зростання ентропії і є математичним виразом другого закону термодинаміки: Ентропія ізольованої системи залишається незмінною, якщо в цій системі протікають оборотні процеси, і зростає, якщо в цій системі протікають необоротні процеси, але ніколи не може зменшуватись.
Цей закон дає можливість визначити напрямок і глибину протікання термодинамічного процесу. Довільні термодинамічні процеси протікають в напрямку збільшення ентропії і збільшуються під час досягнення ентропією максимального значення.
Ексергія теплоти та фізичний зміст ентропії. Рівняння Гюі-Стодоли. Визначення зміни ексергії в основних термодинамічних процесах. Ексергетичний ккд.
Ексергією називається максимальна робота, яку виконує робоче тіло під час переходу з початкового стану до кінцевого, який являє собою стан рівноваги з навколишнім середовищем. Робота виконується за рахунок енергії робочого тіла. Внутрішня енергія робочого тіла складається з вільної і зв’язаної енергій. Робота виконується робочим тілом у два етапи. У першому вільна енергія під впливом теплоти переходить у зв’язану енергію, що супроводжується виконанням роботи. Робота виконується за рахунок зміни якості енергії робочого тіла. У другому етапі робоче тіло виконує роботу за рахунок зменшення кількості внутрішньої енергії піл впливом різниці температур.
Якщо перетворення протікає у двох процесах – ізотермічному і адіабатному:

 У
ізотермічному процесі термодинамічним
потенціалом є вільна енергія
.
У
ізотермічному процесі термодинамічним
потенціалом є вільна енергія
.
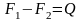 ;
; 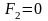 ;
;
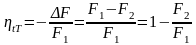
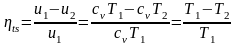 ;
;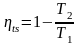
Якщо
 ,
то (6) буде виражати ексергетичну ККД:
,
то (6) буде виражати ексергетичну ККД: 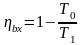
Отримаємо
з (8):
 (9)
(9)
Закон Гюй-Стодоли
Для
необоротніх процесів під час наявності
тертя буде втрачатись частина енергії
на подолання тертя. При цьому буде
збільшуватись ентропія системи на
величину, яка називається ентропією
дисипації
 .
Дисипативними
силами називаються
сили, які направлені у протилежний бік
руху тіла, і на подолання яких витрачається
робота.
.
Дисипативними
силами називаються
сили, які направлені у протилежний бік
руху тіла, і на подолання яких витрачається
робота.
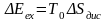 ;
;
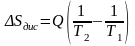 .
.
Закон Гюй-Стодоли виражає втрати ексергії в результаті необоротності проходження в ній необоротних процесів дорівнює добутку температури навколишнього середовища на суму збільшення ентропії всіх тіл, які беруть участь у дисипативних процесах. Метод оцінки ефективності термодинамічних систем, який будується на використанні поняття ексергії, називається ексергетичним методом термодинамічного аналізу системи.
