
- •1. Системы отсчёта. Путь, перемещение, траектория материальной точки.
- •2. Основные кинематические характеристики движения материальной точки.
- •3. Законы равномерного и равнопеременного поступательных движений.
- •4. Движение материальной точки по окружности. Угловая скорость, угловое ускорение. Законы вращательного движения твёрдого тела.
- •5. Первый закон Ньютона. Взаимодействие тел, инерция, инерциальные и неинерциальные системы отсчёта. Масса, сила.
- •2Закон Ньютона. Импульс, общая форма второго закона динамики.
- •7. Механическая система. Импульс механической системы. Закон сохранения импульса.
- •8. Энергия, работа, мощность. Кинетическая и потенциальная энергия.
- •9. Применение закона сохранения в механике на примере удара абсолютно упругих тел.
- •10. Применение закона сохранения в механике на примере удара не упругих тел.
- •11.Вращательное движение абсолютно твердого тела. Момент инерции. Вычисление моментов инерции сплошного цилиндра, полого цилиндра, шара, стержня.
- •12. Теорема Штейнера-Гюйгенса. Кинетическая энергия вращения.
- •13. Момент силы. Уравнение динамики вращательного движения твердого тела.
- •14. Момент импульса. Уравнение момента. Закон сохранения момента импульса.
- •15. Предмет и задачи молекулярной физики.
- •16. Основные положения молекулярно-кинетической теории газов. Модель идеального газа.
- •20.Распределение Больцмана.
- •21. Опытное обоснование мкт (опыт Штейна, броуновское движение, опытное определение постоянной Авогадро).
- •22. Внутренняя энергия. Закон Больцмана о равномерном распределении энергии по степеням свободы молекул.
- •23. Работа и теплота. Пнт.
- •24. Теплоёмкости. Классическая теория теплоёмкостей. Закон Джоуля.
- •25. Применение пнт к изопроцессам.
- •26.Адиабатный процесс. Уравнение Пуассона. Работа при адиабатном процессе.
- •27.Процессы: равновесные и неравновесные, обратимые и необратимые
- •28 Энтропия. Свойства энтропии, изменение энтропии при изопроцессах.
- •29.Свойства энтропии
- •30. Среднее число столкновений, средняя длина свободного пробега.
- •31. Диффузия в газах.
- •3 S 2. Вязкость газов
- •33.Теплопроводность в газах.
- •42.Соотношение между коэффициентами , и д.
- •35. Закон сохранения заряда. Закон Кулона.
- •36.Определение потока, индукции. Теорема Гаусса.
- •37. Применение теоремы Гаусса для расчета напряженности электрического поля.
- •38.Циркуляция вектора напряжённости электростатического поля
- •40.Напряжённость как градиент потенциала. Эквипотенциальные поверхности
- •41.Потенциал в простейших электрических полях. Потенциал поля Диполя.
- •42.Электроёмкость удельного проводника.
- •43.Энергия уединенного заряженного проводника.
- •49.Работа электрического тока.
20.Распределение Больцмана.
Пусть мы находимся на уровне моря(нулевой уровень). -давление на этой поверхности.
П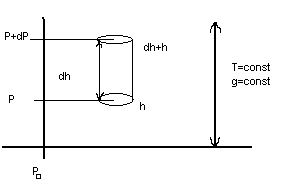 ри
ри
![]() :
:![]() .
Предположим, что площадь основания
цилиндра ровна 1.
для
.
Предположим, что площадь основания
цилиндра ровна 1.
для
![]() .
.
![]() ,
т.к.
,
т.к.
![]() .
Если
.
Если
![]() ,
то
,
то
![]() ,
,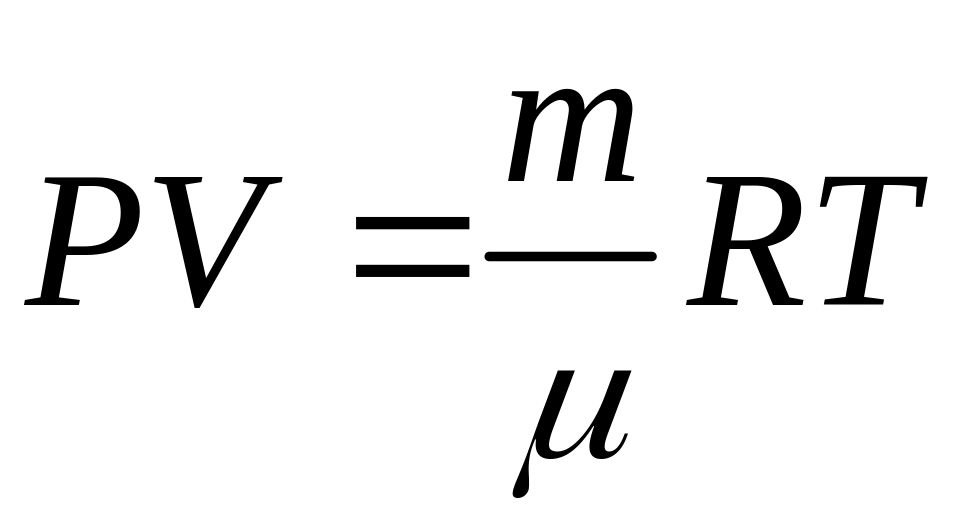 ,
,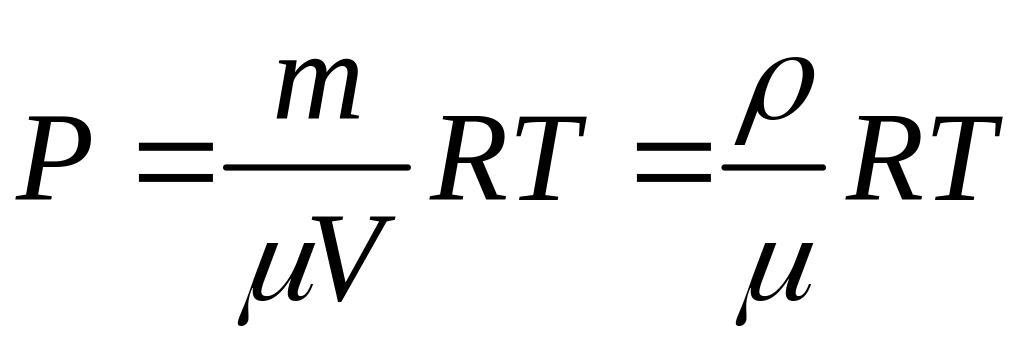 ,
,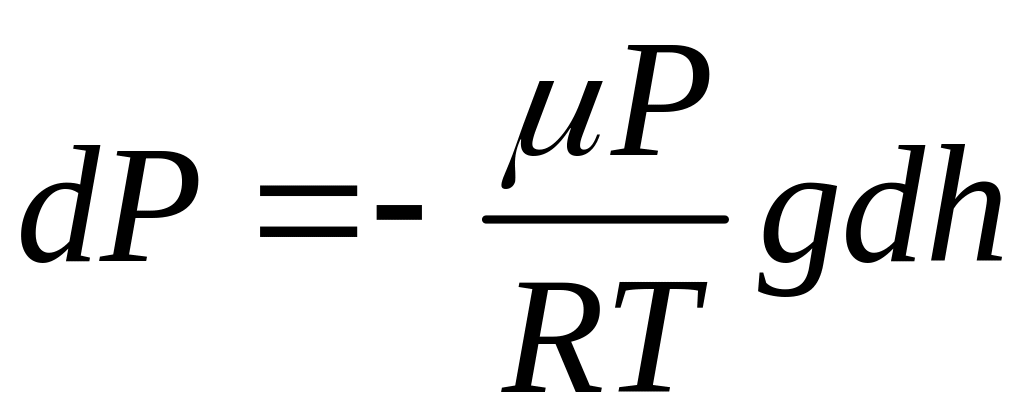 ,
,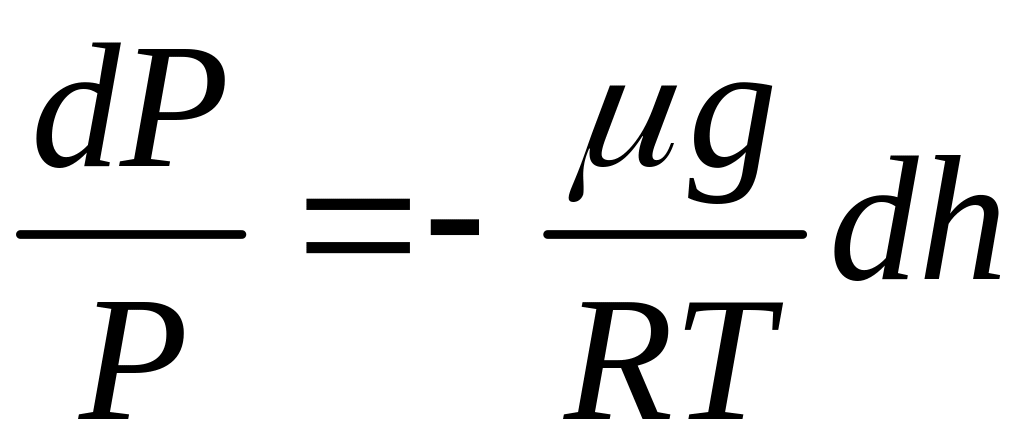 ,
,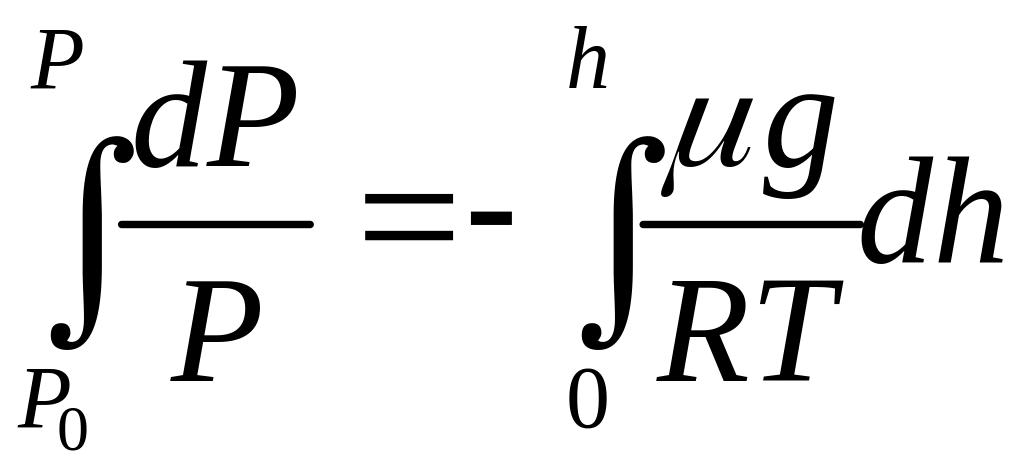 ,
,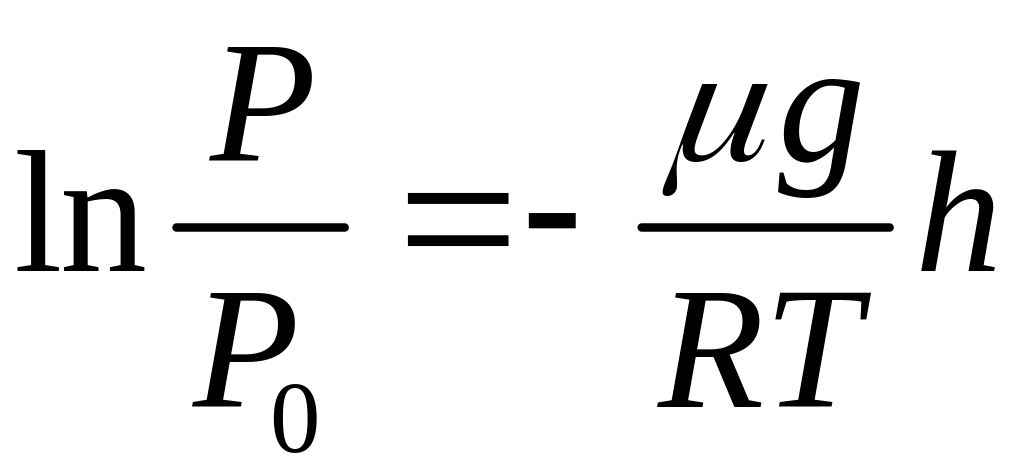 ,
,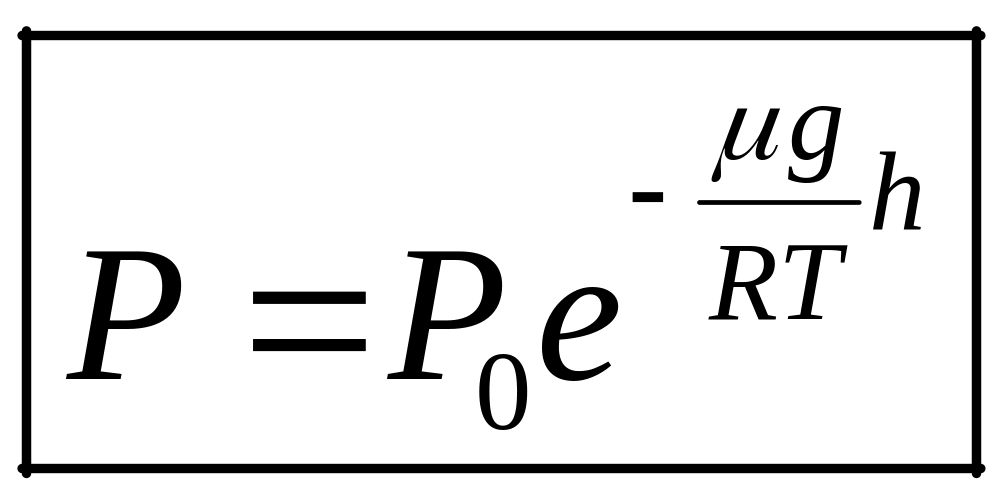 -параметрическая
формула,
-параметрическая
формула,
![]() ,
,![]() ,
,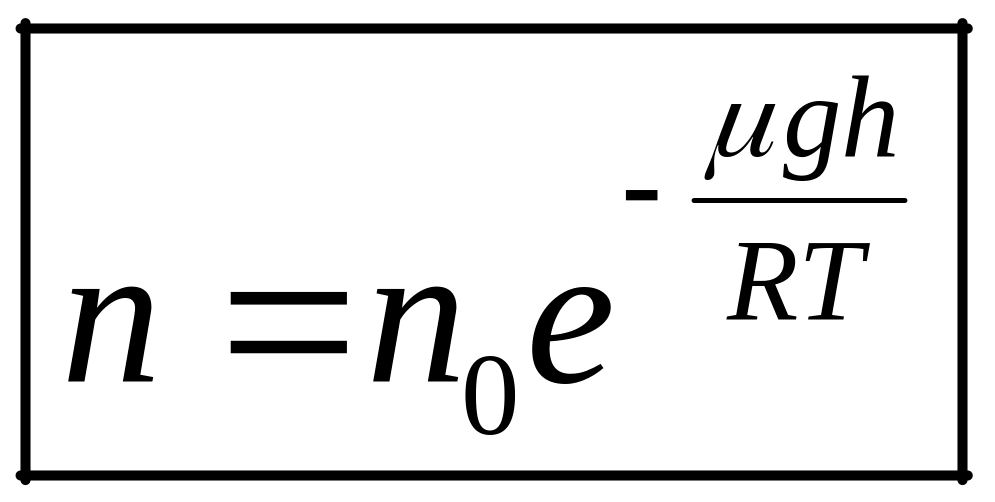 -распределение
Больцмана.
-распределение
Больцмана.
П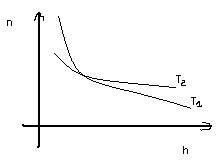 ри
ри
![]() ,
,![]() (Т-повышается)
(Т-повышается)
![]() .
.
![]() ,
,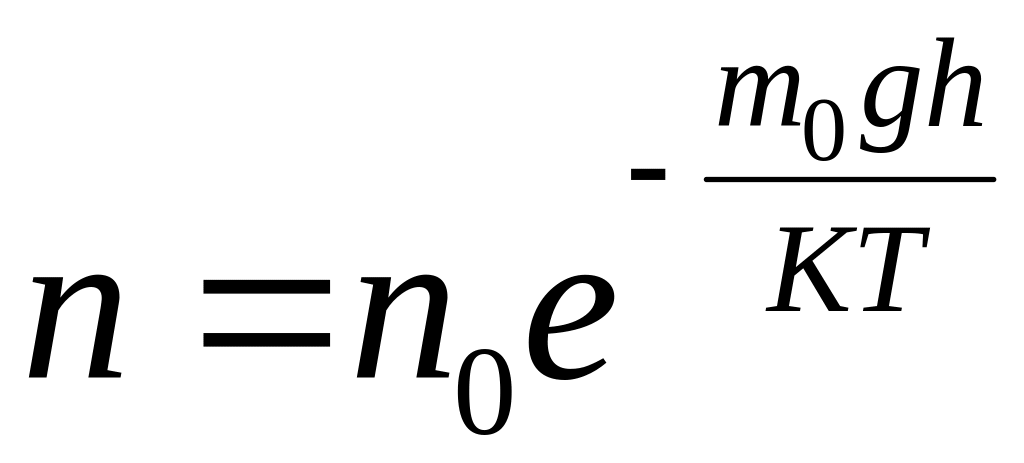 (*).
Величина
(*).
Величина
![]() -потенциальная
энергия, кот. обладает молекула на данной
высоте. Тогда
-потенциальная
энергия, кот. обладает молекула на данной
высоте. Тогда
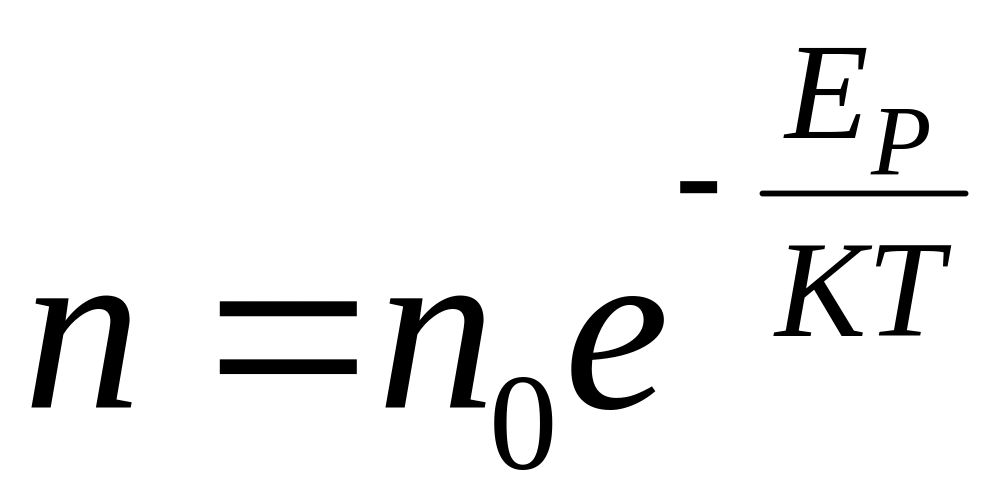 ,
,
 -доля молекул для высоты
с энергией
-доля молекул для высоты
с энергией
![]() .
.
Существ. в атмосфере
распределения молекул воздуха по высоте
устанавливается в результате действия
двух факторов: 1) под действием силы
тяжести молекула стремится опустится
на поверхность Земли. 2) Тепловое движение,
характеризуемое величиной
![]() ,
стремится распределить молекулы
равномерно по высотам.
,
стремится распределить молекулы
равномерно по высотам.
Формула (*) определяет распределение молекул по высоте и выражает также распределение их по значениям потенц. энергии справедливо не только для поля силы тяжести, но и для любого поля потенц. сил.
21. Опытное обоснование мкт (опыт Штейна, броуновское движение, опытное определение постоянной Авогадро).
1. Суть опыта Штейна: берём платиновую проволоку, покрываем её серебром и располагаем по оси цилиндра. Внутри цилиндра находится ещё один цилиндр с прорезью, через которую был удалён воздух. Проволока разогревалась, атомы серебра испарялись и летели в разные стороны.
2. Опытное определение постоянной Авогадро:
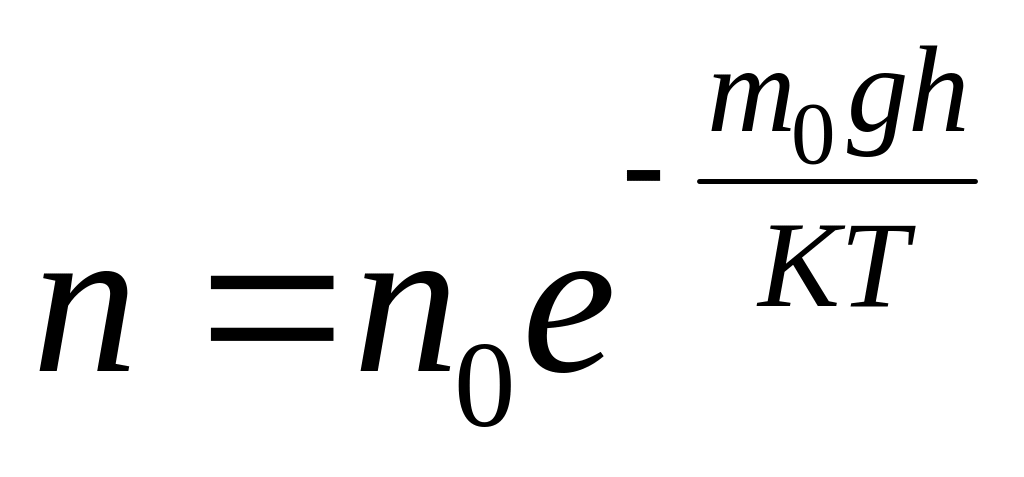 - концентрация на
различных уровнях
- концентрация на
различных уровнях
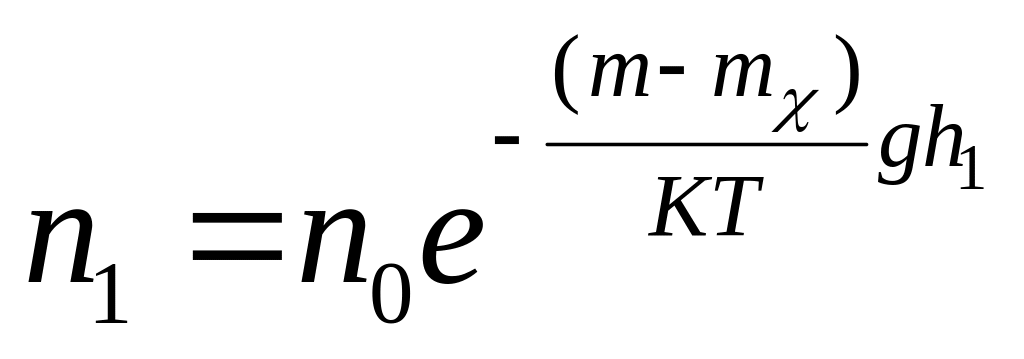
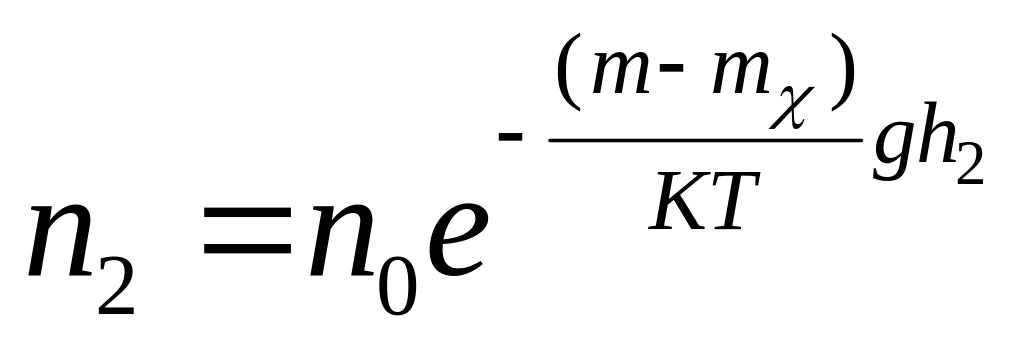
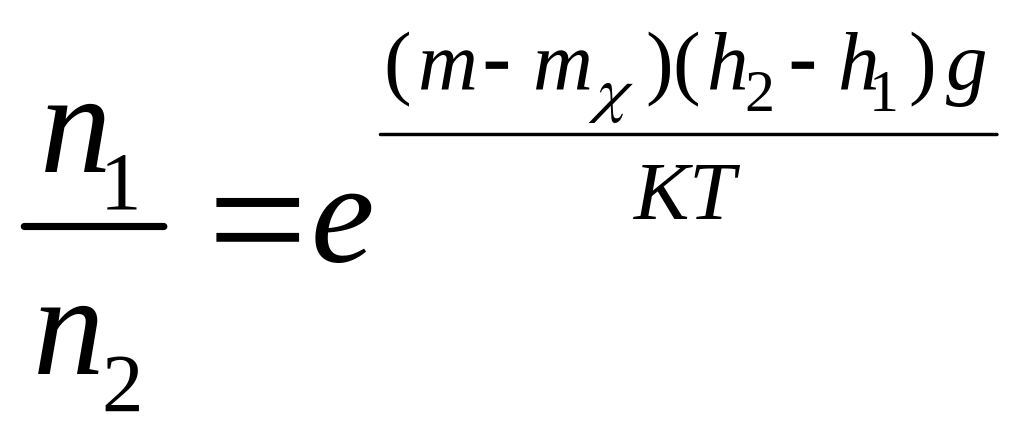
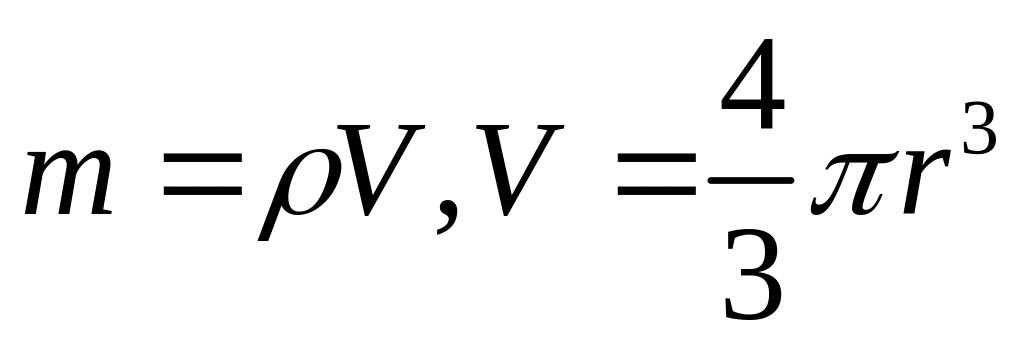
Тогда масса частицы равна
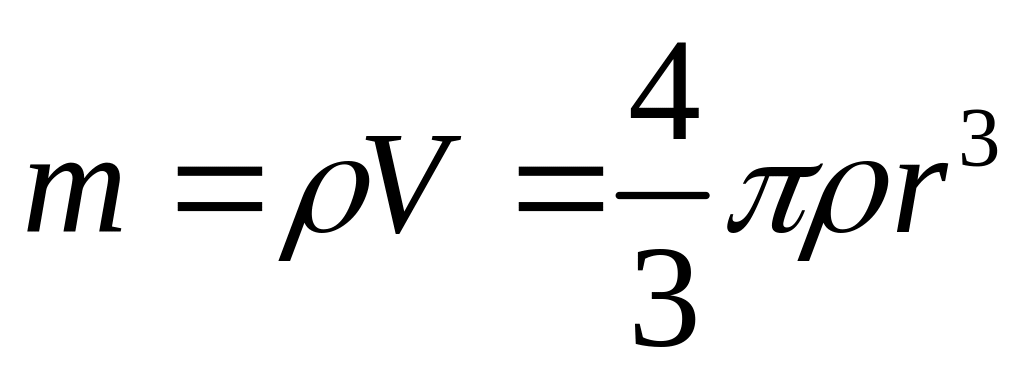
Тогда масса жидкости равна
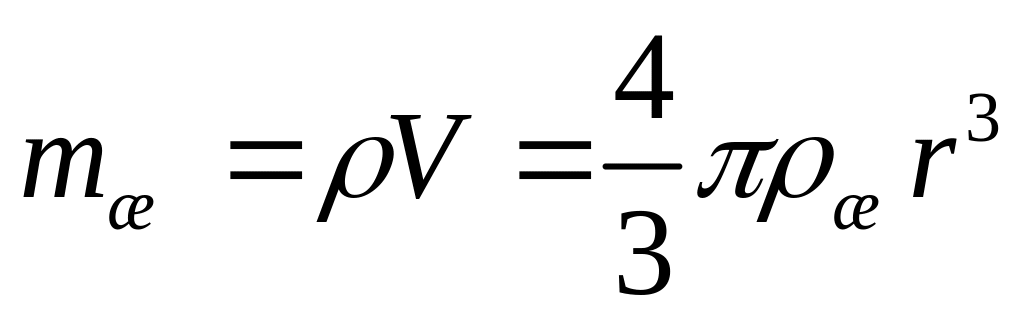
Следовательно,
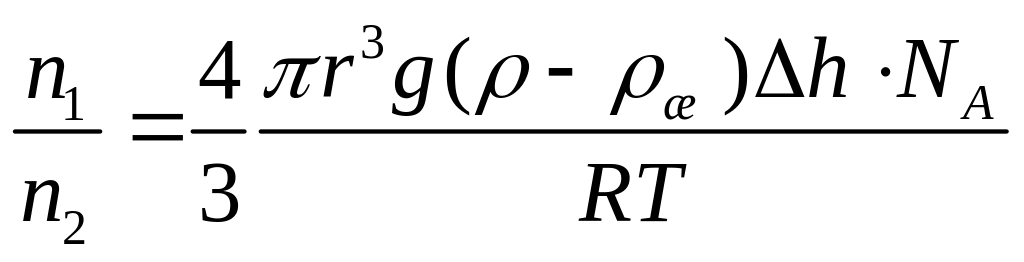
Число Авогадро
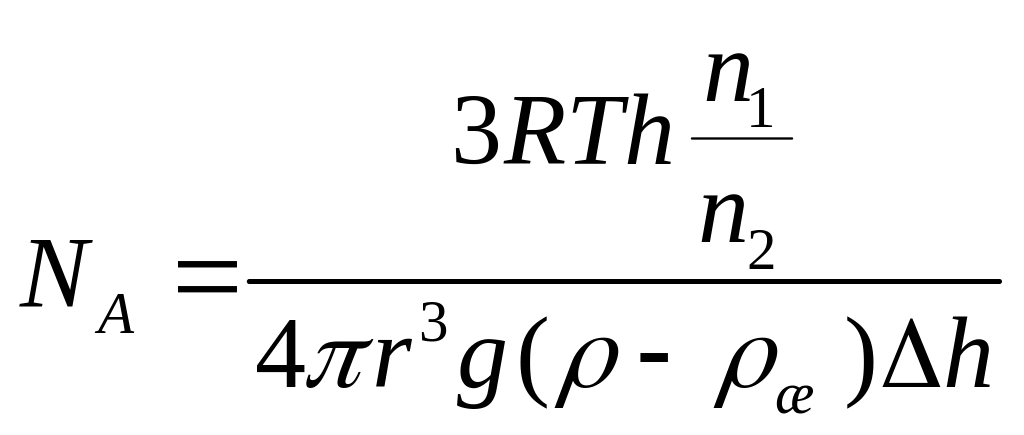
22. Внутренняя энергия. Закон Больцмана о равномерном распределении энергии по степеням свободы молекул.
Под внутренней энергией термодинамической системы понимаем все виды энергии, кроме механической энергии системы (кинетической и потенциальной).
Внутренняя энергия – функция состояния системы и является полным дифференциалом. Свяжем молекулы (одноатомные, двухатомные и трёхатомные с xyz).
1.Одноатомная молекула
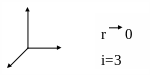
2. Двухатомная
молекула
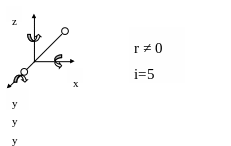
3. Трёхатомная молекула
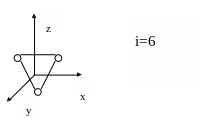
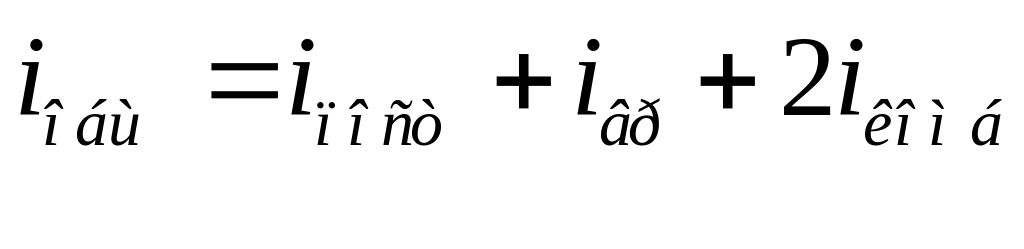
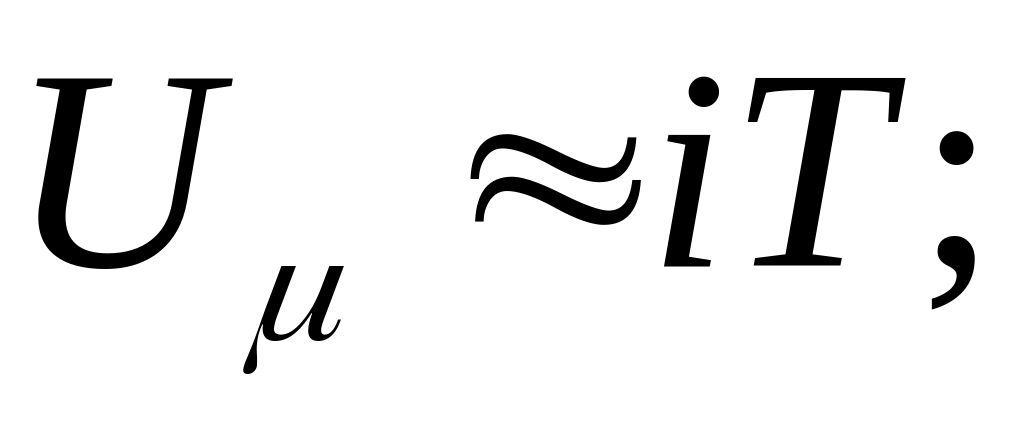
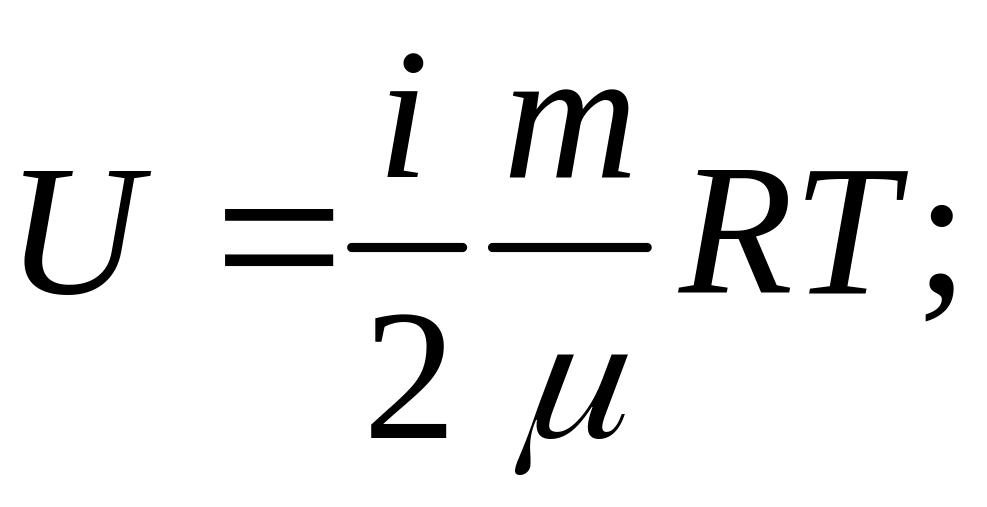
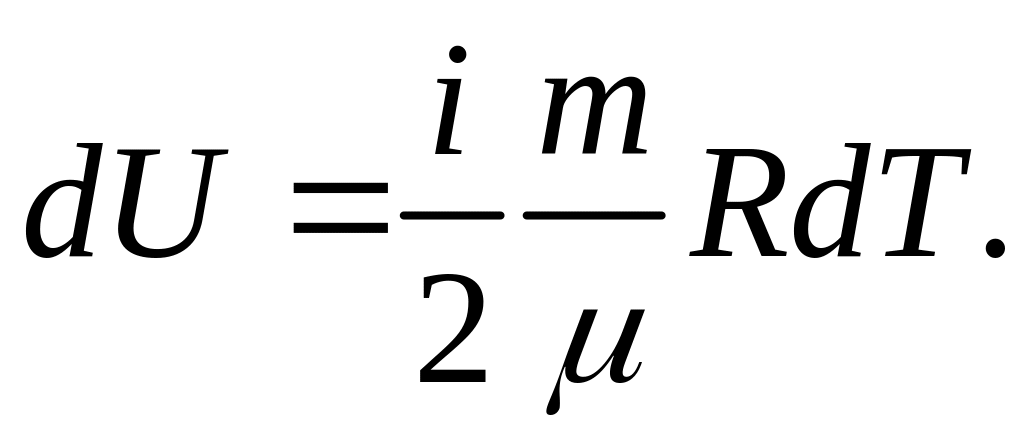
23. Работа и теплота. Пнт.
![]() -
элементарная работа
-
элементарная работа
![]()
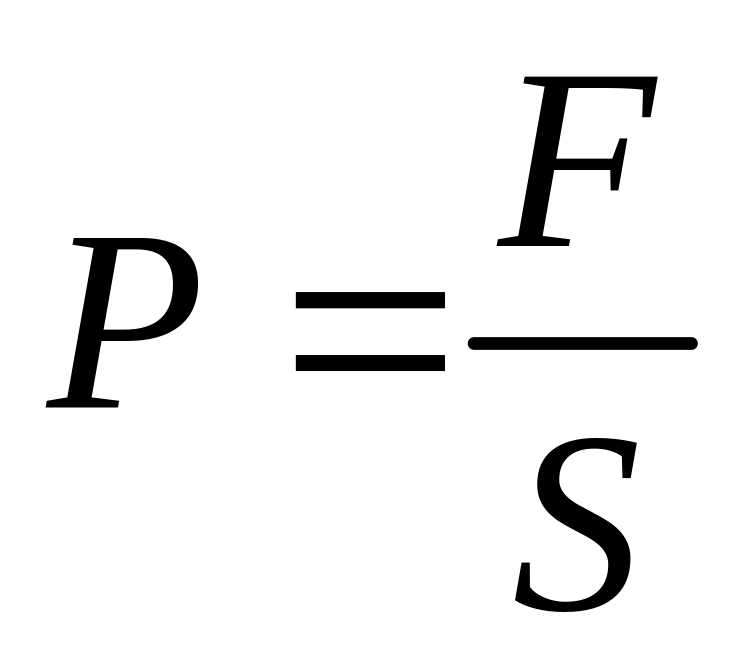 -
давление
-
давление
![]()
![]()
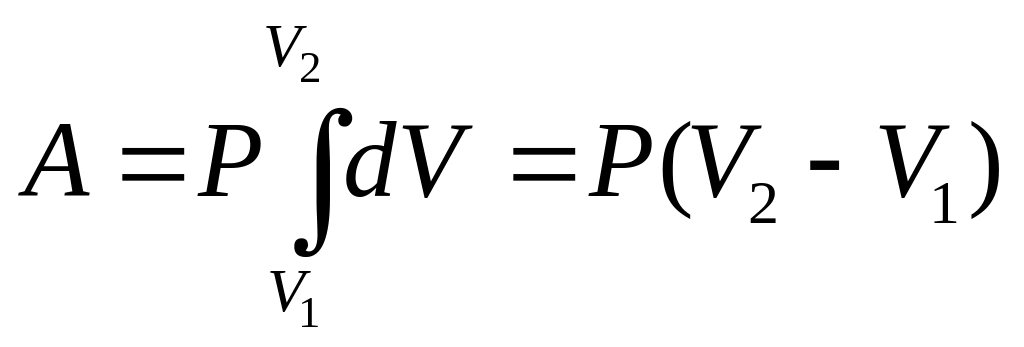 (если Р - постоянное)
(если Р - постоянное)
1. при ΔV>0, ΔA>0 – работа выполняется против внешних сил
2. при ΔV<0, ΔA<0
3. при ΔV=0, ΔA=0
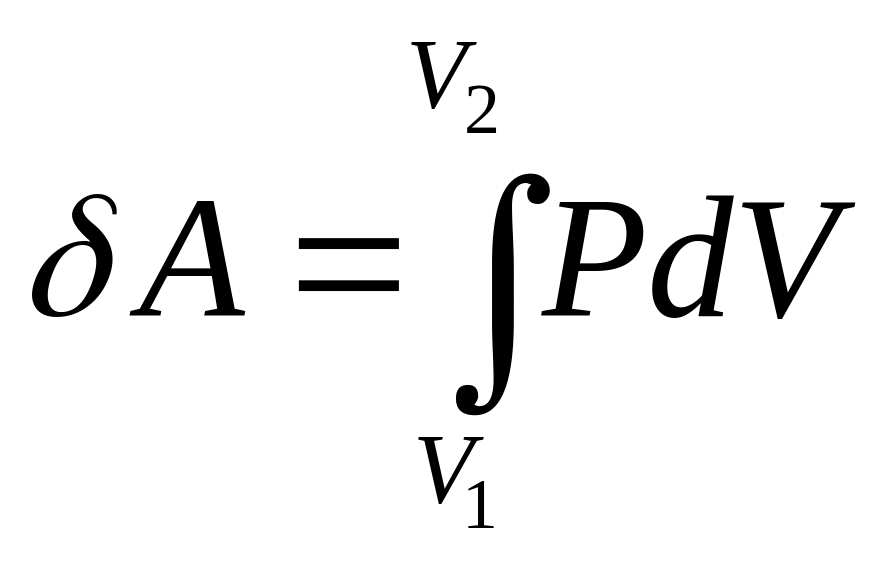
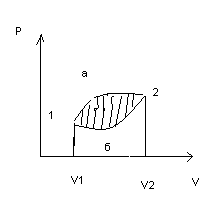

Количество теплоты есть мера изменения той части внутренней энергии, которая обусловлена хаотическим движением частиц, образующих систему. Количество теплоты, получаемая или отдаваемая системой, зависит от пути перехода, поэтому элем. изменение теплоты не является дифференциалом ф-ии параметра системы, т. е. функционал δQ, процесс совершения системой работы и процесс передачи тепла – это качественные различные формы передачи энергии. Работа проявляется в передаче энергии упорядоченного движения, а теплота – в передаче движения хаотического движения частиц.
ΔQ=ΔU+A
δQ=dU+δA
Эти два выражения – матем. Выражения ПНТ(1. в интегральной форме, 2. в дифференциальной форме)
В диф. форме ПНТ: количество теплоты δQ, сообщённая системой, равно сумме изменения её внутр. энергии dU и работы, совершаемой системой над внешней средой.
В интегр. форме
ПНТ: полное количество теплоты Q,
полученное системой, идёт на превращение
её внутренней энергии
![]() и на совершение работы над внешней
средой.
и на совершение работы над внешней
средой.
