
- •Глава 1. Некоронарогенные болезни
- •I II. Стандарты и критерии диагностики воспалительных поражений сердца
- •Глава 2. Функциональные болезни сердца
- •(Заполняется врачом)
- •Глава 3. Метаболические и дегенеративные (дистрофические)
- •Глава 4. Перикардиты
- •Глава 5. Эндокардиты
- •Глава 6. Миокардиты
- •Глава 7. Пролапс митрального клапана
- •Глава 8. Приобретенные пороки сердца
- •Глава 9. Врожденные пороки сердца
- •Глава 10. Дилатационная кардиомиопатия
- •Глава 11. Гипертрофическая кардиомиопатия
- •Глава 12. Рестриктивная кардиомиопатия
- •Глава 13. Аритмогенная кардиомиопатия (дисплазия) правого желудочка
- •Глава 14. Опухоли сердца
- •Глава 15. Травмы сердца
Глава 5. Эндокардиты
Инфекционный эндокардит — воспалительное заболевание эндокарда инфекционной этиологии, обусловленное инвазией возбудителя с его локализацией на клапанных структурах, эндокарде, эндотелии в зоне прилегающих к сердцу магистральных сосудов, сопровождающееся, как правило, бактериемией и поражением различных органов и систем организма.
Первое описание инфекционного эндокардита относится к 1646 г., когда L. Riviere указал на повреждение эндокарда при злокачественной лихорадке. Основоположником учения об инфекционном эндокардите считают Osier, который в 1885 г. подробно описал заболевание и высказал предположение о его инфекционной природе. Он считал возможным развитие первичного патологического процесса на неизмененных клапанах, вторичного — на фоне ревматизма, пневмонии, дифтерии и др. Термин «инфекционный эндокардит» впервые использовал S. Jaccoud в 1885 г.
В течение последних 10-15 лет отмечается увеличение заболеваемости инфекционным эндокардитом, что может быть обусловлено несколькими факторами:
распространением операций, выполняемых на сердце, — появле нием инфекционного эндокардита протезированного клапана;
повышенной предрасположенностью к заболеванию при наличии:
врожденных пороков сердца (в том числе двустворчатого аор тального клапана),
пролапса митрального клапана,
приобретенных пороков сердца,
гипертрофической обструктивной кардиомиопатии,
операции на сердце без замены клапанов;
постинъекционными абсцессами после введения различных лекар ственных средств;
широким использованием инвазивной инструментальной техни ки (катетеров, искусственных водителей ритма сердца), вводимой в сердце и сосуды;
W7
Некоронарогенные болезни сердца
• появлением своеобразной формы — инфекционного эндокардита у наркоманов.
Инфекционный эндокардит может возникать в любом возрасте, до создания антибиотиков наиболее часто им заболевали лица среднего возраста, в последние десятилетия пик заболеваемости сместился к 50-летнему возрасту, в 5 раз увеличилось число заболевших в возрасте старше 60 лет. Мужчины болеют в 2 раза чаще, чем женщины.
Этиология. Инфекционный эндокардит — полиэтиологическое заболевание, потенциальными возбудителями которого могут быть до 128 разновидностей микроорганизмов. Основными среди них являются стрептококк и стафилококк, которые высеваются у 75- 90% больных.
Из всех штаммов стрептококка наиболее часто высевают зеленящий стрептококк. Факторами, способствующими его инвазии, являются тонзиллит, фарингит, манипуляции в полости рта (экстракция зубов), хирургические вмешательства. Удается выделить и другие штаммы стрептококка, в том числе условно-патогенные, являющиеся компонентами нормальной микрофлоры полости рта и кишечника. Прежде всего это энтерококк, вызывающий инфекционный эндокардит в 10-18% случаев. Ему чаще предшествует мочеполовая инфекция или заболевания пищеварительного тракта, у женщин — акушерские полостные операции, катетеризация мочевого пузыря, применение внутри-маточных контрацептивов.
Повышение этиологической роли стафилококка за последние 10— 15 лет объясняется широким внедрением в клиническую практику антибиотиков, а также распространением инвазивных процедур. Инфекционный эндокардит стафилококковой этиологии часто возникает после операций на сердце, имплантации эндокардиального электрода искусственного водителя ритма сердца, инвазивных инструментальных исследований (катетеризация полостей сердца), длительного применения внутривенных катетеров, хронического гемодиализа, гемосорбции, при наличии инфицированных и гнойных ран, абсцессов, пиодермии, а также у инъекционных наркоманов. У таких больных чаще высевается золотистый стафилококк, который вызывает за-
Некоронарогенные болезни сердца
болевание с острым началом, поражает интактные клапаны, быстро приводя к их разрушению, эндокардит протекает с гектической лихорадкой и гнойно-септическими осложнениями.
Пневмококковый эндокардит особенно часто диагностируется у больных после кардиохирургического вмешательства с имплантацией искусственных материалов, а также у пациентов, перенесших в послеоперационный период пневмонию.
Реже причиной инфекционного эндокардита являются коринебак-терии (дифтероиды) — грамположительные палочки, которые входят в состав микробной флоры верхних дыхательных путей. Заболевание отличается стертостью клинической симптоматики, может осложняться развитием миокардита, нефрита, васкулита.
Наблюдения последних лет свидетельствуют об увеличении удельного веса грамотрицательной микрофлоры в этиологии инфекционного эндокардита; эшерихий, протея, сальмонелл, синегнойной палочки, клебсиелл, которые являются причиной заболевания в 3-8% случаев. Потенциальным возбудителем является кишечная палочка, для которой характерно вторичное поражение эндокарда, практически не поддающееся антибактериальной терапии.
Инфекционный эндокардит вызывают также редко встречающиеся возбудители: серрации, морракселлы, иерсинии, акинетобактер, фла-вобактер, цитробактер, энтеробактер, кардиобактер. У наркоманов гра-мотрицательные бактерии вызывают заболевание в 5-64% случаев.
Возросла и частота эндокардита, вызванного грибами (1,5-6%), из возбудителей преобладают дрожжеподобные грибы. Грибковый эндокардит возникает у ослабленных больных, длительно получающих антибактериальную, глюкокортикоидную и цитостатическую терапию, в 5-14% случаев — у наркоманов.
В последнее время в возникновении инфекционного эндокардита возросла этиологическая роль анаэробной флоры, однако механизм повреждающего действия анаэробов на эндотелий не изучен. Предполагается, что повреждающая роль анаэробных бактерий реализуется только совместно с аэробными микроорганизмами. Эндокардит, вы-
109
з ванный анаэробной микрофлорой, характеризуется выраженной манифестацией патологического процесса с развитием тромбофлебитов, высоким риском возникновения тромбоэмболии сосудов легких, сердца, головного мозга, рефрактерностью к традиционной антибиотико-терапии, высоким уровнем летальности (до 46%).
Далеко не всегда удается выделить возбудителя из крови больных инфекционным эндокардитом, поэтому во многих случаях истинный возбудитель болезни остается неизвестным. В 50-55% случаев в острый период и в 80- 85% случаев в подострый период посевы крови оказываются стерильными. Причинами, затрудняющими идентификацию возбудителя заболевания, являются предшествующая забору крови антибактериальная терапия, несовершенное бактериологическое оборудование для проведения посева, наличие в крови бактерий, требующих применения специальных сред (анаэробы, сателлиты и штаммы стрептококка с измененными свойствами (тиол- или витамин В6-зави-симые), L-формы бактерий, бруцеллы). Для выделения вирусов, рик-кетсий, хламидий, грибов требуются специальные методы.
Патологическая анатомия. Внутренняя оболочка сердца, или эндокард, выстилает все полости сердца, плотно сращена с подлежащим мышечным слоем, образована из коллагеновых и эластичных волокон, среди которых располагаются соединительнотканные и гладкомышеч-ные клетки. Со стороны полостей сердца эндокард покрыт эндотелием. На внутреннюю оболочку отходящих от сердца и впадающих в него сосудов— полых и легочных вен, аорты и легочного ствола— эндокард переходит без резких границ.
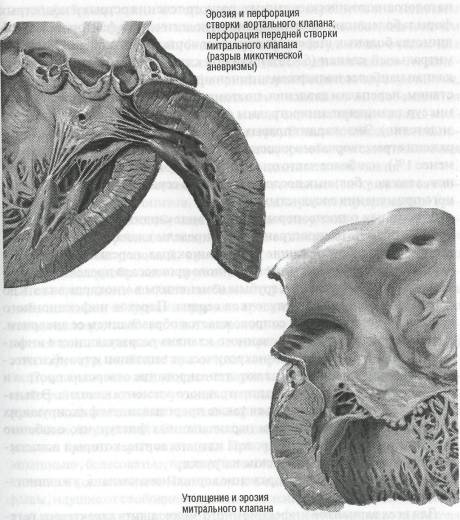
При эндокардите сердце увеличено, обычно преобладает гипертрофия левых отделов в связи с недостаточностью клапана аорты (рис. 8). В миокарде, помимо признаков воспаления, выявляют выраженные дистрофические и некробиотические поражения в виде базофильной и паренхиматозной дистрофии, атакже микромаляций и микроучастков глыбчатого распада мышечных волокон.
В вопросе о преимущественной локализации септического очага на клапанах сердца нет единого мнения ввиду различия клинических и
Некоронарогенные болезни сердца
Рис. 8. Инфекционный эндокардит (по F. Netter, 1969, с изменениями)
Некоронарогенные болезни сердца
патологоанатомических данных, разного течения острых и подострых форм заболевания, многоообразия этиологических факторов. У большинства больных инфекция поражает аортальный клапан (28-45%) митральный клапан (5-36%) или оба клапана (до 35%). Аортальный клапан наиболее подвержен интенсивным гемодинамическим воздействиям, перепадам давления, поэтому по краям створок, в области ко-миссур возникают микротравмы (микрокровоизлияния, деструкция эндотелия). Эндокардит правых отделов сердца встречается реже (поражения трехстворчатого клапана — до 6%, клапана легочной артерии — менее 1 %), наиболее часто он наблюдается у инъекционных наркоманов, а также у больных после операции на сердце и в случаях длительного применения сосудистых катетеров.
У больных с послеоперационным эндокардитом инфекционный процесс обычно распространяется за пределы клапана, поражая фиброзное кольцо, близлежащие участки миокарда, нередко и другие клапаны. Распространение инфекционного процесса за пределы фиброзного кольца может вести к грубым изменениям в миокарде вплоть до образования аневризм желудочков сердца. Переход инфекционного процесса на стенку аорты сопровождается образованием ее аневризм. При эндокардите протезированного клапана разрастающиеся инфицированные грануляционно-некротические вегетации и тромботичес-кие наслоения обычно вызывают стенозирование отверстия протеза и ограничение подвижности запирательного элемента клапана. Эти изменения могут сопровождаться также прорезыванием фиксирующих протез нитей и образованием параклапанных фистул, что особенно характерно для поражения протеза клапана аорты, который испытывает большие гемодинамические нагрузки.
У мужчин преобладает поражение аортального клапана, у женщин -митрального.
Для всех вариантов инфекционного эндокардита характерны вегетации, которые наиболее часто располагаются на створках клапанов и реже — на эндокарде желудочков или левого предсердия, а также на легочной или других артериях. Свежие вегетации состоят из тонких
112
Некоронарогенные болезни сердца
нитей фибрина, среди которых выявляют эритроциты и в меньшем количестве — смешанно-клеточные лейкоциты, тромбоциты и почти всегда колонии бактерий. Очевидно, внутрисосудистым очагом для микроорганизмов в сердце и кровеносных сосудах являются стерильные вегетации, состоящие из фибрина и тромбоцитов, образующиеся, когда поврежденными эндотелиальными клетками высвобождается тканевой фактор. Тромботические массы сначала представляют мелкозернистые структуры, состоящие из тромбоцитов; позднее в них появляется примесь фибрина и лейкоцитов, тромботические наслоения организуются путем врастания в них соединительной ткани.
Микроорганизмы, колонизирующие вегетации, покрываются слоем фибрина и тромбоцитов, что не дает доступа нейтрофильным гра-нулоцитам, иммуноглобулинам и комплементу, таким образом позволяя патогенам противостоять защитным силам организма. Свежие вегетации имеют розовый, красный, желтый или зеленый цвет, но постепенно приобретают серую окраску. При грибковой инфекции клапанов вегетации достигают наибольших размеров, создавая опасность эмболизации и обтурации крупных артерий, что характерно для этого типа эндокардита. Вегетации митрального клапана могут распространяться вдоль хорд к вершине папиллярных мышц, приводя к разрыву этих структур, особенно при острых инфекциях.
При первичном эндокардите створки клапанов чаще тонкие, свободный край клапанов часто утолщен, что вызвано гемодинамическими нарушениями или воспалительной инфильтрацией. По свободному краю клапанов, внутренней оболочке восходящей части аорты располагаются рыхлые красно-серые вегетации. При грибковой инфекции вегетации «пышные», белесоватые, при стафилококковой — с выраженным некротическим компонентом. Чаще в аортальных клапанах наблюдаются надрывы, идущие от свободного края изъязвления, край створок бахромчатый, имеются разрывы створок поперечного и лентовидного характера. Сухожильные хорды тонкие, могут отмечаться их разрывы в области прикрепления к створкам и сосочковым мышцам, а также в центре хорд с явлениями острого некроза. На обрывках сухожильных хорд обнаружи-
т
Некоронарогенные болезни сердца
ваются вегетации. При подостром процессе наряду со свежими имеются вегетации, покрытые фиброзной капсулой, частично или полностью обызвествленные, нередко на ножке, часто организованные вегетации полностью кальцинированы. Элементы свежей деструкции створок сочетаются с перфорациями, имеющими фиброзные края. Характерно наличие фиброзных утолщений разорванных хорд. Нередко в крае разрыва видны кальциевые массы.
При вторичном эндокардите, когда инфекционный процесс поражает уже измененный клапан, свежие вегетации располагаются на фиброзно-измененных или кальцинированных створках, возможен отрыв хорд.
В неактивной стадии инфекционного эндокардита (стадии заживления) видны старые перфорации и разрывы створок с фиброзными краями. Вегетации представлены фиброзными бугорками или полностью кальцинированы.
При инфекционном эндокардите в связи с септикопиемией происходят многообразные вторичные дистрофические и интоксикационные изменения всех жизненно важных органов. На коже обнаруживаются множественные петехии. Селезенка увеличенная, дряблая, с большим соскобом пульпы. При микроскопическом исследовании обнаруживается инфильтрация нейтрофильными гранул оцитами, гиперплазия ретикулярных клеток, лимфатические фолликулы без четких контуров, аргирофильная строма находится в состоянии расплавления. В печени преобладают циркуляторные и дистрофические изменения. В почках обнаруживаются микроабсцессы и инфаркты различной величины.
Патогенез. Вопросы патогенеза инфекционного эндокардита сложны и окончательно не выяснены. В большинстве случаев в анамнезе имеются указания на порок сердца, атеросклероз, операции на сердце, которые предрасполагают к избирательной адгезии микроорганизмов на эндокарде. При первичном инфекционном эндокардите инфекция поражает здоровые клапаны. Однако и в этих случаях имеются микроструктурные повреждения эндокарда, являющиеся следствием ряда состояний, сопровож-
П4
Некоронарогенные болезни сердца
дающихся функциональными перегрузками сердца, во время которых усиленная работа клапанов, особенно в местах соприкосновения створок у комиссур при усиленном их захлопывании, вызывает механическую деструкцию эндотелия. Возникновение эндокардита, по-видимому, следует рассматривать как результат микроструктурных изменений в эндокарде под влиянием функциональных гемодинамических перегрузок. Эти причины в той или иной степени объясняют появление наиболее уязвимого места в эндокарде как местного фактора, обусловливающего данную локализацию инвазии возбудителя.
При инфекционном эндокардите возбудитель локализуется и размножается на клапанах сердца, куда он попадает из тока крови во время преходящей или постоянной бактериемии. Транзиторная бактериемия часто наблюдается при различных инфекциях и во время травмирующих процедур, включая инвазивные исследования, в том числе бронхоскопию, гастроскопию, колоноскопию, хирургические вмешательства, прежде всего, тонзиллэктомию, аденоидэктомию, хирургические манипуляции в ротовой полости. После травмы тканей ротовой полости вирулентные стрептококки наиболее часто выявляются в крови. Считается, что в большинстве случаев «входными воротами» инфекции является одонтогенная (экстракция зубов, удаление корней зубов).
Возможность развития инфекционного эндокардита зависит от выраженности, частоты и видовой специфичности бактериемии. Чаще всего толчком к развитию септического эндокардита является транзиторная бактериемия. Преходящая бактериемия обычно не приводит к оседанию бактерий на эндокарде неповрежденных клапанов, однако при определенных условиях происходит фиксация бактерий к клапанному и париетальному эндокарду. Под влиянием этиологических факторов на фоне измененной реактивности всего организма и клапанного аппарата возникает интерстициальный вальвулит, небактериальный эндокардит, затем происходит присоединение инфекции, развивается инфекционное поражение клапанов с бактериемией и тромбоэмболическими осложнениями.
Факторы, облегчающие адгезию микроорганизмов на эндотелиаль-ной поверхности, подразделяются на местные и общие. Одной из при-
Некоронарогенные болезни сердца
чин фиксации микроба являются нарушения внутрисердечной гемодинамики у больных с врожденными и приобретенными пороками сердца, возникающие перепады давления крови между камерами сердца, образование регургитационных потоков при недостаточности или интенсивных потоков крови при стенозе и дефектах перегородок. Инвазия микроорганизмов и возникновение эндокардита происходят преимущественно в местах высокого градиента давления, клапанной регур-гитации и сужения межполостных сообщений, поэтому инфекционный эндокардит чаще наблюдается при пороках левых отделов сердца, чем правых, так как давление крови в первых в 5 раз выше. Эндокардит редко возникает в участках с небольшим градиентом давления, например при дефектах межпредсердной перегородки. Наряду с прямым повреждающим действием тока крови, текущей с большой скоростью или под большим давлением и нарушающей трофику эндокарда, имеют значение гемодинамические изменения дистальнее суженного участка. Гемодинамическими факторами объясняют расположение вегетации на желудочковой поверхности аортального клапана и на пред-сердной поверхности митрального клапана, большую вероятность заболевания при незначительном дефекте межжелудочковой перегородки, чем при обширном, а также относительную редкость инфекционного эндокардита у больных с фибрилляцией предсердий и сердечной недостаточностью: инфекционный эндокардит возникает в местах наибольшей функциональной нагрузки.
К общим факторам, способствующим развитию инфекционного эндокардита, могут быть отнесены выраженные изменения иммунного статуса организма, наблюдающиеся у наркоманов, больных алкоголизмом, лиц пожилого возраста, пациентов, имеющих определенные нарушения в HLA-системе гистосовместимости, а также у получающих иммуносупрессивную терапию. Эти нарушения, по-видимому, играют важную роль как в период инфицирования, так и при последующем течении заболевания. Ряд иммунологических изменений при инфекционном эндокардите может возникать вторично вследствие наличия в сердце активного очага инфекции. Фиксированные на кла-
Ji6
Некоронарогенные болезни сердца
панах микробы образуют колонии, вызывают развитие иммунных нарушений, обусловливая повреждение различных органов и тканей.
В патогенезе инфекционного эндокардита выделяют три фазы: ин-фекционно-токсическую, иммуновоспалительную (иммунной генерализации процесса) и дистрофическую (с дистрофическими изменениями внутренних органов).
Ключевые процессы патогенеза инфекционного эндокардита происходят на молекулярном уровне. Пусковым фактором является микробный эндотоксин — липополисахарид А, преимущественно содержащийся в грамотрицательных бактериях. Липополисахаридные эндотоксины устойчивы к повышению температуры и образуют на поверхности вырабатывающих их бактериальных клеток прочную оболочку, защищающую от действия антибиотиков. После высвобождения из бактериальной клетки эндотоксин связывается со специфичным белком, образующийся комплекс связывается с рецептором CD 14 (имеющимся на макрофагах), в результате чего происходит выброс медиаторов воспаления. Известно около 40 медиаторов воспаления, которые участвуют в реализации каскада тяжелых патологических процессов при сепсисе.
Воздействие эндотоксина приводит к угнетению защитных сил организма, в частности, при развитии инфекционного эндокардита происходят истощение антиоксидантных ресурсов и накопление продуктов переокисления, что проявляется повышенным уровнем перекис-ного окисления липидов.
Вопрос о характере иммунологических нарушений при инфекционном эндокардите остается недостаточно ясным и требует дальнейшего изучения. Иммунологические изменения затрагивают как гуморальные, так и клеточные факторы системы иммунитета. Показатели иммунограмм свидетельствуют об угнетении функции Т-лимфоцитов в активной стадии заболевания и гиперфункции В-лимфоцитов.
Среди важнейших изменений гуморального иммунитета можно отметить:
1) поликлональную гипергаммаглобулинемию с высокими титрами иммуноглобулинов классов М и G;
117
Некоронарогенные болезни сердца
высокие титры антител (криоглобулины, ревматоидный фактор, антимиокардиальные антитела);
нарушения в механизме активации комплемента;
повышение образования циркулирующих иммунных комплек сов — ведущий признак дисфункции гуморального иммунитета.
Больные с эндокардитом обычно имеют высокие титры антител к патогенным микроорганизмам, что активизирует формирование циркулирующих иммунных комплексов, которые способствуют развитию артрита или васкулита. Продукции циркулирующих иммунных комплексов придается исключительно важное значение, так как возникновение гломерулонеф-рита (фокального, мембранопролиферативного, диффузного) при инфекционном эндокардите рассматривается с новых патогенетических (имму-нокомплексных) позиций. Данные иммунофлуоресцентной микроскопии биоптатов почек позволили обнаружить отложения комплемента и иммуноглобулинов (чаще класса G) на базальной мембране капилляров клубочков. В дистрофической фазе инфекционного эндокардита может возникать миокардит вследствие эмболизации коронарных артерий небольшого калибра, миокардиального абсцесса или иммунокомплексного васкулита.
Разграничить фазы в течении инфекционного эндокардита часто не удается, эти процессы могут протекать одновременно, поэтому можно лишь констатировать преобладание в клинической картине тех или иных симптомов: при инфекционно-токсических проявлениях на первый план выступают септические симптомы, при иммуновоспалитель-ных проявлениях преобладают иммунологические осложнения. От соотношения инфекционно-токсических и иммуновоспалительных проявлений отчасти зависит многообразие клинической картины болезни.
Классификация. Для решения лечебно-тактических вопросов диагностики инфекционного эндокардита целесообразно пользоваться клинической классификацией, которая бы учитывала этиологическую, патогенетическую сущность, а также отражала многогранность кли-нико-морфологических проявлений заболевания. В Украине используется классификация инфекционного эндокардита, принятая на VI Конгрессе кардиологов (Киев, 2000): _
Некоронарогенные болезни сердца
Эндокардит- 139(МКБ-10)
I. Активность процесса: активный, неактивный
П. Эндокардит нативных клапанов:
первичный
вторичный (приобретенные пороки сердца, врожденные пороки сердца, травма, инородные тела)
Эндокардит протезированного клапана
III. Локализация:
аортальный клапан
митральный клапан
трехстворчатый клапан
клапан легочной артерии
эндокард предсердий или желудочков
IV. Возбудитель (грамположительные, грамотрицательные микроор ганизмы, L-формы бактерий, риккетсии, грибы)
V. Стадия порока клапана; стадия сердечной недостаточности
VI. Осложнения
Наличие признаков активного воспалительного процессса (лихорадка, изменения показателей клинических и биохимических анализов крови, наличие вальвулита) свидетельствуют об активном инфекционном эндокардите. По течению различают острый, подострый или затяжной, хронический рецидивирующий и латентный инфекционный эндокардит. К острому относят случаи заболевания длительностью до 2 мес, более 2 мес — к подострому. Помимо временного различия между этими вариантами течения инфекционного эндокардита существуют этиологические, патогенетические и клинические различия. Устранение признаков воспалительного процесса позволяет диагностировать неактивный эндокардит.
Острый септический эндокардит, как правило, возникает на неизмененных клапанах сердца как осложнение сепсиса (хирургического, гинекологического, урологического), а также как осложнение инъекций, инвазивных диагностических манипуляций (инфицирование подключичных катетеров и артериовенозных шунтов). При этом быстро проис-
119
Некоронарогенные болезни сердца
ходит деструкция клапана, образуются метастатические очаги и при отсутствии лечения летальный исход наступает менее чем через 6 нед.
Подострый септический (инфекционный) эндокардит обычно вызывается вирулентным стрептококком, который локализуется на пораженных клапанах, не образует метастатических очагов. Без лечения заболевание может длиться более 6 нед, иногда даже год до фатального исхода. Это особая форма сепсиса, обусловленного наличием внутрисердечного (или в прилежащих артериальных стволах) инфекционного очага, приводящего к рецидивирующей септицемии, эмболиям, нарастающим иммунным нарушениям с развитием вторичных процессов иммунопатологического ге-неза: васкулита, гломерулонефрита, синовита, серозита.
Затяжной септический эндокардит — этиологический вариант под-острого септического эндокардита, вызываемый зеленящим стрептококком или близкими ему штаммами стрептококка, с изначально хро-низированным течением, отсутствием гнойных метастазов, преобладанием иммунопатологических проявлений.
Подострый инфекционный эндокардит может иметь типичное течение с развернутой клинической картиной или протекать атипично, симулируя другую патологию.
К хроническому рецидивирующему варианту течения относят заболевания продолжительностью более 1,5 года. По мнению некоторых авторов (Демин А.А., Демин Ал. А., 1978), выделение хронической формы инфекционного эндокардита нецелесообразно, так как в ряде случаев это отражает несвоевременную диагностику заболевания, неоправданно длительную консервативную терапию, позднее хирургическое вмешательство.
В редких случаях инфекционный эндокардит может протекать латентно при минимальной активности процесса: больные обращаются к врачу лишь в фазе декомпенсации сформированного порока сердца.
Деление инфекционных эндокардитов на первичные и вторичные имеет принципиально важное значение для клиники, течения и прогноза заболевания. Обычно первичный инфекционный эндокардит про -текаеттяжелее, труднее и позже диагностируется, плохо поддается лечению, отличается большим процентом летальности. В последние годы
120
Некоронарогенные болезни сердца
отмечается повышение частоты случаев первичного инфекционного эндокардита (до 40- 65%). К вторичному инфекционному эндокардиту относят случаи заболевания, развившегося на фоне ревматических, ате-росклеротических, врожденных, травматических и иных пороков сердца, после операций на сердце. Искусственный клапан также создает благоприятные условия для развития эндокардита: инфицирование протезированных клапанов происходит у 2- 3% больных в течение года после операции и у 0,5% больных в каждый последующий год.
Клиника инфекционного эндокардита отличается значительным многообразием симптомов, что определяет и трудности диагностики. Болезнь может манифестировать внезапно или длительно протекать латентно, иметь быстрое или затяжное течение. Клиническая картина заболевания, его течение и исход в каждом конкретном случае зависят как от состояния защитных сил организма, его неспецифической резистентнос-ти и реактивности, так и от вида инфекционного возбудителя.
Клинические проявления обычно развиваются в течение 2 нед с момента инвазии. Одним из основных симптомов является лихорадка, которая может сопровождаться ознобами, потливостью. Температурная реакция варьирует от высокой упорной лихорадки на протяжении нескольких месяцев до незначительного повышения температуры тела в течение нескольких дней с последующей стойкой ее нормализацией.
Наблюдения за больными позволили выявить основные типы температурных кривых: а) транзиторный тип характеризуется недлительным субфебрилитетом, отмечается у 40% больных в начальной стадии эндокардита; б) интермиттирующая 1-2-недельная или 1-2-дневная высокая лихорадка чередуется с 1- 2-недельными периодами нормальной или субфебрильной температуры тела; в) стойкое умеренное повышение температуры тела сохраняется длительно на фоне лечения и после ликвидации очагов хронической инфекции; г) при гектической температуре суточный градиент достигает 2- 3 °С, наблюдается озноб и повышенная потливость; д) при гипотермическом типе температура тела ниже нормальных значений, что наблюдается у резко ослабленных больных с клинически выраженной недостаточностью крово-
121
Некоронарогенные болезни сердца
о бращения. Потоотделение не облегчает состояние больного, бывает профузным, иногда испариной покрываются только отдельные участки тела (голова, лоб, верхняя половина туловища).
Клинические симптомы обусловлены появлением вегетации, части которых могут отрываться и эмболизировать сердце, мозг, почки, селезенку, печень, сосуды конечностей и легких (при правостороннем эндокардите). Септическая эмболизация vasa vasorum или прямая бактериальная инвазия артериальной стенки может приводить к образованию аневризм, которые могутразрываться. Эти аневризмы наиболее часто развиваются в мозговых артериях, аорте, синусе Вальсальвы, коронарных и легочных артериях.
При развернутой клинической картине отмечаются следующие симптомы:
• выраженная интоксикация:
слабость,
анорексия,
головная боль,
миалгия,
артралгия,
похудание;
• изменения кожных покровов:
бледно-желтоватый цвет кожи, иногда с желтовато-коричне вым оттенком (цвет кофе с молоком) вследствие одновременно анемии и цианоза,
петехии (мелкоточечные геморрагии) на коже и слизистых оболоч ках, конъюнктиве нижнего века (симптом Лукина — Либмана),
пятна Джейнуэя — красно-фиолетовые до 5 мм в диаметре пят на на ладонях, ступнях, туловище,
узелки Ослера — болезненные, величиной с горошину, узелки красноватого цвета на ладонных поверхностях пальцев рук и подошвенных поверхностях пальцев ног; гистологически харак теризуются пролиферацией эндотелия артериол с периваску- лярной клеточной инфильтрацией;
• изменения концевых фаланг («барабанные палочки») и ногтей («часовые стекла»);
122
Некоронарогенные болезни сердца
поражение суставов — моно- или олигоартриты крупных суставов верхних и нижних конечностей;
поражение сердца:
• поражение аортального клапана:
систолический шум в точке Боткина вследствие появления полипозных вегетации на створках,
протодиастолический шум, лучше всего выслушивающий ся в точке Боткина при вертикальном положении или в по ложении лежа на левом боку;
• поражение митрального клапана:
систолический шум, в основном на верхушке сердца,
абсцессы в области клапанного кольца;
• поражение миокарда:
дистрофические изменения,
васкулит мелких разветвлений коронарных артерий со вто ричной воспалительной реакцией вокруг них,
инфаркт миокарда,
развитие очагового и диффузного миокардита;
• при вторичном эндокардите выявляют признаки вновь возник шего повреждения аортального или митрального клапана, фор мирование нового клапанного порока — появление новых шу мов, изменение выраженности и продолжительности ранее су ществовавших, меняющаяся сила тонов;
тромбоэмболический синдром: тромбоэмболии селезеночной, по чечных, легочной, коронарных, мозговых артерий с развитием ин фарктов соответствующих органов, сосудов сетчатки глаза;
поражение перикарда:
• признаки сухого перикардита:
- шум трения перикарда,
- постоянная боль в области сердца, усиливающаяся при дви жении,
• признаки экссудативного перикардита;
• поражение сосудов:
т
Некоронарогенные болезни сердца
микотические (инфекционные) аневризмы артерий,
генерализованный васкулит;
• поражение печени: гепатомегалия, обусловленная как наличием застоя, так и развитием гепатита;
•поражение селезенки: спленомегалия, обусловленная гиперплазией пульпы и фолликулов в ответ на наличие инфекции;
• увеличение лимфатических узлов;
•поражение почек (диффузные гломерулонефриты, очаговые нефриты, инфаркт почек):
боль в поясничной области справа или слева,
развитие нефрита часто приводит к снижению температуры тела с фебрильной до субфебрильной;
• поражение центральной нервной системы:
менингоэнцефалит,
субарахноидальное кровоизлияние,
тромбоэмболия сосудов мозга,
психоз;
• прогрессирующая сердечная недостаточность.
В последние годы повысилась частота развития инфекционного эндокардита у лиц пожилого и старческого возраста, который может быть первичным, но чаще развивается на фоне ревматического порока или атеросклеротического поражения сердца, в том числе и после перенесенного инфаркта миокарда. В связи с «постарением» заболевания у этого контингента больных отмечаются некоторые особенности клиники инфекционного эндокардита:
раннее развитие застойной сердечной недостаточности, что обу словлено предшествующим изменением клапанного аппарата и миокарда;
нередко безлихорадочное течение;
более частые неврологические осложнения (тромбоэмболия сосу дов головного мозга, разрыв микотических аневризм);
более частые нарушения ритма сердца и проводимости;
кардиотоксическое действие используемых антибиотиков и рези- стентность патогенных микроорганизмов ко многим из них.
124
Некоронарогенные болезни сердца
Изменения показателей лабораторных исследований при инфекционном эндокардите не являются специфичными, в периферической крови часто обнаруживаются признаки гипо- и нормохромной анемии. Прогрес-сирование анемии сопровождается анизоцитозом, пойкилоцитозом, ба-зофильной зернистостью эритроцитов, гипохромией, увеличением количества ретикулоцитов. В большинстве случаев отмечается лейкопения, но при осложнениях можно обнаружить лейкоцитоз со сдвигом лейкоцитарной формулы влево, моноцитоз. Для инфекционного эндокардита типичным является увеличение СОЭ, однако следует учитывать, что вследствие диспротеинемии этот симптом не может своевременно отражать положительную динамику при лечении заболевания. В периферической крови также обнаруживается тромбоцитопения, появляются гистиоциты. В костном мозге увеличивается число плазматических клеток.
При лабораторном исследовании мочи определяются следующие изменения:
микрогематурия,
преходящая макрогематурия,
протеинурия,
цилиндрурия (особенно зернистые цилиндры),
снижение показателей относительной плотности мочи в пробе Зимницкого,
снижение клубочковой фильтрации,
повышение уровня креатинина,
• повышение уровня азота мочевины сыворотки крови.
Биохимическими исследованиями выявляются следующие патологические изменения: диспротеинемия (повышение содержания у-гло-булинов и снижение уровня альбуминов), положительные осадочные пробы (формоловая, тимоловая), повышение уровня фибриногена и серомукоида, наличие С-реактивного протеина в крови.
Иммунологические исследования позволяют выявить следующие отклонения:
наличие ревматоидного и антиглобулинового факторов,
увеличение количества циркулирующих иммунных комплексов,
125
Некоронарогенные болезни сердца
поликлональная гипериммуноглобулинемия с повышением уров ня иммуноглобулинов классов М и G,
иммунокомплексные депозиты в почках, миокарде, сосудах, тром- ботических вегетациях миокарда,
снижение титра общей гемолитической активности комплемента,
образование противотканевых антител (антиэндокардиальные, ан- тисарколемные, антимиолемные, почечные, печеночные),
угнетение Т-системы лимфоцитов,
• повышение фагоцитарной активности лейкоцитов, •антитела к рибитолтейхоевой кислоте у больных эндокардитом,
вызванным золотистым стафилококком.
Для оценки тяжести инфекционного эндокардита А.А. Демин и Ал А. Демин (1975) предложили выделять три степени активности процесса. Основные критерии активности процесса, дополненные данными исследования гуморального иммунитета, представлены в табл. 10.
Течение. Для первичного инфекционного эндокардита, обусловленного высоко вирулентной микрофлорой — стафилококком, энтерококком и грамотрицательными бактериями, типично острое начало с высокой лихорадкой, ознобами, профузным потом, тяжелой общей интоксикацией. При вторичном эндокардите начало заболевания часто проявляется прогрессирующей сердечной недостаточностью на фоне ревматических пороков сердца.
Особенности течения инфекционного эндокардита обусловлены видом возбудителя. Для грибкового эндокардита характерны высокая степень активности процесса, образование гигантских вегетации и мико-тических аневризм, склонность к тромбоэмболическим осложнениям. Большие вегетации при грибковых эндокардитах могут закупоривать клапанное отверстие.
При заражении золотистым стафилококком происходит быстрая деструкция клапанов с возникновением регургитации крови. После эради-кации возбудителя происходит формирование рубца с последующим развитием стеноза клапанного кольца (отверстия). В случаях, когда инфекция распространяется на миокард, вызывая абсцесс, могут возникать
126
Некоронарогенные болезни сердца
Таблица 10. Клинические и лабор
Критерии |
Степень активности инфекционного эндокардита |
||
Температура тела |
Отсутствует |
II (умеренная) 37,5-38 °С |
III (высокая) |
Потливость тппмирование порока сердца Гломерулонефрит Миокардит Эмболии и инфаркты |
Отсутствует Медленное Очаговый Очаговый Отсутствуют |
Повышенная Медленное Очаговый Очаговый Могут быть |
Профузная Быстрое Диффузный Диффузный Часты |
грмоглобин, г/л |
120-150 |
120-110 |
110-90 |
СОЭ мм/ч |
10-20 |
20-40 |
Более 40 |
7_Глобулиновая фракция, % |
20-22 |
22—25 |
|
Фибриноген, мкмоль/л |
11,7-14,6 |
14,6-16,9 |
16,9-29,3 |
Иммуноглобулины, мкмоль/л А М G |
12,5-16,2 1,27-1,61 71,2-86,3 |
16,2-19,4 1,61-2,03 86,3-106,5 |
19,4-25,0 2,03-2,63 106,5-151,2 |
Циркулирующие иммунные комплексы, ед. опт. плотн. |
100-140 |
140-200 |
200-280 |
нарушения проводимости, фистулы (между камерами сердца и перикардом или большими сосудами) или разрыв хорд, папиллярных мышц.
Пневмококковый эндокардит наиболее часто выявляется у больных пожилого возраста с пневмонией или менингитом. Вегетации обычно локализуются на неизмененных клапанах, преимущественно аортальных. Эндокардит присоединяется либо на высоте пневмонии либо в период реконвалесценции. В клинике преобладают лихорадка, озноб и выраженная токсемия.
После протезирования клапана в большинстве случаев синтетические чужеродные ткани быстро прорастают фибротическими элементами из окружающих тканей, покрываются эндотелием и становятся недосягаемыми для циркулирующих в крови микроорганизмов. Однако в ряде случаев участки имплантированных тканей, особенно если они имеют сетчатое строение, являются очень уязвимыми для инвазии возбудителей инфекционного эндокардита.
Различают две формы инфекционного эндокардита протезированного клапана. Ранний эндокардит возникает в течение первых меся-
1 27
Некоронарогенные болезни сердца
цев (чаще в первые 5 нед) после операции и является следствием инфицирования больного во время хирургического вмешательства. Вызывается преимущественно экзогенными микроорганизмами, попавшими в организм из воздуха операционной, с кожи больного, из аппарата искусственного кровообращения и др., в первую очередь эпидер-мальным стафилококком, грамотрицательными микробами, грибами. У больных с биологическими протезами клапанов инфекция локализуется на створках клапанов, с механическими — в окружающих протез тканях. Морфологическим субстратом патологического процесса являются тромботические массы и парапротезные фистулы, которые приводят одновременно и к дисфункции протеза.
Поздний инфекционный эндокардит протезированного клапана развивается через 2- 6 мес и более после операции. Среди возбудителей преобладает стрептококк, что сближает его с другими вариантами под-острого инфекционного эндокардита.
Септический процесс с инфицированием биопротезов протекает обычно более благоприятно, чем при наличии механического клапана, чаще удается добиться стойкой нормализации температуры тела и стерилизации крови, тромбоэмболические осложнения не возникают. При инфицировании механического протеза у всех больных отмечается высокая температура тела с ознобами, тромбоэмболии артерий, дисфункция протеза клапана.
При инфекционном поражении протезированных клапанов нередко поражается клапанное кольцо, что приводит к разрывам клапана или пенетрации инфекции в миокард и окружающие ткани. Следствием этого может быть развитие абсцесса миокарда, нарушение проводимости, появление аневризмы синуса Вальсальвы или фистулы в правые отделы сердца или в перикард. Распространение инфекции из области митрального кольца может сопровождаться появлением непароксизмальной функциональной тахикардии, AV-блокады II- III степени с узкими комплексами QRS. Отрыв протеза с возникающей регургитацией наблюдается у 80% больных с протезом аортального клапана и у 30% — с протезом митрального клапана. Инфицирование протезированного клапана, осложнившееся его стенозом, разрывом, сочетающееся с застойной сер-
Некоронарогенные болезни сердца
дечной недостаточностью, повторными эмболиями, резистентностью к антибактериальной терапии, признаками вовлечения миокарда, требует неотложного хирургического вмешательства.
Диагноз. В типичных случаях диагностика инфекционного эндокардита несложна и основывается на следующих признаках: лихорадка с ознобами, наличие клапанных дефектов с появлением шумов сердца при первичном эндокардите или выраженном изменении их характера при вторичном, тромбоэмболические осложнения и положительные результаты бактериологического исследования. Спленомегалия, характерная форма пальцев и ногтей, мочевой синдром, нарастание анемии, изменения белковых фракций крови, увеличение СОЭ помогают поставить правильный диагноз. Значительные трудности представляет диагностика заболевания при стертом или атипичном течении.
Электрокардиограмма отражает изменения электрической позиции сердца в соответствии с имеющимся или формирующимся пороком сердца: гипертрофия левого желудочка (при поражении аортального или митрального клапана) или правого желудочка (при вовлечении в процесс трехстворчатого клапана или клапана легочной артерии). На ЭКГ выявляются диффузные изменения миокарда, возможны нарушения AV-npo-водимости, предсердная и желудочковая экстрасистолия. В 25% случаев обнаруживают мерцание илитрепетание предсердий, реже — очаговые изменения миокарда. AV-блокада указывает на возможность существования абсцесса клапанного кольца вблизи проводящей системы.
Эхокардиографию рекомендуется проводить всем больным с подозрением на инфекционный эндокардит, поскольку это исследование позволяет верифицировать диагноз: своевременно выявить вегетации клапанов, кальциноз, разрыв хорд или створки клапана, абсцесс клапанного кольца и миокардиальный абсцесс, уточнить характер порока сердца, а также определять необходимость срочного оперативного лечения больных с остро развившейся недостаточностью клапана аорты и выраженной перегрузкой левого желудочка объемом.
При одномерном исследовании признаками вегетации являются неравномерное утолщение одной из створок клапана, густо располо-
129
1-136
131
Некоронарогенные
болезни сердца
женные «лохматые» мелковолновые ее осцилляции, подвижность створки при этом не ограничивается (рис. 9). Метод позволяет визуализировать вегетации размером 2- 3 мм.
При двухмерной эхокардиографии вегетации определяются в виде дополнительных эхотеней, тесно связанных со створками и выходящих за обычные границы их локации (рис. 10). Частота выявления вегетации при эхокардиографическом исследовании зависит от их величины, структуры, локализации, предшествующего клапанного порока, продолжительности заболевания. Выделяют три типа вегетации: «сидячие», «на ножке», «нитчатые».
Эхокардиография позволяет в значительной степени объективно оценить состояние клапанного аппарата сердца. Отрыв створки аортального клапана проявляется хаотическими колебаниями створки с регистрацией эхосигналов от нее в полости левого желудочка во время диастолы и в просвете аорты во время систолы. Отрыв хорд от передней створки митрального клапана проявляется крупноволновым хаотическим трепетанием створки во время диастолы с деформацией диа-столического наклона. Отрыв хорд от задней створки характеризуется появлением грубого беспорядочного и высокоамплитудного трепетания створки во время диастолы, увеличением амплитуды движения межжелудочковой перегородки и стенки левого предсердия, появлением эхосигналов от створок в полости левого предсердия.
С помощью допплер-эхокардиографии определяется регургитация на аортальном и митральном клапанах в соответствующую фазу сердечного цикла.
Тяжесть течения инфекционного эндокардита на основании данных эхокардиографического исследования оценивается степенью разрушения створок, их деформацией, образованием абсцессов створок, основания аорты, разрывом хорд митрального клапана, отрывом аортальной створки, результатом чего является нарастание недостаточности клапанов с перегрузкой соответствующих камер сердца. Сохранение или исчезновение вегетации на фоне лечения (по данным эхокардиографии) не является надежным критерием успеха или неудачи антибиотикотерапии.
1зо
Рис. 9. ЭхоКГ аортального клапана у пациента с инфекционным эндокардитом
и вегетациями (вег) на аортальном клапане (М-режим)
(по Н. Feigenbaum, 1987, с изменениями)
Рис.10. Вегетация на передней створке митрального клапана (В-режим), парастернальная позиция по длинной оси
Некоронарогенные болезни сердца
Следует отметить, что хотя нормальные показатели эхо кардиограммы не исключают наличие инфекционного эндокардита, однако данные, которые указывают на имеющуюся патологию, редко бывают ложно-позитивными. Причиной гиподиагностики могут явиться вегетации менее 2 мм в диаметре, локализующиеся на глубине более 7 мм отдатчика, а также проведение эхокардиографического исследования в первые дни заболевания. Вегетации обычно выявляются через 2 нед от начала инфекционного эндокардита при острой (стафилококковой) форме и через 6-8 нед при подострой. Проведение эхокардиографии должно быть полипозиционным с использованием максимального количества точек обзора. Чреспищеводная эхокардиография имеет значительно более высокую чувствительность в отношении выявления внутрисердечных вегетации (95-100% против 60- 65% при трансторакальной эхокардиографии).
Катетеризация сердца позволяет выявить пороки клапанов, врожденные дефекты, поражения коронарных артерий, оценить степень выраженности гемодинамических нарушений у больных с инфекционным эндокардитом. В ряде случаев проводить это исследование опасно, учитывая риск отрыва вегетации от клапана с последующей эмболией сосудов большого круга кровообращения.
Посевы крови на стерильность ~ один из основных методов верификации диагноза инфекционного эндокардита. Успешное выделение микроорганизмов из крови зависит от соблюдения ряда условий. Посевы производят при подозрении на инфекционный эндокардит до назначения антибиотиков, рекомендуемое число посевов не менее 6. Следует иметь в виду, что положительная гемокультура при однократном определении возбудителя, особенно стафилококка, может быть обусловлена случайным попаданием бактерий в среду при взятии крови. Важно получить положительные результаты при двух или трех посевах. Обязательным условием считается взятие крови на стерильность во время озноба или максимального повышения температуры тела.
Предварительное применение антибиотиков значительно снижает эффективность бактериологической диагностики. Бактериемия может исчезать на несколько дней после единственной инъекции пенициллина. Перед
Т 32
Некоронарогенные болезни сердца
посевом крови антибиотики следует отменить, через 5- 7 дней повторяют посевы крови на стерильность и возобновляют антибактериальную терапию. На высеваемость оказывает влияние количество микроорганизмов в крови: если их от 5 до 30 в 1 мл, то роста бактерий получить обычно не удается. Если посевы крови взяты у пациента, не получавшего лечение в предшествующие 2 нед, то возбудитель устанавливается в 96% случаев. Большие перспективы в идентификации возбудителя инфекционного эндокардита открывает бактериологическое исследование артериальной крови, частота выявления положительной гемокультуры при этом возрастает.
Разработаны диагностические критерии инфекционного эндокардита, среди которых выделяют достоверные, вероятные и исключающие эндокардит.
1. Диагноз достоверного инфекционного эндокардита устанавлива ют, учитывая:
а) морфологические критерии: возбудитель выявлен методом посева
или при гистологическом исследовании вегетации или их фрагментов, формирующих эмболы,
или в зоне внутрисердечного абсцесса;
б) клинические критерии (см. ниже): 2 основных критерия
или один основной и 3 вспомогательных критерия, или 5 вспомогательных критериев.
Диагноз инфекционного эндокардита вероятен при наличии при знаков заболевания, не позволяющих отнести его ни к достоверному эндокардиту, ни исключить его
Диагноз инфекционного эндокардита исключается:
а) при наличии убедительного альтернативного диагноза, объясняющего имеющиеся признаки, характерные для инфекционного эндокардита,
б) при исчезновении синдрома, напоминающего эндокардит, пос ле 4 (или менее) дней антибиотикотерапии,
в) при отсутствии морфологических признаков инфекционного эндокардита во время операции или при аутопсии, если антибактери альную терапию проводили не более 4 дней.
Ш
Некоронарогенные болезни сердца
Основные диагностические критерии
1. Положительные результаты посевов крови:
а) обнаружение типичного возбудителя инфекционного эндокар дита в двух разных культурах крови,
б) стойко положительный рост микроорганизмов:
•в посевах крови с интервалом более 12 ч, •в 3 или более из 4 и более отдельных посевов, если интервал между первым и последним забором крови не менее 1 ч.
2. Признаки поражения эндокарда:
а) эхокардиографические:
осциллирующие внутрисердечные образования на клапанах или подклапанных структурах, на пути регургитационного потока или на имплантированных тканях без альтернативного анато мического объяснения,
наличие абсцесса клапанного кольца,
впервые возникшее повреждение клапанного протеза;
б) впервые возникшая недостаточность клапана (усиление или из менение имевшихся шумов не является достоверным признаком).
Вспомогательные диагностические критерии
Наличие предрасполагающего заболевания сердца или регуляр ное внутривенное введение наркотиков (у наркоманов).
Лихорадка > 38 °С.
Сосудистые осложнения: эмболия крупных артерий, септический инфаркт легких, микотическая аневризма, внутричерепное и конъюн- ктивальное кровоизлияние, пятна Джейнуэя.
Иммунологические нарушения: гломерулонефрит, узелки Осле- ра, пятна Рота, появление ревматоидного фактора в крови.
Микробиологические исследования: положительный бактериаль ный посев крови, не отвечающий основным критериям, или серологи ческие признаки активной инфекции, вызванной потенциальным воз будителем инфекционного эндокардита.
Эхокардиографические изменения, характерные для инфекцион ного эндокардита, но не отвечающие основным критериям.
Ш
Некоронарогенные болезни сердца
К сожалению, средний срок установления диагноза инфекционного эндокардита от первых жалоб и обращений к врачу составляет не менее 2- 3 мес, а при поражении правых отделов сердца и того более, до 87% больных поступают в стационар с неправильным диагнозом. Причины поздней или неправильной диагностики инфекционного эндокардита можно условно разделить на субъективные и объективные. Первые заключаются прежде всего в сложившемся у многих практических врачей представлении об инфекционном эндокардите как о редком заболевании с типичной клиникой затяжного септического эндокардита, развившегося на фоне приобретенного порока сердца, в недостаточной информированности практических врачей о клинической симптоматике, течении инфекционного эндокардита на разных стадиях болезни, которое существенно изменилось за последние десятилетия. В настоящее время соотношение между первичным и вторичным эндокардитом, связанным с пороками клапана ревматической и другой этиологии, существенно изменилось в пользу первого, частота которого составляет более 30%.
Как правило, у больных инфекционным эндокардитом имеются очаги хронической инфекции, что позволяет врачам объяснить появление лихорадки и симптомов общей интоксикации.
Объективные причины поздней диагностики обусловлены деформацией клапанов, которая ведет к возникновению большого градиента давления, узости отверстия и изменению скорости кровотока, тем самым создавая условия, способствующие внедрению инфекционных агентов в эндокард с образованием инфекционного очага. При этом происходит повреждение эндокарда, которое заключается в изменении реактивности эндотелия, его дегенерации и десквамации и образовании вегетации на клапанах и эндокарде, способствующих инокуляции инфекционных агентов. Такое повреждение обычно не диагностируется.
Весьма трудной бывает диагностика инфекционного эндокардита, когда преобладают системные поражения внутренних органов и лихо-радка, как правило, отсутствует. На этом этапе диагностические ошибки часто возникают, если в клинической картине инфекционного эндокардита преобладают симптомы поражения какого-либо одного органа или
Некоронарогенные болезни сердца
возникает синдром, который маскирует течение основного заболевания и расценивается как самостоятельное заболевание без учета связи его с другими менее выраженными синдромами. К таким ошибкам может приводить, например, начальная манифестация в виде инсульта, застойной сердечной недостаточности, инфаркта миокарда, экссудативного перикардита, диффузного гломерулонефритаили гипертензивного криза. Первыми признаками могут быть тромбоэмболические или геморрагические осложнения, желтуха, множественные легочные абсцессы. Очевидно, что для установления правильного диагноза необходим учет всего комплекса проявлений патологического процесса. Возможные «маски» инфекционного эндокардита
Общие: недомогание, анорексия, уменьшение массы тела, блед ность кожных покровов, ночная потливость.
Со стороны сердца: миокардит, перикардит, поражение клапанов, инфаркт (шумы, нарушения ритма сердца, сердечная недостаточность).
Со стороны легких — чаще наблюдаются при поражении клапанов правых отделов сердца и обусловлены развитием повторных инфаркт- пневмоний, инфаркта легкого (плеврит, кровохарканье, отек легких)
Со стороны органа зрения: внезапная слепота, петехии на веках, на глазном дне — петехиальные кровоизлияния и пятна Рота (белые округ лые пятна диаметром 1-2 мм, расположенные поверхностно, иногда за крывающие сосуды сетчатки, состоящие из скоплений клеток, образовав шихся вследствие инфарктов сетчатки), отек и неврит зрительного нерва.
Церебральные— протекающие под видом острого нарушения моз гового кровообращения, реже — менингита или менингоэнцефалита (ге- миплегия, афазия, атаксия, головная боль, психические нарушения).
Почечные— проявляющиеся симптомами диффузного гломеру- лонефрита или инфаркта почки (протеинурия, гематурия, гипертен- зивныйкриз).
Гематологические— проявляющиеся анемией.
Со стороны опорно-двигательного аппарата: артрит, остеомиелит.
Сосудистые— воспроизводящие клинику системного васкулита,тром-
бангиита (геморрагический синдром, тромбоэмболические осложнения).
Некоронарогенные болезни сердца
Большие трудности возникают при диагностике инфекционного эндокардита протезированных клапанов, несмотря на то, что внимание врачей привлечено к факту имплантации искусственного клапана. Отсутствие гемодинамических нарушений или признаков дисфункции протеза даже при транзиторной бактериемии не позволяет считать диагноз верифицированным. Диагностическое значение придают изменениям аускультативной картины со стороны сердца, при развитии па-рапротезной фистулы в аортальной позиции выявляют диастоличес-кий шум, нередко быстро прогрессирует сердечная недостаточность (тромбоз механического протеза). Эхокардиография в диагностике инфекционного эндокардита протезированных клапанов (особенно шарикового протеза) мало информативна, лишь в отдельных случаях позволяет обнаружить тромбоз механического протеза и вегетации.
Диагностика инфекционного эндокардита у больных пожилого возраста особенно затруднительна, причем число диагностических ошибок достигает 50%.
Предложены диагностические критерии инфекционного эндокардита у пациентов пожилого и старческого возраста (Gantz N., 1991):
лихорадка с необъяснимой сердечной недостаточностью,
лихорадка с цереброваскулярными расстройствами,
лихорадка с необъяснимой почечной недостаточностью,
лихорадка и боль в области спины,
анемия неясного происхождения и уменьшение массы тела,
вновь появившийся шум над областью сердца,
внутрибольничная инфекция с лихорадкой у больных с внутри венными катетерами.
Дифференциальный диагноз. Не существует четко очерченной границы между фазами инфекционного эндокардита, но при каждой из них болезнь характеризуется такими особенностями, которые требуют проведения дифференциальной диагностики с другими заболеваниями.
В начальный период важно дифференцировать инфекционный эндокардит и острые инфекции: сальмонеллез, лептоспироз, псевдотуберкулез. Высокая лихорадка, слабость, головная боль, кашель, тен-
137
Некоронарогенные болезни сердца
денция к лейкопении дают основания для установления диагноза «грипп». В случаях лихорадки с увеличением селезенки, диареей следует думать о брюшном тифе или малярии. Трудно проводить дифференциальную диагностику с висцеральным сифилисом, так как обоим заболеваниям свойственны появление шумов над аортальным клапаном, субфебрилитет, артралгия. Диагностическое значение имеют данные анамнеза и результаты реакции иммобилизации бледной трепоне-мы. Иногда окончательный диагноз может быть поставлен в результате проведения пробной антибактериальной терапии. Считается, что если в течение 7-10 дней причина лихорадки неясна, то при выявлении шума в области сердца следует думать о бактериальном эндокардите и начинать лечение антибиотиками.
При проведении дифференциальной диагностики с ревматизмом следует иметь в виду, что удлинение интервала P-Q на ЭКГ, ранее считавшееся характерным признаком ревмокардита, нередко встречается и при инфекционном эндокардите. Показатели титров антистрептолизинаи анти-стрептогиалуронидазы бывают повышены при обоих заболеваниях, но в отличие от ревматизма при инфекционном эндокардите обычно не бывает повышения обоих титров одновременно, а лишь одного из них.
Первыми признаками инфекционного эндокардита может быть эмболия сосудов головного мозга, при этом у больных пожилого возраста ее могут принимать за нарушение мозгового кровообращения на почве атеросклероза сосудов головного мозга. Дифференциальную диагностику у больных пожилого и старческого возраста необходимо проводить с атеросклеротическим поражением сердца и крупных сосудов, а также со злокачественными новообразованиями, в том числе раком паренхимы почек, при котором нередко наблюдаются неспецифические синдромы с инфекцией мочевых путей
При стертой клинической картине первичного инфекционного эндокардита может возникнуть необходимость в проведении дифференциальной диагностики с тиреотоксикозом. Установлению последнего помогают результаты исследования функции щитовидной железы с помощью радионуклидных методов.
т
Некоронарогенные болезни сердца
Прогноз. Без лечения инфекционный эндокардит практически всегда приводит к летальному исходу, при медикаментозном лечении летальность достигает 80%, при хирургическом — 30%, что объясняется прежде всего несвоевременностью установления диагноза.
Для прогноза исхода заболевания важное значение имеют возбудитель, его вирулентность и устойчивость к антибактериальным средствам, а также локализация клапанного поражения. Возобновление болезни в течение первых 12 мес после выписки из стационара расценивается как рецидив, возобновление болезни позже чем через 1 год — как повторное возникновение инфекционного эндокардита.
Факторами, ухудшающими прогноз болезни, являются наличие застойной сердечной недостаточности, пожилой возраст, вовлечение в процесс клапана аорты или нескольких клапанов сердца, полимикробная бактериемия, невозможность идентификации этиологического агента вследствие отрицательных результатов посевов крови, резистент-ность возбудителя к бактерицидным препаратам первого ряда, позднее начало терапии. Особенно неблагоприятный прогноз отмечается при наличии протезированных клапанов, развитии абсцессов клапанного кольца или миокарда, обнаружении грамотрицательных микроорганизмов. При наличии грибкового эндокардита вследствие сложности выделения возбудителя из гемокультуры, малоэффективное™ лечения, генерализации процесса по сосудистой системе за счет частых эмболии умирают 80-90% больных.
Наиболее частой причиной смерти даже в случаях адекватного лечения является сердечная недостаточность, развившаяся вследствие деструкции клапана или повреждения миокарда. Кроме того, к летальному исходу могут привести эмболия сосудов жизненно важных органов, развитие почечной недостаточности или микотической аневризмы, осложнений после хирургических вмешательств.
Лечение инфекционного эндокардита базируется на нескольких принципах:
1 - Терапия должна быть по возможности этиотропной, то есть направленной на эрадикацию конкретного возбудителя.
139
Некоронарогенные болезни сердца
Терапия должна быть продолжительной: при заболевании стрептокок ковой этиологии — не менее 4 нед, стафилококковой — 6 нед, при заболева нии, вызванном грамотрицательными возбудителями, — не менее 8 нед.
При нарастании признаков иммунного конфликта в форме гло- мерулонефрита, васкулита, миокардита и др., а также проявлений ин- фекционно-токсического шока рассматривается вопрос о назначении глюкокортикоидов.
При острых формах инфекционного эндокардита, вызванного пре имущественно стафилококками и грамотрицательными микроорганиз мами, целесообразно проведение иммунотерапии (антистафилококко вая плазма, антистафилококковый у-глобулин) и дезинтоксикации.
Хирургическое лечение должно проводиться по строгим показа ниям и своевременно.
Основными принципами антибиотикотерапии инфекционного эндокардита является выбор бактерицидных антибиотиков и длительное лечение для обеспечения полной эрадикации возбудителя в клапанах сердца и вегетациях. При выборе антибиотика следует учитывать результаты микробиологического исследования, чувствительность выделенного возбудителя к антибиотикам.
Трудности лечения прежде всего обусловлены широким распространением нетипичных возбудителей заболевания с высокой резис-тентностью многих микроорганизмов к существующим антибиотикам. Немаловажное значение имеет и тот факт, что антибиотики плохо проникают в клапаны сердца и миокард и во многих случаях (например, при наличии искусственных клапанов сердца, шунтов, кардиостимуляторов) течение эндокардита не всегда прогнозируемо. Наконец, одна из главных трудностей обусловлена тем, что даже в оптимальных условиях далеко не всегда удается идентифицировать возбудитель. Между тем при выявлении инфекционного эндокардита антибактериальное лечение необходимо начинать как можно раньше, не дожидаясь идентификации возбудителя, поскольку процесс быстро диссеминирует. В случаях с неустановленным возбудителем инфекционного эндокардита рекомендуют начинать терапию З-лактамными антибиотиками и
140
Некоронарогенные болезни сердца
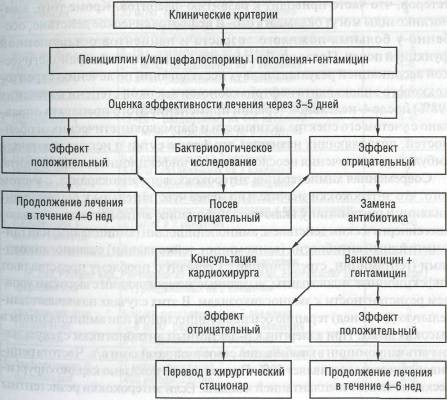
аминогликозидами (схема 2). Отсутствие эффекта через 3- 5 дней и отрицательные результаты бактериологического исследования позволяют предположить наличие стафилококкового эндокардита, который вероятнее всего обусловлен пенициллино- и метициллинорезистент-ными стафилококками, что требует замены антибиотика.
Наиболее эффективными считаются бензил пенициллин, цефалоспо-рины и аминогликозиды. Антибиотиком выбора для начальной терапии, как правило, является бензил пенициллин в суточной дозе 12 000 000-
Схена 2. Алгоритм эмпирического лечения инфекционного эндокардита (Белоусов Ю.Б., 1998)
Некоронарогенные болезни сердца
20 000 000 ЕД. Назначение этого антибиотика в такой дозе объясняется его доступностью, высоко выраженным бактерицидным действием на многие микроорганизмы и широким терапевтическим диапазоном.
Современная этиотропная химиотерапия инфекционного эндокардита у больных с нормальной функцией почек представлена в табл. 11
Наиболее частым возбудителем инфекционного эндокардита является стрептококк. Для лечения назначают бензилпенициллин в течение 4 нед или бензилпенициллин в комбинации с аминогликозидом (гентамицин, тобрамицин в течение 2 нед). Эти режимы требуют длительной госпитализации больных и использования внутривенных катетеров, что часто приводит к развитию флебитов. Кроме того, ами-ногликозиды могут оказывать ото- и нефротоксическое действие, особенно у больных пожилого возраста и пациентов с нарушенной функцией почек. После опубликования Американской кардиологической ассоциацией результатов двух исследований по лечению стрептококкового эндокардита цефтриаксоном и высокой степени излечения (98%) после 4-недельной терапии применение этого препарата оправдано с учетом его спектра активности и фармакокинетических особенностей, позволяющих назначать его 1 раз в сутки и использовать для амбулаторного лечения неосложненного инфекционного эндокардита.
Современная химиотерапия энтерококкового эндокардита, с учетом того, что энтерококки значительно менее чувствительны к бензилпени-циллину и гентамицину, включает комбинацию антибиотиков, обладающих синергическим действием: аминопенициллин (ампициллин) или гли-копептидный антибиотик (ванкомицин, тейкопланин) с аминогликози-дами (гентамицин, стрептомицин). Серьезную проблему представляют инфекционные эндокардиты, вызванные энтерококками с высоким уровнем резистентности к аминогликозидам. В этих случаях назначают длительную (8-12 нед) терапию бензилпенициллином или ампициллином в высоких дозах. При аллергии к бета-лактамным антибиотикам следует назначать ванкомицин в комбинации с аминогликозидами в/в. Частота рецидивов при этом составляет 50%. При рецидиве показано кардиохирурги-ческое лечение с имплантацией клапана. Если энтерококки резистентны
Некоронарогенные болезни сердца
Таблица 11. Этиотропная химиотерапия инфекционного эндокардита
Антибиотик |
Суточная доза препарата (предпочтительно вводить в/в) |
Длительность терапии (недели) |
Стрептококки [S. bovis, s. pneumonie, s. pyogenes и др.) |
|
|
1. Бензилпенициллин или цефтриаксон или ампициллин |
12 000 000-20 000000 ЕД в 6 введении 2 г однократно 4-8 г, разделенных на 6 введений |
4 4 4 |
2.Бензилпенициллинили цефтриаксон или ампициллин + гентамицин или тобрамицин или нетилмицин |
10 000 000-20 000 000 ЕД в 6 введений 2 г в однократно 4-8 г, разделенных на 6 введений 3 мг/кг, разделенных на 3 введения 3 мг/кг, разделенных на 3 введения 4 мг/кг однократно |
4 4 4 2 2 2 |
3 Цефазолин |
4-8 г, разделенных на 3 введения |
4 |
4 Ванкомицин |
30 мг/кг, разделенных на 2 введения |
4 |
Энтерококки (Е faecalis, Е. faecium) |
||
1. Бензилпенициллин или ампициллин + гентамицин |
20 000 000-30 000 000 ЕД, разделенных на 6 введений 8-16 г, разделенных на 4 введения 3-5 мг/кг, разделенных на 3 введения |
4-6 4-6 4-6 |
2.Ванкомицин + гентамицин |
30 мг/кг, разделенных на 2 введения 3-5 мг/кг, разделенных на 3 введения |
4-6 4-6 |
|
Стафилококки {S. aureus, S. epidermidis) |
|
1. Оксациллин + гентамицин или амикацин |
12-20 г, разделенных на 4-6 введений 3-5 мг/кг, разделенных на 3 введения 1-1,5 г, разделенных на 3 введения |
4-6 2 2 |
2. Цефазолин + гентамицин |
6 г, разделенных на 3 введения 3 мг/кг, разделенных на 3 введения |
4-6 2 |
3. Цефотаксим + амикацин |
6-8 г, разделенных на 3-4 введения 1-1,5 г, разделенных на 3 введения |
6 2 |
При неэффективности или аллергии к пенициллинам |
|
|
1. Ванкомицин + аминогликозид и/или рифампицин |
30 мг/кг в 2 введения 1 г однократно |
4-6 4-6 |
|
Грамотрицательные бактерии |
|
(Е. coli, Proteus spp., |
Pseudomonas spp., Klebsiella spp., Enterobacter spp. |
Serratia spp) |
1- Цефепим или цефтазидим + гентамицин или тобрамицин |
4 г, разделенных на 2 введения 5 мг/кг, разделенных на 3 введения 5-8 мг/кг, разделенных на 3 введения |
4 2 2 |
2. Имипенем |
2 г, разделенных на 4 введения |
4 |
|
Грибы Candida spp., Aspergillus spp. |
|
1-Амфотерицин В + флуконазол |
1 мг/кг однократно 400 мг однократно |
4-6 4-6 |
Некоронарогенные болезни сердца
к пенициллину и ванкомицину, эффективной терапии нет. Цефалоспо-рины не следует использовать для лечения энтерококковых эндокардитов из-за первичной резистентности к ним этих микроорганизмов.
Золотистый стафилококк является вторым по частоте возбудителем инфекционного эндокардита у пациентов с неизмененными клапанами сердца. В многочисленных исследованиях доказано, что при стафилококковом эндокардите бактерицидный эффект, стерилизация клапанов и профилактика их тяжелых повреждений наступает быстрее при использовании комбинации пенициллинов или цефалоспоринов, устойчивых к действию β-лaктaмaз, и аминогликозидов. При неэффективности терапии, выделении пенициллине- и метициллинорезистент-ных штаммов золотистого или эпидермального стафилококка или аллергии к β-лaктaмным антибиотикам применяются гликопептиды (ван-комицин) в сочетании с аминогликозидами. В случаях аллергии к β-лaктaмным антибиотикам при стафилококковом эндокардите применяют также линкозамиды (линкомицин, клиндамицин). Высокой противостафилококковой активностью отличается цефепим.
Эндокардиты, вызванные грамотрицательными микроорганизмами, почти всегда возникают в результате внутригоспитального инфицирования, и лечить их сложно из-за наличия у возбудителей различных механизмов резистентности. Современная антибиотикотерапия предполагает назначение аминогликозидов II- III поколения (тобрамицин, нетилмицин, амикацин) в сочетании с цефалоспоринами III- IV поколения (цефтриаксон, цефепим) или карбапенемов (имипенем, меро-пенем) в течение 4- 6 нед.
При грибковых эндокардитах проводят комбинированную химиотерапию амфотерицином В и флуконазолом в сочетании с хирургическим лечением. Даже при оптимальном лечении наблюдается высокая смертность и поздние рецидивы заболевания (через 2 года и более).
У больных с искусственным клапаном сердца в 50% случаев раннего эндокардита высевается золотистый и эпидермальный стафилококк, в 21 % — грамотрицательная микрофлора, в 10% — грибы. Для лечения можно использовать комбинацию цефалоспоринов с гентамицином или тобра-
744
Некоронарогенные болезни сердца
мидином, эффективен ванкомицин. Возбудителями позднего эндокардита протезированного клапана являются эпидермальный стафилококк и стрептококк (50%), золотистый стафилококк (16%), энтерококк (11%), грамотрицательная микрофлора (12%). При заболевании, вызванным эпи-дермальным стафилококком, чаще применяют ванкомицин с рифампи-цином и гентамицин. Монотерапия рифампицином нецелесобразна.
При длительном проведении антибактериальной терапии в/в рекомендуют добавлять гепарин из расчета 1 ЕД/мл раствора антибиотика для предотвращения образования тромбов и 1 раз в неделю вводить ам-фотерицин В (50 000 ЕД в/в капельно) для предупреждения грибковой инфекции. Противогрибковые препараты целесообразно применять не с первых дней лечения, а приблизительно с середины курса антибио-тикотерапии, когда можно ожидать развития грибковой инфекции. Для диагностики последней и оценки эффективности терапии необходимо проводить посевы соскобов с корня языка и посевы мочи для выявления грибковой флоры.
Антибактериальная терапия инфекционного эндокардита должна проводиться под тщательным клиническим и микробиологическим контролем.
Дискуссионным остается вопрос об использовании глюкокортико-стероидов, многие исследователи обращались к этой проблеме, но она до сих пор не решена. С первых лет применения глюкокортикостерои-дов при инфекционном эндокардите в начале 50-х годов XX века были получены противоречивые данные об их эффективности. Наряду с благоприятными результатами сообщалось о случаях обострения токси-коинфекционного процесса под влиянием гормональной терапии вплоть до летального исхода. В настоящее время можно утверждать, что применение глюкокортикостероидов не предотвращает разрушения клапанного аппарата. Подавляя воспалительную реакцию вокруг очага инфекции, они, наоборот, способствуют более быстрому разрушению клапана. Гормональная терапия ведет к угнетению клеточного и гуморального иммунитета, необходимого для борьбы с инфекцией, вызывает снижение фагоцитарной активности лейкоцитов и уровня об-
145
Некоронарогенные болезни сердца
разования антител, которые могут способствовать генерализации септического процесса. Наблюдающееся в начале применения гормонов субъективное улучшение самочувствия со снижением температуры тела или ее нормализацией, повышением уровня гемоглобина крови обманчиво, поскольку септический процесс продолжается в стертом, завуалированном виде. Назначение глюкокортикостероидов нежелательно до достижения надежного подавления возбудителя антибиотиками (нормализации температуры тела, тенденции к уменьшению СОЭ). Глюкокортикостероиды опасно применять в случаях заболевания с отрицательной гемокультурой, когда врачи вынуждены проводить эмпирическую антибактериальную терапию, а гормоны, устраняя лихорадку, анемию и замедляя СОЭ, лишают их критериев оценки эффективности этой терапии. Недопустимо применение глюкокортикостероидов при рецидивах заболевания, особенно ранних (в течение первых 2-3 мес), когда нет возможности провести полную эрадикацию возбудителя. В случаях заболевания с установленным возбудителем и известной его чувствительностью к антибиотикам в назначении гормонов, как правило, нет необходимости.
Таким образом, глюкокортикостероиды не являются препаратами первого ряда, они противопоказаны при остром септическом эндокардите, наличии септического синдрома при подостром септическом эндокардите, неустановленном возбудителе, отсутствии эрадикации возбудителя, при рецидивирующем инфекционном эндокардите. Неблагоприятное влияние глюкокортикостероидов на течение инфекционного эндокардита, особенно в дозах 30 мг/сут и более, делают их применение нежелательным.
Показанием к назначению кортикостероидов является инфекцион-но-токсический шок, при котором кратковременное применение кортикостероидов в высоких дозах (100- 200 мг и более в пересчете на преднизолон) жизненно необходимо. Несомненным показанием к их назначению является медикаментозная аллергия. Относительным показанием к их назначению является тяжелое иммуновоспалительное поражение почек (протеинурия более 1 г/л) и миокарда.
~146
Некоронарогенные болезни сердца
Следует указать, что появление AV-блокады I- III степени может свидетельствовать не о тяжести миокардита и показании к назначению гормонов, а о развитии абсцессов клапанного кольца, преимущественно аортального.
При инфекционном эндокардите, особенно остром, проводят иммунотерапию — вводят готовые антитоксические сыворотки (пассивная иммунизация) с целью нейтрализации циркулирующих в крови микробных токсинов. Наиболее эффективным препаратом для пассивной иммунизации является гипериммунная плазма (в зависимости от вида возбудителя — антистафилококковая, антисинегнойная и т. д.). Антистафилококковую плазму вводят в/в капельно по 125- 250 мл ежедневно или через день (4- 6 вливаний на курс). Антисинегнойную плазму вводят в/в из расчета 4-6 мл/кг (в среднем 250 мл) с интервалами между вливаниями 1 - 3 дня (на курс 4- 6 вливаний). Антистафилококковый у-глобулин не только является источником антител, но стимулирует также факторы неспецифического иммунитета, применяется в виде в/м инъекций по 5-10 мл ежедневно в течение 10 дней. Иммуноглобулин человека вводят в/в по 50 мл со скоростью 20- 40 капель в 1 мин ежедневно в течение 3- 5 дней.
В комплексном лечении инфекционного эндокардита могут применяться препараты системной энзимотерапии (Воробьева A.M., 2000).
Современная терапия инфекционного эндокардита немыслима без своевременного оперативного лечения. Оно проводится как в ранние сроки заболевания при сохраняющихся лихорадке и бактериемии, так и по завершении как минимум 4- 6-недельного курса антибактериальной терапии. В хирургическом лечении нуждаются около 20% больных инфекционным эндокардитом.
Показаниями к оперативному вмешательству являются:
1. Наличие гемодинамически значимого порока сердца с прогрессирующей сердечной недостаточностью:
приступы сердечной астмы,
остро возникшая недостаточность аортального клапана со снижением Диастолического артериального давлениядо уровня 40 мм рт. ст. иниже,
147
Некоронарогенные болезни сердца
острая деструкция клапанов сердца,
тромбоэмболии артерий.
Неэффективность медикаментозной этиотропной терапии — если через 15 дней лечения сохраняется бактериемия и из крови продолжа ют выделять возбудитель.
Абсцессы миокарда и фиброзного кольца.
Наличие больших подвижных вегетации на клапанах (грибковый эндокардит).
Инфекционный эндокардит клапанного протеза.
Хирургический метод заключается в удалении пораженного клапана и имплантации вместо него искусственного механического или биологического протеза. Имеются сообщения о новых подходах: иссечении вегетации, ушивании перфорации створки клапана, изолированном протезировании одной из створок митрального или аортального клапана ксеноперикардом и санации камер сердца, закрытии полости абсцесса. Общая 5-летняя выживаемость с учетом госпитальной летальности составляет 70-75%. Операция может потребоваться также для лечения тяжелых системных эмболических осложнений, для иссечения абсцесса селезенки или для лечения микотических аневризм.
Внедрение хирургического метода лечения, правильный подбор и своевременное направление больных на оперативное лечение позволяют добиться лучших результатов терапии, снизить летальность.
Профилактика развития инфекционного эндокардита у больных с повышенным риском сводится к предупреждению бактериемии, которая возникает после различных вмешательств и манипуляций. Ан-тибиотикопрофилактику следует проводить пациентам с патологией сердца при риске развития инфекционного эндокардита перед проведением инвазивных процедур.
Профилактика эндокардита необходима при следующих заболеваниях сердца:
аортальная регургитация при клапане с тремя, двумя или одной створкой
двустворчатый аортальный клапан или аортальный стеноз с каль- цинозом клапана
U8
Некоронарогенные болезни сердца
дегенеративные изменения клапана у лиц пожилого возраста
гипертрофическая кардиомиопатия
митральная регургитация
митральный стеноз
пролапс митрального клапана с регургитацией
большинство врожденных аномалий, в том числе цианотические состояния, дефекты межжелудочковой перегородки, незаращение боталлова протока и коарктация аорты
инфекционный эндокардит в анамнезе, даже при отсутствии за болевания сердца в данный момент
искусственные клапаны сердца (как био-, так и механические протезы)
стеноз легочной артерии
ревматическая или другая клапанная дисфункция, даже после кар- диохирургической коррекции
внутрисердечная патология после хирургической коррекции с остаточными нарушениями гемодинамики или остаточными или небольшими гемодинамическими нарушениями в первые 6 мес после коррекции
• патология трехстворчатого клапана. Профилактику не проводят при:
ишемической болезни сердца при наличии атеросклеротических изменений
изолированном дефекте межжелудочковой перегородки
пролапсе митрального клапана без регургитации (хотя риск воз растает, если пролапс совпадает с утолщением створки клапана)
физиологических, функциональных и других «невинных» шумах в сердце
наличии кардиостимулятора или имплантированного дефибрил лятора
аортокоронарном шунтировании в анамнезе
болезни Кавасаки без дисфункции клапана
кардиохирургической коррекции внутрисердечной патологии без остаточных явлений через 6 мес после операции
149
Некоронарогенные болезни сердца
• умеренной клапанной регургитации без структурных изменений клапана по данным эхокардиографии.
Антибиотикопрофилактика инфекционного эндокардита не является необходимой при выполнении многих относительно безопасных процедур, таких, как диагностическая катетеризация сердца, имплантация электрокардиостимулятора, интубация, бронхоскопия гибким бронхоскопом, неосложненные диагностические процедуры на органах пищеварения, пломбирование зубов выше линии десен и стоматологическое протезирование.
Некоронарогенные болезни сердца
