
- •Глава 1. Некоронарогенные болезни
- •I II. Стандарты и критерии диагностики воспалительных поражений сердца
- •Глава 2. Функциональные болезни сердца
- •(Заполняется врачом)
- •Глава 3. Метаболические и дегенеративные (дистрофические)
- •Глава 4. Перикардиты
- •Глава 5. Эндокардиты
- •Глава 6. Миокардиты
- •Глава 7. Пролапс митрального клапана
- •Глава 8. Приобретенные пороки сердца
- •Глава 9. Врожденные пороки сердца
- •Глава 10. Дилатационная кардиомиопатия
- •Глава 11. Гипертрофическая кардиомиопатия
- •Глава 12. Рестриктивная кардиомиопатия
- •Глава 13. Аритмогенная кардиомиопатия (дисплазия) правого желудочка
- •Глава 14. Опухоли сердца
- •Глава 15. Травмы сердца
Глава 11. Гипертрофическая кардиомиопатия
Гипертрофическая кардиомиопатия характеризуется очаговой или диффузной гипертрофией миокарда левого и/или правого желудочка, чаще асимметричной, с вовлечением межжелудочковой перегородки, нормальным или уменьшенным объемом левого желудочка.
Впервые данные о гипертрофической кардиомиопатии систематизированы в конце 50-х годов XX века. Заболевание имело несколько названий: гипертрофическая обструктивная кардиомиопатия, идиопа-тический гипертрофический субаортальный стеноз и мышечный субаортальный стеноз. Термин «гипертрофическая кардиомиопатия» в настоящее время является наиболее универсальным.
Долгое время считалось, что гипертрофическая кардиомиопатия — достаточно редкое заболевание, однако проспективное исследование В. J. Магоп и соавторов (1995) показало, что распространенность его составляет 0,2% общей популяции и наблюдается преимущественно у мужчин.
Этиология. В настоящее время многочисленные исследования подтвердили роль генетических нарушений в развитии гипертрофической кардиомиопатии, доказано, что это наследственное заболевание с аутосомно-доминантным типом наследования. Причиной болезни является мутация саркомерных генов.
Результаты молекулярно-генетических исследований свидетельствуют, что все мутации генов касаются белков миофибрилл:
1) саркомерных сократительных белков:
бета-миозина тяжелой цепи (14-я хромосома, ген MYH7)
дополнительной легкой цепи-1 желудочкового миозина (3-я хро мосома, ген MYL3)
регуляторной легкой цепи-2 желудочкового миозина (12-я хромо сома, ген MYL2)
2) ассоциированных белков:
сердечного тропонина-Т (1-я хромосома, ген TNNT2)
сердечного тропонина-I (ген TNNI3)
381
Некоронарогенные
болезни сердца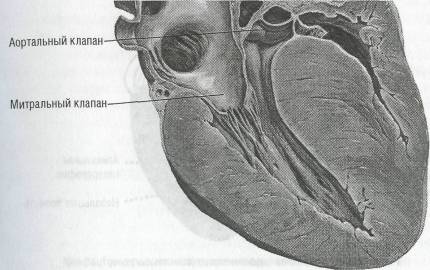
• а-тропомиозина (15-я хромосома, ген ТРМ1) 3) миозинсвязывающего белка:
• связывающего протеин-С сердечного миозина (11-я хромосома, ген MYBPC3).
В возникновении заболевания может также иметь значение нарушение взаимодействия развивающегося сердца плода с катехоламина-ми, тиреоидными гормонами, соматотро пином, аденозином.
Распространенность и локализация гипертрофии значительно варьирует, даже среди родственников. Одинаковая мутация может привести к тяжелой гипертрофии желудочка у одного члена семьи и умеренной гипертрофии у другого. Причины этих фенотипических различий у лиц с идентичной генетической мутацией не совсем понятны, но могут быть следствием других генетических факторов, которые играют роль в экспрессии гипертрофии сердца, таких, как DD-генотип ангиотензинпревращающего фермента, натрийуретические пептиды и другие детерминанты роста миоци-тов. Установлено, что DD-генотип ангиотензинпревращающего фермента наиболее часто обнаруживается у больных с тяжелой гипертрофией и у больных из семей с высокой частотой внезапной коронарной смерти.
Патологическая анатомия. Макроскопически гипертрофическая кардиомиопатия наблюдается в виде трех вариантов:
асимметричная — изолированная гипертрофия межжелудочковой перегородки (изолированный гипертрофический субаортальный стеноз) (рис. 49);
гипертрофия различных отделов левого желудочка, чаще апикаль ной части (рис. 50);
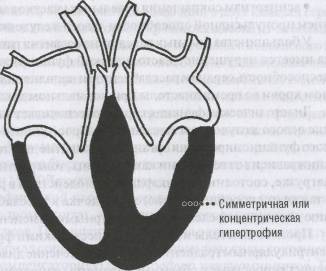
•симметричная— тотальная концентрическая гипертрофия (рис. 51).
При морфологическом исследовании чаще (60- 95%) выявляется асимметричная гипертрофия левого желудочка — преимущественная гипертрофия межжелудочковой перегородки, при которой часто стенозируется выносящий тракт левого желудочка. Иногда следствием гипертрофии является одновременное сужение выносящего тракта правого желудочка. Гораздо реже отмечается симметричная гипертрофия, верхушечная гипертрофия, гипертрофия средней части или свободной стенки левого желудочка. Рав-
3 82
Рис. 49. Гипертрофическая кардиомиопатия (идиопатический гипертрофический субаортальный стеноз; по F. Netter, 1969, с изменениями)
номерная концентрическая гипертрофия миокарда сопровождается значительным увеличением массы сердца, но обструкции желудочков не наблюдается. Правый желудочек вовлекается в патологический процесс примерно в 50% случаев, что значительно усугубляет течение заболевания.
В зависимости от выраженности утолщения миокарда выделяют три степени гипертрофии:
умеренная гипертрофия — 15-20 мм,
средней степени — 21-25 мм,
выраженная гипертрофия — более 25 мм.
383
Некоронарогенные болезни сердца
Некоронарогенные болезни сердца
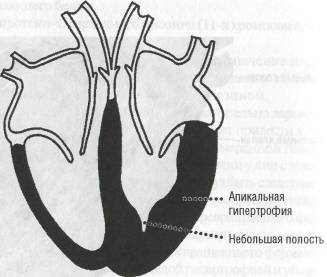
Характерным анатомическим признаком гипертрофической кардиомио-патии является структурное изменение митрального клапана, передняя створка которого расположена под углом к плоскости клапана, утолщена и «выпадает» в просвет выносящего тракта левого желудочка, образуя дополнительное препятствие кровотоку. Полость левого желудочка небольших размеров, левое предсердие часто гипертрофировано и дилатировано.
Типичные патогистологические изменения включают гипертрофию кардиомиоцитов и нарушение взаимной ориентации мышечных волокон (как наиболее частый результат мутаций саркомеров), а также очаги фиброза и рубцовые изменения вследствие некроза миокарда. Волокна размещаются короткими рядами, имеют склонность к закручиванию при отсутствии изменений интрамуральных сосудов. Ядра клеток изменены, имеют уродливую форму, часто окружены светлой зоной («пери-нуклеарным нимбом»), в которой отмечается накопление гликогена.
Рис.51. Гипертрофическая кардиомиопатия (симметричная гипертрофия)
Патогенез и патофизиология. При гипертрофической кардиомиопа-тии генетическая неполноценность сократительных белков обусловливает нарушение обменных и сократительных процессов в гипертрофированной мышце. Морфологические изменения левого желудочка определяют состояние кардиогемодинамики.
К основным патогенетическим факторам гипертрофической кар-диомиопатии относятся:
снижение эластичности и сократительной способности гипертро фированного миокарда левого желудочка с ухудшением его диастоли- ческого наполнения, в результате чего в пересчете на единицу массы миокарда работа сердца существенно уменьшается;
несоответствие коронарного кровотока в неизмененных сосудах степени гипертрофии миокарда;
сдавление коронарных сосудов гипертрофированным миокардом;
Некоронарогенные болезни сердца
• нарушение скорости проведения возбуждения в желудочках с асинхронным сокращением различных отделов миокарда;
• асинергизм сокращения отдельных участков миокарда со снижением пропульсивной способности левого желудочка.
У большинства больных вследствие развития гипертрофии миокарда имеется нарушение диастолической функции левого желудочка — неспособность сердца к расслаблению и наполнению адекватным объемом крови во время диастолы при нормальном давлении наполнения.
Диастолическая функция сердца обеспечивает адекватное наполнение левого желудочка и сердечный выброс, достаточный для нормального функционирования организма. Развитие диастолической дисфункции зависит от геометрии камер сердца, толерантности желудочков к нагрузке, состояния перикарда, взаимодействия в работе желудочков, а также от способности левого желудочка к расслаблению и наполнению, которая определяется структурными изменениями миокарда.
Процесс диастолы модулируется несколькими факторами: 1) атрио-вентрикулярным градиентом давления в течение диастолы, который изменяет скоростные и объемные параметры наполнения левого желудочка и зависит от сократимости левого предсердия, конечно-систолического объема левого желудочка, расслабления и жесткости камер сердца; 2) активной релаксацией камер сердца, которая захватывает по времени вторую половину систолы, период изоволюмического расслабления и начало фазы быстрого наполнения левого желудочка и зависит от структурных изменений миокарда; 3) жесткостью миокарда и общей жесткостью камер (левого предсердия и левого желудочка) — пассивными характеристиками диастолы, проявляющимися после полного завершения процессов расслабления. Повышенная жесткость миокарда желудочка приводит к увеличению сопротивления диастолическому току крови в него и ухудшению диастолического расслабления.
Диастолическая функция включает в себя активные и пассивные фазы. После закрытия аортального клапана происходитизоволюмическое расслабление левого желудочка, при котором меняется форма камеры сердца, однако ее объем не увеличивается, эта фаза требует энергетических затрат (см.
386
Некоронарогенные болезни сердца
рис. 47). Когда открывается митральный клапан, начинается фаза быстрого наполнения, во время которой кровоток из левого предсердия в левый желудочек осуществляется за счет разницы давления в двух камерах сердца (см. рис. 21). В начале диастолы скорость кровотока высока из-за большой разницы в давлении, которая уменьшается по мере наполнения левого же -лудочка, и наступает фаза медленного наполнения. Когда давление в левом предсердии и желудочке выравнивается, дальнейшее пассивное наполнение желудочка становится невозможным и дополнительное наполнение обеспечивается за счет сокращения предсердия (фаза систолы предсердий). При отсутствии патологии сердца наполнение левого желудочка происходит в основном в фазу медленного наполнения, доля которой составляет около 50-60%. Доля фаз быстрого наполнения и систолы предсердий составляет 25- 30% и 15- 20% соответственно.
При гипертрофической кардиомиопатии первичное повреждение происходит в кардиомиоцитах, где осуществляются мутации генов сократительных белков. Повышение нагрузки на оставшиеся интактны-ми части миофибрилл сопровождается повышением силы сокращения и стимулирует компенсаторную гипертрофию кардиомиоцитов. При развитии гипертрофии левого желудочка происходит структурное ре-моделирование миокардиальной ткани, обусловленное изменением внеклеточного матрикса — коллагеновой сети, состоящей преимущественно из коллагена и белков, связывающих коллагеновую сеть с мембраной кардиомиоцитов и миофибриллами. Состав коллагеновой сети во многом определяет механические свойства миокарда во время диастолы. Изменение нагрузки на сердечную мышцу требует соответствующего уплотнения коллагеновой сети, вследствие чего возникает реактивный или добавочный фиброз. При гипертрофической кардиомиопатии отмечается также ишемическое повреждение миокарда, которое сопровождается некрозом кардиомиоцитов, на месте которых происходит разрастание коллагеновых волокон, закрывающее дефект, — развивается также репаративный, или заместительный фиброз. Фиброз миокарда сочетается с преимущественным накоплением коллагена I типа.
Содержание коллагена во внеклеточном матриксе находится под контролем ренин-ангиотензиновой системы, циркулирующий ангио-
Некоронарогенные болезни сердца
тензин II может прямо стимулировать синтез коллагена и ингибиро-вать активность коллагеназы — ключевого энзима в процессе распада коллагена. В настоящее время многие исследователи допускают также возможность прямой паракринной или опосредованной регуляции диастолической функции за счет высвобождения медиаторов из коронарного эндотелия (оксида азота, эндотелина-1, предсердного натрий -уретического фактора или других неизвестных агентов).
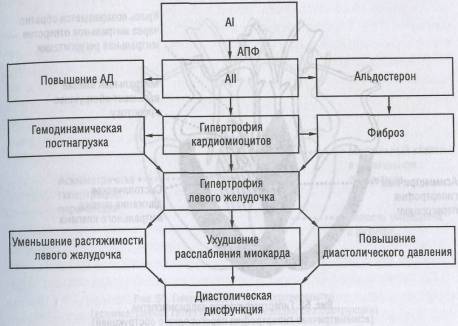
При гипертрофической кардиомиопатии рост коллагеновой сети продолжается непрерывно. Связанная с ростом матрикса возрастающая упругость миокарда облегчает сокращение во время систолы, но в значительной мере затрудняет наполнение камер сердца во время диастолы. Фиброз миокарда ухудшает расслабление миокарда и растяжимость левого желудочка, что приводит к повышению диастолического давления при любом фиксированном объеме наполнения (схема 9).
Ухудшение диастолической функции также может вызывать тканевый ангиотензин II, который ухудшает расслабление миокарда путем повышения концентрации свободных ионов кальция в кардиомиоцитах.
В результате диастолической дисфункции возникает хроническое повышение конечно-диастолического давления левого желудочка, давления заклинивания капилляров легочной артерии, застой в легких, прогрессирующая гипертрофия предсердий, фибрилляция предсердий. В измененных участках миокарда электрический сигнал может стать нестабильным вследствие наличия участков фиброза и дезориентированных кардиомиоцитов. Нарушение взаимной ориентации кардиомиоци-тов является патологическим субстратом для развития злокачественных желудочковых аритмий, которые могут быть причиной внезапной смерти. Вероятно, провоцирующими факторами являются ишемия и/или чрезмерная катехоламиновая стимуляция миокарда при нагрузках.
Нарушение диастолической функции еще больше усиливается во время тахикардии — из-за уменьшения продолжительности диастолы и ослабления систолы предсердий (уменьшения «предсердной надбавки»). Брадикардию больные также плохо переносят из-за невозможности компенсаторного расширения сердца с увеличением ударного объема.
388
Некоронарогенные болезни сердца Схема 9. Роль ренин-ангиотензиновой системы в патогенезе диастолической дисфункции
Систолическая функция при гипертрофической кардиомиопатии не нарушена или даже усилена вследствие гипердинамичности левого желудочка (фракция выброса достигает 80-90%). Левый желудочек выбрасывает почти всю кровь, поступающую в него во время диастолы, однако этого объема крови нередко бывает недостаточно для поддержания адекватной гемодинамики, так как конечно-диа-столический объем уменьшен (нередко менее 100 мл, иногда даже менее 70 мл).
В зависимости от степени выраженности преграды оттоку крови выделяют две основные формы гипертрофической кардиомиопатии:
обструктывная — характеризуется наличием градиента давления между полостью левого желудочка и аортой (рис. 52)
необструктывная — без градиента давления (рис. 53).
389
Некоронарогенные болезни сердца
Некоронарогенные болезни сердца
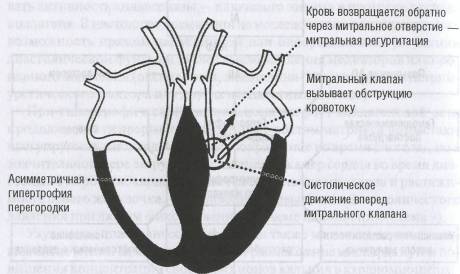
Возникновение обструкции объясняют противопоставлением гипертрофированной межжелудочковой перегородки и передней створки митрального клапана во время систолы (передняя створка митрального клапана втягивается в выходной тракт левого желудочка). Обструкция может быть постоянной (регистрироваться в покое) или латентной (динамической), возникающей только при инотропной стимуляции и/или уменьшении объема левого желудочка. У некоторых больных отмечается не обструкция, а скорее элиминация полости левого желудочка — соприкосновение стенок левого желудочка во время систолы с почти полным исчезновением полости. Первоначально именно обструкции придавали основное значение в возникновении нарушений гемодинамики при гипертрофической кардиомиопатии, однако последующие исследования показали, что хотя обструкция, несом-
390
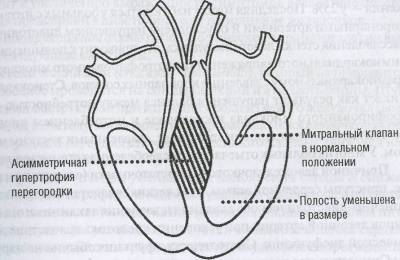
Рис. 53. Гипертрофическая кардиомиопатия (асимметричная гипертрофия перегородки без обструкции)
ненно, играет важную роль в характере клинических симптомов, в диагностике и выборе лечебных мероприятий, определяющим моментом является нарушение диастолической функции.
Клиника и диагностика. Степень обструкции и гипертрофии левого желудочка не коррелирует с наличием клинических симптомов. Гипертрофическая кардиомиопатия может быть полностью бессимптомной или манифестировать в любом возрасте. Появление симптомов прежде всего обусловлено нарушением диастолической функции, а также возникновением аритмий, которые ее усиливают. В некоторых случаях внезапная смерть может быть первым проявлением заболевания. Наиболее часто симптомы проявляются у 40- 50-летних пациентов.
Классическая триада симптомов при гипертрофической кардиомиопатии включает стенокардию напряжения, одышку при нагрузке и обмороки.
Некоронарогенные болезни сердца
Болевые ощущения в грудной клетке отмечаются у 75% больных с гипертрофической кардиомиопатией, классическая стенокардия напряжения— у 25%. Последняя может наблюдаться у больных с интактными коронарными артериями и обусловлена нарушением диастолического расслабления стенки левого желудочка, что приводит к повышению внут-римиокардиального напряжения гипертрофированного миокарда и ин-трамиокардиальному сдавлению коронарных сосудов. Стенокардия возникает как результат нарушения баланса между потребностью гипертрофированного миокарда в кислороде и потреблением кислорода, доставляемого коронарными артериями, сдавленными жестким миокардом. У многих больных отмечается послеобеденная стенокардия.
Причиной левожелудочковой недостаточности (одышка при нагрузке, приступы сердечной астмы, отек легких) является быстрый подъем конечно-диастолического давления и давления заклинивания капилляров легочной артерии при ускорении кровотока вследствие диасто-лической дисфункции. Систолическая функция обычно не нарушена.
Синкопальное состояние — наиболее тяжелое проявление гипертрофической кардиомиопатии, основными причинами его являются нарушение диастолического наполнения левого желудочка, возникновение аритмий, обструкция выносящего тракта. Сердце не способно увеличить сердечный выброс при физической нагрузке, в результате происходит перераспределение кровотока к работающим мышцам и наступает ишемия мозга с кратковременной потерей сознания. Обмороки вызваны увеличением степени обструкции (и снижением сердечного выброса) вследствие редуцированного периода диастолического наполнения, что обусловлено синусовой тахикардией при физической нагрузке. Чаще всего обмороки наблюдаются у больных молодого возраста, у многих из них при суточном мониториро-вании ЭКГ регистрируются эпизоды желудочковой тахикардии, нарушений проводимости.
У значительного числа больных (5-28%) возникает фибрилляция предсердий, повышающая риск развития тромбоэмболических ослож-
392
Некоронарогенные болезни сердца
нений. При тяжелой диастолической дисфункции ее возникновение приводит к увеличению выраженности симптомов вследствие потери «вклада» предсердий в диастолическое наполнение желудочков.
При обструктывной форме гипертрофической кардиомиопатии выявляют следующие симптомы:
систолический шум (crescendo-diminuendo), который не проводится или слабо проводится на сонные артерии и в область спины. Шум вызван обструкцией при изгнании крови из левого желудочка (воз никает в систолу, когда гипертрофированная межжелудочковая пе регородка и передняя створка митрального клапана движутся на встречу друг другу);
шум усиливается при уменьшении наполнения сердца и сниже нии общего периферического сосудистого сопротивления (вста вание из положения сидя на корточках, натуживание, прием нит роглицерина) и ослабевает при увеличении наполнения сердца, повышении общего периферического сосудистого сопротивления (в положении лежа, сидя на корточках, при сжимании кулаков);
пульсация сонных артерий, быстрый «отрывистый» пульс при пальпации сонных артерий, являющиеся отражением очень быст рого изгнания крови в первую половину систолы;
усиленный продолжительный верхушечный толчок, занимающий всю систолу вплоть до II тона, что является признаком гипертро фии левого желудочка;
при пальпации верхушечного толчка в положении на левом боку с задержкой дыхания на выдохе иногда ощущается двойной подъем — пальпируется IVтон, являющийся отражением усиленного сокраще ния предсердий при уменьшении податливости левого желудочка;
• при аускультации тоны сердца глухие, выявляется IVтон.
При необструктивной форме гипертрофической кардиомиопатии отклонений от нормы при физикальном обследовании может не быть, но иногда определяются:
• увеличение продолжительности верхушечного толчка, •IVтон сердца.
393
Некоронарогенные болезни сердца
Характернькрентгенолопетескихгфизнаковптертрофическаякардио-миопатия не имеет, картину во многом определяет степень выраженности заболевания. Возможны следующие рентгенологические изменения:
в первом косом положении появляется выбухание левого желу дочка, обусловленное гипертрофией путей оттока,
отсутствие талии сердца и закругления дуг,
расширение левого предсердия.
Специфических для гипертрофической кардиомиопатии ЭКГ-признаков не существует, наиболее часто выявляются следующие изменения;
признаки гипертрофии левого желудочка;
нарушения реполяризации в виде депрессии сегмента ST u инвер сии зубца Т;
у 25- 30% больных глубокие и патологически уширенные зубцы Q в отведениях II, III, aVF,V5_6;
•при асимметричной септальной гипертрофии регистрируются очень глубокие зубцы Q в отведениях I, aVL, V5_6;
QS-комплекс в отведениях V1 и V2, что может симулировать пере несенный инфаркт миокарда;
при апикальной гипертрофии могут определяться глубокие «ги гантские» (до 4 см) симметричные отрицательные зубцы T в отве дениях I, aVL, V5_6;
•признаки гипертрофии левого предсердия: уширенный и зазубренный зубец Pβ отведениях II, III, aVF с двухфазной волной Р в отведениях V1- 2;
нарушения ритма сердца: суправентрикулярные и желудочковые экстрасистолы, фибрилляция предсердий, пароксизмы желудоч ковой тахикардии;
нарушения внутрижелудочковой проводимости.
Наличие или отсутствие глубоких отрицательных зубцов T не имеет прогностического значения.
Эхокардиография является методом выбора для диагностики гипертрофической кардиомиопатии. По данным эхокардиографического исследования можно выявить асимметричный характер гипертрофии
3 94
Некоронарогенные болезни сердца
левого желудочка и определить наиболее распространенные варианты локализации гипертрофии миокарда:
гипертрофия базальных отделов межжелудочковой перегородки;
тотальная гипертрофия межжелудочковой перегородки и/или свободной стенки левого желудочка;
гипертрофия верхушки сердца с распространением на свободную стенку левого желудочка.
При эхокардиографическом исследовании наиболее часто обнаруживаются:
гипертрофия стенок желудочков,
увеличение фракции выброса (часто более 80%),
увеличение полости левого предсердия,
нарушение диастолической функции при допплер-эхокардиографии.
При проксимальной форме гипертрофической кардиомиопатии (субаортальном стенозе) наиболее характерными эхокардиографическими признаками являются (рис. 54):
• утолщение межжелудочковой перегородки в базальном сегменте,
снижение экскурсии межжелудочковой перегородки в базальном сегменте,
увеличение соотношения толщины межжелудочковой перегород ки и задней стенки более 1,3(1,5- 2),
увеличение соотношения размера левого предсердия и корня аор ты более 0,9,
уменьшение размера полости левого желудочка (во время систо лы может полностью спадаться),
снижение скорости диастолического закрытия передней створки митрального клапана,
наличие градиента давления при допплер-эхокардиографии,
переднесистолическое движение передней створки митрального клапана,
уменьшение расстояния от митрального клапана до межжелудоч ковой перегородки к началу систолы,
среднесистолическое закрытие аортального клапана.
395
Некоронарогенные
болезни сердца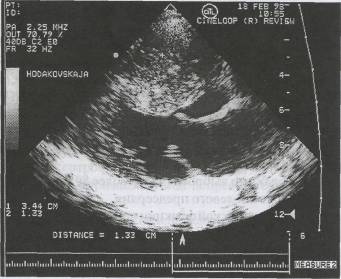
тракта (В-режим)
Для дистальной формы (верхушечной гипертрофической кардиомио-патии) при эхокардиографическом исследовании наиболее характерно:
утолщение межжелудочковой перегородки в верхушечном сегмен те по длинной оси в двухмерном изображении,
уменьшение амплитуды движения гипертрофированных участков межжелудочковой перегородки и прилегающих к ней участков задней стенки в верхушечном сегменте левого желудочка,
полость левого желудочка в левой апикальной 4-мерной позиции имеет пикоподобную форму за счет гипертрофии дистальных отделов межжелудочковой перегородки и прилегающих отделов задней стенки левого желудочка.
Концентрическая (симметричная) форма характеризуется:
• утолщением межжелудочковой перегородки и задней стенки ле вого желудочка в диастолу при значительном увеличении общей массы миокарда,
396
Некоронарогенные болезни сердца
уменьшением систолического утолщения межжелудочковой пе регородки и задней стенки левого желудочка,
снижением экскурсии движения гипертрофированных участков миокарда,
уменьшением систолического и диастолического объемов левого желудочка,
повышением индекса соотношения размеров левого предсердия и устья аорты.
Изолированная гипертрофия правого желудочка при эхокардиографическом исследовании имеет следующие признаки:
увеличение диастолической толщины межжелудочковой перего родки в верхушечном сегменте,
утолщение передней стенки правого желудочка,
уменьшение диастолического размера правого желудочка (на уров не верхушечного сегмента),
уменьшение амплитуды движения межжелудочковой перегород ки в верхушечном сегменте.
При биопсии миокарда обнаруживается:
хаотическое расположение волокон миокарда,
укорочение волокон миокарда,
дегенеративные изменения с исчезновением миофибрилл,
деформация ядер клеток,
фиброзное замещение миокарда.
Методом верификации диагноза является магнитно-резонансная томография, с помощью которой возможно наиболее точно оценить морфологические изменения, оценить распространенность и выраженность гипертрофии миокарда у больных с гипертрофической кардиомиопатией. Особенно ценен метод для диагностики верхушечной формы заболевания и гипертрофии нижней части межжелудочковой перегородки и правого желудочка.
Катетеризация полости сердца обычно проводится при клинически выраженной митральной регургитации для оценки возможности хирургического лечения. Внугрижелудочковые градиенты давления обнаружи-
~397
Некоронарогенные болезни сердца
ваются в левом и реже правом желудочке. Градиент повышается после экстрасистол, во время пробы Вальсальвы и после ингаляции амилнитри-та. Конечно-диастолическое давление повышено вследствие плохой податливости желудочка. Вентрикулография обнаруживает характерную де-формированность камеры, зависящую от формы гипертрофической кар-диомиопатии и также иногда подтверждает митральную регургитацию. Коронарные артерии обычно широкие с адекватным кровотоком.
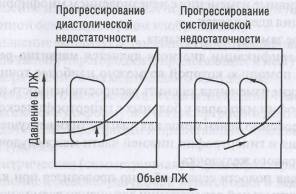
Рис. 55. Оценка диастолической дисфункции: связь давление — объем
Хотя и не существует единственного параметра для глобальной оценки диастолической функции, ценные результаты могут быть получены путем графического построения кривой давление - объем, которая показывает связь между давлением в левом желудочке и объемом в течение сердечного цикла. При диастолической дисфункции более высокое диа-столическое давление требует достижения заданного диастолического объема, отражая сниженную растяжимость миокарда левого желудочка и сдвигая кривую давление — объем вверх (при систолической дисфункции кривая давление — объем сдвигается вправо, отражая повышенный конечно-систолический объем левого желудочка с уменьшением ударного объема и повышением конечно-диастолического давления левого желудочка, диастолическии участок кривой сдвигается вверх и вправо без изменений растяжимости миокарда левого желудочка) (рис. 55).
Некоронарогенные болезни сердца
Для оценки диастолической функции сердца могут использоваться и другие показатели, например, жесткость миокарда левого желудочка, представленная графически как кривая тангенциальной зависимости диастолического давления — объема (dP/dV) для последовательных измерений диастолической функции. Однако этот показатель пригоден лишь для тех случаев, когда измерения проводятся при одинаковом объеме левого желудочка. Для диагностики диастолической дисфункции может также иметь значение оценка давления наполнения левого желудочка, которое может повышаться из-за ухудшения скорости и степени релаксации миокарда левого желудочка. Поскольку технически проще оценить гемодинамику левого желудочка, чем скорость и степень изо-волюмической релаксации, то диастолическое наполнение более часто используется как показатель диастолической функции, чем изоволюми-ческое расслабление или кривая давление — объем.
При подозрении на гипертрофическую кардиомиопатию в установлении диагноза может помочь генетическое исследование, которое позволяет выявить характерные мутации генов, ответственных за синтез сократительных белков кардиомиоцитов, однако эти исследования мало доступны в клинической практике.
Дифференциальная диагностика
Диагностика гипертрофической кардиомиопатии не представляет сложностей при наличии классических признаков, однако они часто отсутствуют. В случае подозрения на гипертрофическую кардиомиопатию важно исключить наличие гипер- или гипотиреоза, артериальной гипертензии, аортального стеноза.
Трудности возникают при обнаружении умеренной гипертрофии левого желудочка у больных с нормальным или пограничным уровнем артериального давления. Наиболее сложной представляется дифференциальная диагностика гипертрофической кардиомиопатии с повышенным артериальным давлением и эссенциальной артериальной гипертензии. При обнаружении умеренной или выраженной гипертрофии левого желудочка у больных без указания в семейном анамнезе на гипертрофическую кардиомиопатию для дифференциального диагноза следует проводить 24-часовое амбулаторное мониторирование артериального давления.
399
Некоронарогенные болезни сердца
Принципы дифференциальной диагностики гипертрофической кардиомиопатии и «спортивного» сердца приведены в табл. 16.
Таблица 16. Дифференциальная диагностика гипертрофической кардиомиопатии и «спортивного» сердца
Признаки |
«Спортивное» сердце |
Гипертрофическая хардиомиопатия |
Характер гипертрофии левого желудочка |
Симметричный |
Чаще асимметричный |
Полость левого желудочка в диастолу |
>55 мм |
<45мм |
Наполнение левого желудочка |
Нормальное |
Аномальное |
Размеры левого предсердия |
Нормальные |
Увеличены |
Систолическое смещение вперед митрального клапана |
Отсутствует |
Часто наблюдается |
Толщина стенки левого желудочка |
Уменьшается при прекращении тренировок |
Остается постоянной |
Несмотря на высокую точность современных диагностических методов, иногда при трактовке эхокардиографических находок случаются принципиальные диагностические ошибки, которые влекут за собой неправильную лечебную тактику.
Приводим клиническое наблюдение.
Больной К., 27лет, поступил в клинику 30.03. 98 г. с жалобами на одышку, возникающую при подъеме на несколько этажей, ноющую ирра-диирующую под левую лопатку боль в области сердца, которая возникает без видимой причины, длится несколько часов, не купируется приемом нитроглицерина.
В кардиологическом отделении районной больницы в марте 1997 г. впервые была проведена эхокардиография, обнаружено утолщение межжелудочковой перегородки в апикальных отделах до 18 мм, установлен диагноз: гипертрофическая кардиомиопатия. Амбулаторно назначен ве-рапамил, на фоне применения которого в течение года пациент отмечал дальнейшее снижение переносимости физических нагрузок.
При эхокардиографическом исследовании в клинике Института кардиологии: размеры левого предсердия нормальные (35мм), некоторое увеличение полости левого желудочка (конечно-диастолический объем 157 мл, конечно-диастолический индекс — 87мл/м2), утолщение межжелудочковой перегородки до 12мм и ее гипокинез в области верхушки, толщина зад-
400
Некоронарогенные болезни сердца
ней стенки нормальная (10 мм), снижение фракции выброса левого желудочка до 50%. В апикальной части обоих желудочков обнаружен пучок дополнительных хорд (рис. 56).
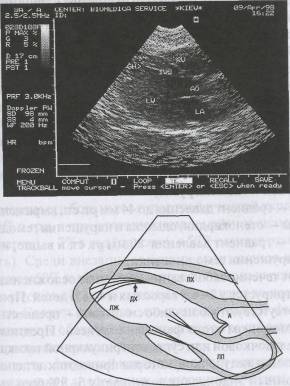
Рис. 56. ЭхоКГ больного К.
При велоэргометрическом исследовании выявлено умеренное снижение толерантности к физической нагрузке (75 Вт в течение Змин), при расчетной нагрузке 180 Вт проба прекращена в связи с жалобами пациента на одышку, усталость.
Установлен диагноз: аномалия развития хордального аппарата сердца, сердечная недостаточность I стадии.
401
Некоронарогенные болезни сердца
Под влиянием ингибитора АПФ и диуретика отменено улучшение самочувствия, уменьшение одышки при физической нагрузке.
Таким образом, правильная трактовка эхокардиографических данных позволила установить правильный диагноз и причины возникновения сердечной недостаточности, исключить наличие у больного гипертрофической кардиомиопатии и назначить адекватное лечение.
Течение гипертрофической кардиомиопатии медленно прогрессирующее. Тяжесть течения зависит от локализации и степени гипертрофии миокарда в зоне утолщения, а также от обструкции выносящего тракта левого желудочка. В настоящее время общепринятой является классификация Нью-Йоркской ассоциации сердца:
/стадия — градиент давления до 25 мм рт. ст., как правило, жалоб больные не предъявляют;
IIстадия - градиент давления до 36 мм рт. ст., самочувствие ухудшается при физической нагрузке;
IIIстадия — градиент давления до 44 мм рт. ст., выражены клинические симптомы - стенокардия, одышка и нарушения гемодинамики
IVстадия — градиент давления 80 мм рт. ст. и выше, имеются значительные нарушения гемодинамики.
Усугубляют течение заболевания серьезные осложнения. Внезапная смерть регистрируется у 2-4% взрослых и 4- 6% детей. При этом у многих больных отсутствуют какие-либо симптомы — предвестники внезапной смерти, механизм этого феномена не ясен. Предполагается, что вследствие желудочковой или суправентрикулярной тахикардии возникает фибрилляция желудочков, которая приводит к летальному исходу.
Инфекционный эндокардит возникает у 5-9% больных. Поражения эндокарда провоцируются митральной регургитацией, турбулентными потоками в выносящем тракте левого желудочка (что приводит к утолщению аортального клапана), а также могут возникать из-за поражения митрального клапана вследствие нарушенной геометрии левого желудочка и эффекта Вентури, вызываемого быстрым ранним систолическим потоком через выносящий тракт (ударом передней створки митрального клапана о межжелудочковую перегородку).
402
Некоронарогенные болезни сердца
у 10-15% больных развиваются дилатация левого желудочка и систолическая дисфункция.
Прогноз при гипертрофической кардиомиопатии неблагоприятный, наиболее часто больные умирают внезапно, на фоне тяжелой физической нагрузки, в том числе при бессимптомном течении заболевания. Хроническая сердечная недостаточность развивается менее часто. Установленные факторы риска внезапной смерти при гипертрофической кардиомиопатии:
манифестация заболевания в молодом возрасте (до 16 лет),
наличие в семейном анамнезе эпизодов внезапной смерти,
частые синкопальные состояния,
непродолжительные эпизоды желудочковой тахикардии, выявлен ные при 24-часовом мониторировании ЭКГ,
патологическое изменение уровня артериального давления во вре мя нагрузок.
Уровень смертности больных с гипертрофической кардиомиопати-ей — около 4% в год, а при отягощенном семейном анамнезе (случаи внезапной смерти) — 7% в год (при этом в 50% случаев отмечается внезапная смерть). Среди внезапно умерших спортсменов в возрасте до 35 лет примерно у 50% выявляют гипертрофическую кардиомиопатию. Большинство случаев летального исхода возникают во время или сразу после нагрузки. Следует отметить, что степень гипертрофии левого желудочка или наличие обструкции выносящего тракта левого желудочка не имеет прогностического значения.
Лечение гипертрофической кардиомиопатии направлено на уменьшение диастолической дисфункции, гипердинамической функции левого желудочка и устранение нарушения ритма сердца.
Общие мероприятия включают ограничение физических нагрузок, которые усугубляют гипертрофию миокарда, повышают внутрижелу-дочковый градиент давления и риск внезапной смерти.
Основными препаратами являются блокаторы бета-адренорецепторов, которые эффективно устраняют симптомы у 30- 60% больных, их следует назначать больным независимо от выраженности градиента внут-
403
Некоронарогенные болезни сердца
рижелудочкового давления в покое. Благоприятные эффекты блока-торов бета-адренорецепторов включают:
блокирование избыточной активации симпатоадреналовой системы,
уменьшение потребности миокарда в кислороде,
отрицательный инотропный и хронотропный эффекты, •снижение частоты сердечных сокращений, удлинение периода
диастолического наполнения,
уменьшение гипердинамической систолической функции (сниже ние сердечного выброса),
уменьшение обструкции выносящего тракта,
•улучшение диастолической податливости гипертрофированного миокарда,
уменьшение микрососудистых повреждений миокарда,
стабилизация клеточных и лизосомальных мембран (мембрано- стабилизирующее действие),
угнетение возбудимости водителя ритма и проводимости,
уменьшение клинической симптоматики — боли в области серд ца, одышки, сердцебиения, обмороков.
Предпочтительно воздерживаться от назначения блокаторов β-aope-норецепторов с внутренней симпатомиметической активностью (пин-дол ол, окспренолол). Пропранолол назначают в дозе 240-320 мг в сутки и более (максимальная суточная доза — 480 мг), метопролол — в дозе 200 мг в сутки и более. Кардиоселективные блокаторы бета-адренорецеп-торов при гипертрофической кардиомиопатии не имеют преимуществ перед неселективными, так как в высоких дозах селективность практически утрачивается.
В случае противопоказаний к назначению блокаторов бета-адреноре-цепторов или неполного исчезновения симптомов, несмотря на их применение, альтернативой могут быть блокаторы кальциевых каналов. Эти препараты различаются по выраженности отрицательного ино-тропного эффекта и вазодилатирующего действия.
Препаратом выбора для больных с гипертрофической кардиомио-патией является верапамил, так как он обладает наиболее ВЫражеН-
Некоронарогенные болезни сердца
ным отрицательным инотропным действием по сравнению с дилтиа-земом и нифедипином.
В основе терапевтического эффекта верапамил а лежит его способность существенно влиять на диастолическую дисфункцию левого желудочка: он вызывает укорочение продолжительности и повышение скорости изометрического расслабления, повышение диастолического расслабления камеры желудочка, что сопровождается смещением кривой «давление — объем» книзу. Улучшение диастолического расслабления миокарда обусловлено непосредственным воздействием верапамила на кардиомиоци-ты и уменьшением ишемии субэндокардиальных слоев гипертрофированного миокарда в результате коронародилатации и снижения потребности в кислороде. Вызываемое верапамилом уменьшение внугрижелудочкового градиента обусловлено главным образом улучшением диастолических свойств миокарда и увеличением объема левого желудочка.
У некоторых больных, преимущественно с обструктивной гипертрофической кардиомиопатией, на фоне приема верапамила отмечались серьезные осложнения вплоть до отека легких, заканчивающегося летально (вероятно, вследствие резкого снижения общего периферического сосудистого сопротивления и увеличения внугрижелудочковой обструкции с усугублением диастолической дисфункции). При назначении блокаторов кальциевых каналов необходима максимальная осторожность при наличии выраженной гипертрофии и очень высоком давлении наполнения левого желудочка. Следует иметь в виду, что блокаторы кальциевых каналов, включая верапамил, при длительном применении могут повышать диастолическое давление и снижать сердечный выброс. Лечение верапамилом следует начинать с назначения в низких дозах — по 20-40 мг 3 раза в сутки, постепенно повышая до суточной дозы 240-320 мг и более. Клиническое улучшение при приеме верапамила сопровождается повышением толерантности к физической нагрузке.
Следует указать, что несмотря на улучшение клинической симптоматики, длительное применение блокаторов бета-адренорецепторов и верапамила не снижает риск внезапной смерти и не улучшает прогноз. В последние годы все чаще назначают производные бензотиазепи-на — дилтиазем, оказывающий положительное влияние на диастоли-
Некоронарогенные болезни сердца
ческую дисфункцию миокарда. Дилтиазем назначают в суточных дозах 180- 360 мг, максимальная доза — 480 мг в сутки.
К положительным эффектам блокаторов кальциевых каналов можно отнести:
улучшение диастолического расслабления путем сокращения фазы изоволюмического расслабления,
увеличение скорости раннего диастолического наполнения,
улучшение взаимоотношений между «вкладом» левого предсер дия и быстрым наполнением левого желудочка в раннюю систолу,
блокирование транспорта ионов кальция через мембраны кардио- миоцитов и гладкомышечных клеток сосудов,
снижение степени обструкции выносящего тракта левого желу дочка,
отрицательный инотропный эффект,
улучшение клинической симптоматики.
Следует указать, что блокаторы кальциевых каналов — производные дигидропиридина (нифедипин) — нельзя назначать больным с обструкцией из-за их выраженного вазодилатирующего эффекта, что связано с повышенным риском возникновения осложнений в результате увеличения препятствия изгнанию крови из левого желудочка.
При наличии нарушений сердечного ритма целесообразно назначать блокаторы бета-адренорецепторов и антиаритмические средства, однако следует отметить, что применение последних не снижает риск внезапной смерти. Есть данные, что дизопирамйд при гипертрофической кардиомиопа-тии действует как антиаритмическое средство (в отношении как супра-вентрикулярных, так и желудочковых аритмий) и как отрицательный инотропный агент. Дизопирамйд значительно уменьшает градиент давления вследствие уменьшения переднесистолического движения митрального клапана. Определенную роль играет улучшение диастолической податливости желудочка, связанной со снижением постнагрузки. Однако применение дизопирамида ограничивается развитием побочных эффектов. При наличии признаков систолической сердечной недостаточности и сниженной фракции выброса его следует применять с осторожностью, так как обладая выраженным кардиодепрессивным действием, он может
406
Некоронарогенные болезни сердца
приводить к снижению сердечного выброса и усугублению дисфункции миокарда. Рекомендуемые дозы составляют 400- 800 мг в сутки.
Единственным препаратом, на фоне которого на сегодняшний день отмечено устранение желудочковой тахиаритмии, снижение частоты случаев внезапной смерти и улучшение прогноза заболевания, является амиодарон. Помимо антиаритмического действия амиодарон вызывает улучшение и другой клинической симптоматики: уменьшение боли в области сердца, одышки, сердцебиения, головокружения, обмороков. Имеются сведения о свойстве препарата улучшать диастолическую функцию левого желудочка и повышать работоспособность. Амиодарон назначают в суточной дозе 1200 мг в течение 5-7 дней, затем в суточной дозе 800 мг и 600 мг в течение 2-й и 3-й недель лечения с последующим переходом на поддерживающую суточную дозу 200 мг. К сожалению, амиодарон имеет значительное число побочных эффектов, связанных с накоплением его в тканях, некоторые из них необратимы. Можно использовать и более низкие насыщающие дозы: 600 мг в 1-ю неделю, 400 мг — во 2-ю, а затем поддерживающую — 200 мг.
Наличие фибрилляции предсердий обычно хорошо переносится больными, однако у больных с тяжелой диастолической дисфункцией потеря предсердного «вклада» вследствие аритмии может иметь необратимые гемодинамические последствия, что требует неотложного восстановления синусового ритма посредством электрической кардио-версии или медикаментозной кардиоверсии с помощью амиодарона. В любом случае контроль ритма амиодароном или комбинацией амиодарона и блокаторов бета-адренорецепторов улучшает клинические симптомы заболевания. Последняя комбинация требует тщательного контроля ЭКГ из-за опасности развития нарушений проводимости (препараты угнетают функцию синусного и атриовентрикулярного узла).
В комплексном лечении гипертрофической кардиомиопатии можно использовать системную энзимотерапию (Коваленко В.Н.исоавт., 1999). При лечении стенокардии средством выбора являются блокаторы бета-адренорецепторов. Органические нитраты следует применять с осторожностью, так как состояние больных на фоне их применения может ухудшаться.
407
1-:" ' ■ •
Некоронарогенные болезни сердца
Рекомендуется профилактическое применение антибиотиков для предупреждения возникновения инфекционного эндокардита.
Лечебные мероприятия при гипертрофической кардиомиопатии и сердечной недостаточности в определенной степени носят парадоксальный характер: противопоказаны диуретики, которые, хотя и эффективно уменьшают застой в легких, однако могут вызвать гиповолемию, которая может усилить обструкцию выносящего тракта у больных! Слишком длительное применение диуретиков может обусловить уменьшение ударного объема и сердечного выброса.
Вазодилататоры (нитроглицерин, натрия нитропруссид) имеют ограниченное применение, поскольку несмотря на благоприятный эффект в плане сдвига кривой диастолическое давление — объем вниз, эти препараты требуют осторожного применения из-за возможного риска развития выраженной гипотензии и уменьшения размера полости левого желудочка, что может ухудшить состояние больного. Артериальные вазодилататоры (гидралазин) оказывают минимальное действие на диастолическое давление и не подходят для лечения больных с диастолической сердечной недостаточностью, так как увеличивают градиент выносящего тракта и вызывают рефлекторную тахикардию, что приводит к ухудшению диастолической функции левого желудочка.
Инотропные агенты, направленные на стимуляцию систолического выброса (сердечные гликозиды и прессорные амины), могут давать неблагоприятный гемодинамический эффект — они усиливают обструкцию выносящего тракта и не снижают повышенное конечно-диастолическое давление, могут вызвать развитие асистолии. При сохраненной систолической функции может возникнуть негативный эффект из-за усиления сократимости путем повышения внутриклеточной концентрации ионов кальция. Таким образом, при гипертрофической кардиомиопатии «чистый» эффект от положительных инотропных средств — как увеличение жесткости миокарда, так и повышение давления наполнения левого желудочка, — приводят к ухудшению диастолической функции. Тем не менее , дигоксин может использоваться у больных с диастолической дисфункцией и фибрилляцией предсердий для уменьшения частоты сердечных сокращений и/или для восстановления синусового ритма.
При лечении сердечной недостаточности у больных с гипертрофической кардиомиопатией терапевтическая стратегия должна быть на-
408
Некоронарогенные болезни сердца
правлена на стимуляцию регрессии гипертрофии левого желудочка и устранение симптомов сердечной недостаточности путем снижения давления наполнения левого желудочка без уменьшения величины сердечного выброса. В этих случаях препаратами выбора могут быть ингибиторы АПФ из-за их способности блокировать ренин-ангиотензиновую систему и вызывать обратное развитие гипертрофии левого желудочка.
Клинические исследования, проведенные в последние годы, продемонстрировали благоприятное действие ингибиторов АПФ на ряд важных показателей диастолической функции, включая диастолическое наполнение, изоволюмическое расслабление и взаимосвязь давление — объем левого желудочка и возможного обратного развития процессов ремоделирования миокарда. При этом улучшение диастолической функции (улучшение диастолической растяжимости и способности к расслаблению миокарда, снижение конечно-диастолического давления наполнения левого желудочка) было более выражено у больных с исходно более тяжелой степенью дисфункции. Ингибиторы АПФ способствуют регрессии и гипертрофии миокарда левого желудочка благодаря нормализации диастолической функции.
Хирургическое лечение, как правило, септальную миотомию или мио-эктомию, используют у больных с рефрактерными к медикаментозному лечению симптомами, у которых обструкция выносящего тракта подтверждена при катетеризации и градиент превышает 50 мм рт. ст. Хирургическое вмешательство позволяет улучшить состояние некоторых пациентов, однако не улучшает прогноз и сопряжено с повышенным риском осложнений и высокой летальностью во время операции (3-10%). Приблизительно у 5% больных операция осложняется аортальной регургитацией.
В последнее время успешно апробирован новый метод для уменьшения обструкции выносящего тракта у больных, рефрактерных к медикаментозной терапии, — алкогольная абляция межжелудочковой перегородки. Методика включает уменьшение размера левой части межжелудочковой перегородки путем ее избирательной деструкции инъецированием этилового спирта в септальную артерию. Получены предварительные результаты, однако для достоверных выводов необходимы дальнейшие исследования.
4 09
Некоронарогенные болезни сердца
