
- •Практическая работа №1
- •Материальное обеспечение:
- •Практическая работа №2
- •Материальное обеспечение:
- •Практическая работа №3
- •Материальное обеспечение:
- •Типы гидролиза солей
- •Практическая работа №4
- •Практическая работа №5
- •Материальное обеспечение:
- •Практическая работа №6
- •Материальное обеспечение:
- •Приложения
Практическая работа №1
Тема работы Упражнения в расчетах по приготовлению растворов различной концентрации
Цель работы: научиться рассчитывать и пересчитывать концентрации растворов из одних единиц в другие; на основе расчетов определять необходимые массу, объем и др. для приготовления растворов различных видов концентраций.
Количество часов: 2 ч.
Материальное обеспечение:
Краткий справочник физико-химических величин / Под редакцией К. П. Мищенко и А. А. Равделя, Л. : Химия, 1974. – 200 с.
Периодическая система химических элементов Д. И. Менделеева.
Задание
Научиться решать типовые задачи: расчет и пересчет концентраций растворов.
Порядок выполнения работы
Примеры решения типовых задач
Задача №1.
Определите: а) процентную; б) молярную; в) нормальную; г) моляльную концентрацию поваренной соли NaCl в растворе, полученном при растворении 5,85г соли в 100г воды. Плотность полученного раствора равна 1,04 г/см3.
Дано: m
|
Алгоритм решения: а)
б)
|
См=? СN=? Сm=? |
 ;
;
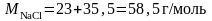
в)
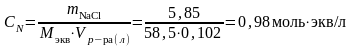
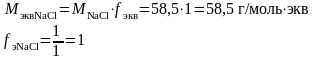
г)
Сm=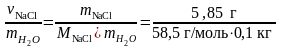 =1 моль/кг
=1 моль/кг
Ответ:
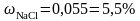 ;
СМ=0,98
моль/л; Сm=1
моль/кг; СN=0,98
моль·экв/л
;
СМ=0,98
моль/л; Сm=1
моль/кг; СN=0,98
моль·экв/л
Задача №2.
Определите процентную концентрацию поваренной соли NaCl в растворе, в 4 л которого содержится 500 г NaCl. Плотность полученного раствора равна 1,12 г/см3.
Дано: mNaCl = 500 г Vр-ра = 4 л =1,12 г/см3 |
Алгоритм решения.
mр-ра = ρр-ра ∙ Vр-ра = 1,12 г/см3 ∙ 4000 см3 = 4480 г.
|
= ? |
Ответ:

Задача №3.
Определите молярность и нормальность 12%, раствора серной кислоты с плотностью 1,08 г/см3.
Дано:
ρр-ра = 1,08 г/см3 |
Алгоритм решения.
1.
Для расчета примем
mр-ра = ρр-ра ∙ Vр-ра = 1,08 г/см3 ∙ 1000 см3 = 1080 г. 2. Определим массу серной кислоты в 1 л раствора:
|
СN(H2SO4) = ? |
3. Определим молярную концентрацию раствора (молярность):

4. Определим нормальную концентрацию раствора (нормальность):

fэкв(в-ва) = 1/(число катионов ∙ валентность).
Ответ:
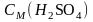 =1,32
моль/л;
=1,32
моль/л;
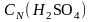 =
2,64 моль∙экв/л.
=
2,64 моль∙экв/л.
При пересчете процентной концентрации в молярную и наоборот, необходимо помнить, что процентная концентрация рассчитывается на определенную массу раствора, а молярная и нормальная – на объем, поэтому для пересчета необходимо знать плотность раствора. Если мы обозначим: С – процентная концентрация; M – молярная концентрация; N – нормальная концентрация; Э – эквивалентная масса, ρ – плотность раствора; m – мольная масса, то формулы для пересчета из процентной концентрации будут следующими:
M = (С • ρ • 10) / m
N = (С • ρ • 10) / Э
Этими же формулами можно воспользоваться, если нужно пересчитать нормальную или молярную концентрацию на процентную.
Форма предоставления результата
Выполнение индивидуальных заданий по вариантам: решение задач по названной тематике.

 NaCl=5,85
г
NaCl=5,85
г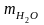 =100г
=100г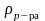 =1,04г/см3
=1,04г/см3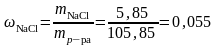 или 5,5%
или 5,5%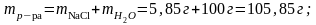
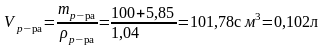
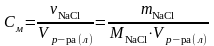
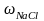 =
?
=
?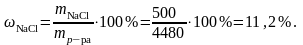
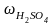 =12%
=12% =
1000 см3,
тогда
=
1000 см3,
тогда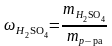 ,
отсюда
,
отсюда
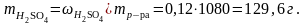
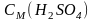 =?
=?