
- •Массообменные процессы
- •Фазовое равновесие
- •Закон Генри
- •Основное уравнение массопередачи
- •Материальный баланс массообменных процессов
- •Движущая сила массообменного процесса.
- •Средняя интегральная разность концентраций.
- •Среднелогарифмическая разность концентраций
- •Число единиц переноса
- •Ступени изменения концентрации
- •Кинетика диффузионных процессов.
- •Массообмен между двумя фазами
- •Выражение коэффициента массопередачи через коэффициенты массоотдачи
- •Подобие диффузионных процессов
- •Абсорбция
- •Равновесие при абсорбции
- •Материальный баланс абсорбции.
- •Движущая сила процесса абсорбции
- •Массопередача при абсорбции
- •Дистилляция и ректификация
- •Фазовое равновесие бинарных смесей
- •Простая перегонка. Материальный баланс простой перегонки
- •Ректификация
- •Материальный баланс ректификационной колонны
- •Уравнения рабочих линий
- •Изображение процесса ректификации на диаграмме y – X
- •Расчёт минимального флегмового числа
- •Расчет действительного числа флегмы
- •Зависимость между числом флегмы, размерами колонны и расходом теплоносителя
- •Тепловой баланс ректификационной колонны
- •Ректификация многокомпонентных смесей
- •Азеотропная и экстрактивная ректификация
- •Устройство ректификационных установок
- •Экстракция
- •Равновесие в тройных системах. 3-х угольная диаграмма Гиббса
- •Изображение процесса экстракции на 3-х угольной диаграмме
- •Методы экстрагирования
- •Одноступенчатая периодическая экстракция
- •М ногоступенчатая прямоточная экстракция
- •Массопередача в системах с твердой фазой
- •Кинетика массопроводности
- •Сушка. Общие сведения
- •Формы связи влаги с материалом
- •Р авновесие между материалом и жидкостью, находящейся во влажном материале
- •Физические свойства влажного воздуха
- •Материальный баланс сушки.
- •Основная схема конвективной сушки
- •Тепловой баланс процесса конвективной сушки.
- •Кинетика сушки
- •Интенсивность испарения влаги
- •Адсорбция
- •Равновесие при адсорбции
- •Способы кристаллизации
Подобие диффузионных процессов
Уравнение конвективной диффузии математически описывает процесс массопереноса в одной фазе и для вывода критериев подобия оно должно быть дополнено соответствующими условиями, характеризующими массообмен на границе раздела фаз.
При одномерном диффузионном потоке в соответствии с 1-м законом Фика к поверхности раздела фаз будет передано количество вещества:
dM
= - D![]() dFdτ.
По Закону Щукарева: dM
=
dFdτ.
По Закону Щукарева: dM
=
![]() dF
ΔC
d
, отсюда:
dF
ΔC
d
, отсюда:
- D
=![]() .
.
На основе теории
подобия после деления правой части на
левую без учета знаков математических
операций, замены x
на
![]() (определяющий размер) получим:
(определяющий размер) получим:
 - диффузионный
критерий Нуссельта
– характеризует
массообмен на границе фаз и является
аналогом теплового критерия Нуссельта.
- диффузионный
критерий Нуссельта
– характеризует
массообмен на границе фаз и является
аналогом теплового критерия Нуссельта.
Из дифференциального уравнения конвективной диффузии для одномерного случая:
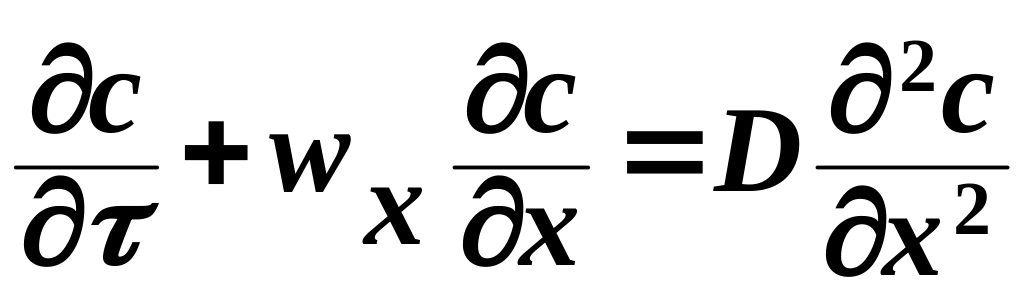 путем
деления правой части уравнения на 1-ое
слагаемое левой части, после преобразований
получаем:
путем
деления правой части уравнения на 1-ое
слагаемое левой части, после преобразований
получаем:
![]() - диффузионный
критерий Фурье,
который характеризует
нестационарный диффузионный процесс.
- диффузионный
критерий Фурье,
который характеризует
нестационарный диффузионный процесс.
Поделив 2-ое слагаемое левой части на правую, получим:
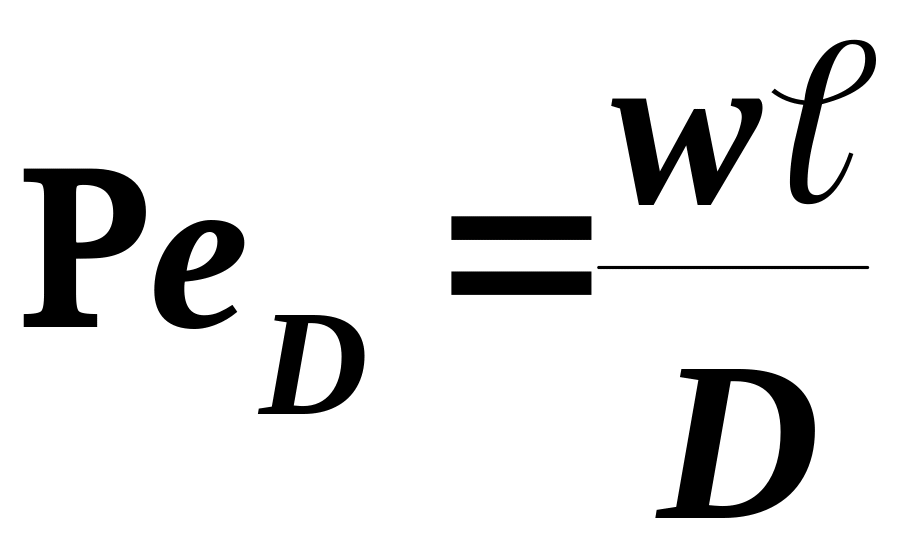 - диффузионный
критерий Пекле,
который характеризует
подобие полей концентраций по длине
пути.
- диффузионный
критерий Пекле,
который характеризует
подобие полей концентраций по длине
пути.
Гидродинамическое
подобие в массообменных аппаратах
характеризуется критерием: Re=![]() ;
;
![]() ,
,
PrD- диффузионный критерий Прандтля, характеризует подобие полей физических величин.
Учитывая, что
критерий NuD
является определяемым, общее критериальное
уравнение конвективной диффузии
записывается следующим образом:
![]() .
.
При вынужденном
движении исключается Gr,
т.к. естественной конвекцией можно
пренебречь, и
![]() или
или
 .
.
Для естественной
конвекции из общего уравнения выпадает
критерий Re:
![]() или
или
 .
.
Значения коэффициентов А, m и n определяются исходя из опытных данных для конкретных случаев диффузионных процессов.
Критерий NuD
вычисляется по полученным критериальным
уравнениям и по нему определяют
![]() :
:
 .
.
Абсорбция
Абсорбция – процесс поглощения газов или паров из газовой или парогазовой смеси жидким поглотителем.
Поглощаемое вещество – абсорбтив, распределен в инертном газе.
Поглотитель – абсорбент (жидкость).
Процесс – избирательный и обратимый. Различают физическую и химическую абсорбцию. Примеры абсорбции: получение Н2S04, аммиачной воды, чистка отходящих газов.
Равновесие при абсорбции
Условия равновесия
– равенство
температур и Р обеих фаз и равновесие
концентраций для всех компонентов в
обеих фазах, которое характеризуется
константой фазового равновесия m.
В общем случае m=f(P,
T,
x).
В большинстве случаев эта функция
находится экспериментально. В системе
газ-жидкость
![]() - закон Генри (
- закон Генри (![]() -
парциальное давление газа над раствором,
Е
– константа Генри, х
– концентрация газа в растворе в мольном
выражении). Е
зависит от природы растворимого газа
и температуры. С ростом температуры
растворимость газов уменьшается.
-
парциальное давление газа над раствором,
Е
– константа Генри, х
– концентрация газа в растворе в мольном
выражении). Е
зависит от природы растворимого газа
и температуры. С ростом температуры
растворимость газов уменьшается.
Согласно закону
Дальтона p=
Py;
сопоставим и получим
![]() ,
,
![]() .
Условия абсорбции улучшаются, если Р
- повысить, а температуру снизить.
.
Условия абсорбции улучшаются, если Р
- повысить, а температуру снизить.
Материальный баланс абсорбции.
Если принять, что
L
и G
постоянны по высоте аппарата, а
концентрации выразить в относительных
массовых концентрациях![]() ,
,
![]() , то G(
, то G(![]() )
= L(
)
= L(![]() -
-![]() ),
отсюда
),
отсюда
 ;
Обозначим
;
Обозначим
 (*), где
(*), где
![]() -
удельный расход абсорбента.
-
удельный расход абсорбента.
(*) – уравнение рабочей линии процесса абсорбции. (*) показывает, что изменение концентрации в абсорбционых аппаратах при L, G = Const по высоте аппарата является линейным. Построим рабочую линию, где
tgα
=
![]() ,
т.е.
различным удельным расходам абсорбента
будут отвечать различные рабочие линии;
точки Ai
лежат на одной и той же горизонтальной
прямой, соответствующей
,
т.е.
различным удельным расходам абсорбента
будут отвечать различные рабочие линии;
точки Ai
лежат на одной и той же горизонтальной
прямой, соответствующей
![]() .
.

