
- •Содержание
- •Введение
- •I. Основные характеристики газового топлива и продуктов его сгорания
- •1.1. Основные термины и понятия
- •Удельное теплосодержание газов, кДж/м3
- •Средняя объемная теплоемкость горючих газов
- •Состав (в % по объему), плотность и теплота сгорания газа основных газовых и газоконденсатных месторождений рф
- •1.2. Состав и основные характеристики газообразного топлива и продуктов его сгорания
- •2. Расчеты горения газового топлива
- •2.1. Теплота сгорания природного газа
- •Теплота сгорания газов
- •2.2. Определение объемов воздуха, расходуемого на горение и продуктов сгорания
- •Основные постоянные компоненты атмосферы земли
- •2.2.1. Подсчет коэффициента избытка воздуха по коэффициенту разбавления продуктов сгорания
- •2.2.2. Подсчет максимального содержания со2max в продуктах сгорания
- •2.3. Температура горения
- •2.4. Методика теплотехнических расчетов потерь теплоты на основе обобщенных характеристик природного газа
- •В окружающую среду для котлов:
- •2.5. Определение потерь теплоты с несконденсировавшимся водяным паром в продуктах сгорания газа
- •Давление насыщенного водяного пара в температурном интервале 30-49°с
- •Значение коэффициентов zв и qун.
- •3. Расчетные характеристики жидкого и твердого углеводородного топлива
- •Литература
2.2. Определение объемов воздуха, расходуемого на горение и продуктов сгорания
Объемы кислорода воздуха и продуктов сгорания подсчитывают исходя из уравнений реакций горения основных компонентов природного газа.
Для составления уравнений горения газов в воздухе необходимо, знать содержание в нем кислорода и других составляющих.
На 1 м3 кислорода в воздухе приходится 3,76 м3 азота и редких газов (табл. 2.2).
Таблица 2.2
Основные постоянные компоненты атмосферы земли
-
Газ
Содержание, %
по массе
по объему
Азот
73,53
78,09
Кислород
23,14
20,94
Аргон
1,28
0,93
Диоксид углерода
0,05
0,035
Неон
1,2 10-3
0,001
Гелий
5,24 10-3
0,001
Криптон
3,3 10-3
0,001
Водород
5 10-3
0,001
Стехиометрическими называют уравнения реакций, в которых отношение количеств исходных веществ строго соответствует условию получения конечных продуктов. Стехиометрические уравнения горения не отражают всех сложных промежуточных явлений процесса, а характеризуют итоговые количественные соотношения.
Уравнения сгорания основных компонентов природного газа в воздухе приведены ниже:
СН4+2О2+7,52N2=СО2+2Н2О+7,52N2; (2.3) С2Н6 +3,5О2 + 13,16N2 = 2СО2 + ЗН2О + 13,16N2; (2.4)
С3Н8 + 5О2+ 18,8N2 = ЗСО2 + 4Н2О + 18,8N2; (2.5)
С4Н10 + 6,5О2 + 24,4N2 = 4СО2 + 5Н2О + 24,4N2; (2.6)
С5Н12 + 8О2 + 3ON2 = 5СО2 + 6Н2О + 30N2. (2.7)
Аналогичным образом составляются уравнения горения продуктов неполного сгорания - СО, Н2:
Н2 + 0,5О2 + 1 ,88N2 = Н20 + 1 ,88N2; (2.8)
СО + 0,5О2 + 1 ,88N2 = СО2 + 1 ,88N2. (2.9)
В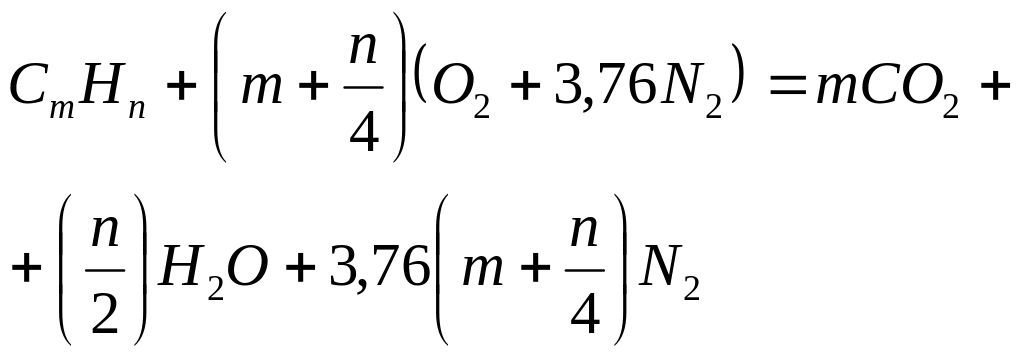 общем виде стехиометрическое уравнение
полного сгорания
смеси углеводородного газа с воздухом
имеет следующий
вид:
общем виде стехиометрическое уравнение
полного сгорания
смеси углеводородного газа с воздухом
имеет следующий
вид:
(2.10)
где m- число атомов углерода в газе;
п - число атомов водорода в газе.
С![]() уммарный
расход кислорода
(м3),
необходимый для сгорания
1 м3
природного газа, подсчитывают по формуле
уммарный
расход кислорода
(м3),
необходимый для сгорания
1 м3
природного газа, подсчитывают по формуле
![]() (2.11)
(2.11)
где СН4, С2Н6 и т.д. - содержание в газе горючих компонентов в процентах по объему.
В соответствии с содержанием в воздухе по объему около 21% кислорода и 79% азота необходимый для полного сгорания газа объем воздуха определяют из выражения:
![]()
![]() , а
объем азота воздуха соответственно
, а
объем азота воздуха соответственно
О![]()
![]()
![]() бъем
двуокиси углерода, образующийся при
сгорании 1
м3
природного газа (м3)
подсчитывают по формуле (2.12),
а объем водяного пара
по
формуле (2.13) (без учета
влаги, содержащейся в воздухе и газе):
бъем
двуокиси углерода, образующийся при
сгорании 1
м3
природного газа (м3)
подсчитывают по формуле (2.12),
а объем водяного пара
по
формуле (2.13) (без учета
влаги, содержащейся в воздухе и газе):
(2.12)
![]() (2.13)
(2.13)
Кроме того, в продуктах сгорания содержится азот, подсчитываемый по формуле
![]() (2.14)
(2.14)
![]()
где - объем азота в исходном горючем газе.
П![]() ри
сжигании газа с избытком воздуха объем
воздуха, расходуемый
в топке, подсчитывают по формуле
ри
сжигании газа с избытком воздуха объем
воздуха, расходуемый
в топке, подсчитывают по формуле
![]() (2.15)
(2.15)
где α - коэффициент избытка воздуха.
При полном сгорании газа с коэффициентом избытка воздуха в продуктах сгорания содержится избыточный кислород в количестве
![]() (2.16)
(2.16)
а![]() содержание азота в продуктах сгорания
возрастает и определяется
по формуле
содержание азота в продуктах сгорания
возрастает и определяется
по формуле
(2.17)
П ри неполном сгорании 1 м3 природного газа объем сухих
п![]() родуктов
сгорания, состоящих из СО2,
СО, СН4,
Н2,
N2
и избыточного О2
(м3)
можно подсчитать по балансу
углерода по формуле
родуктов
сгорания, состоящих из СО2,
СО, СН4,
Н2,
N2
и избыточного О2
(м3)
можно подсчитать по балансу
углерода по формуле
(2.18)
В числителе - углеродосодержащие компоненты природного газа, а в знаменателе - углеродосодержащие компоненты продуктов сгорания по данным газового анализа.
О![]() бъем
водяного пара в продуктах неполного
сгорания природного газа (м3)
можно
подсчитать по формуле
бъем
водяного пара в продуктах неполного
сгорания природного газа (м3)
можно
подсчитать по формуле
(2.19)
Суммарный объем влажных продуктов полного сгорания 1 м3 бессернистого газообразного топлива:
![]()
Объем сухих продуктов сгорания:
![]()
Пример 1. Определить объем воздуха, объем и состав продуктов сгорания при полном сжигании природного газа следующего состава (%): СН4 - 95; С2Н6 - 1; С3Н8 - 0,6; C4H10-0,4; CO2-l;N2-2.
Коэффициент избытка воздуха = 1,1.
Расчет объема кислорода ведем по формуле (2.11):

![]() Состав
сухих продуктов сгорания:
Состав
сухих продуктов сгорания:
![]()
При сжигании газообразного топлива объем сухих продуктов сгорания меньше объема воздуха, израсходованного на горение, а объем влажных продуктов сгорания - больше объема воздуха. Соотношения объемов воздуха и продуктов сгорания газообразного топлива приведены в табл. 2.3.
Таблица 2.3
Соотношение объемов воздуха и продуктов сгорания
Сжигаемый газ
|
, м3 |
, м3 |
, м3 |
|
|
Природный |
8,5 |
9,5 |
10,5 |
0,90 |
0,9 |
Окись углерода |
2,88 |
2,38 |
2,88 |
0,83 |
0,79 |
Водород |
1,88 |
2,38 |
2,88 |
0,83 |
0,79 |
Метан |
8,52 |
9,52 |
10,52 |
0,90 |
0,9 |
Этан |
15,16 |
16,66 |
18,16 |
0,92 |
0,91 |
Пропан |
21,80 |
23,80 |
25,80 |
0,925 |
0,91 |
Бутан |
28,44 |
30,94 |
33,44 |
0,93 |
0,92 |
Пентан |
35,08 |
38,08 |
41,08 |
0,93 |
0,92 |
