
- •1.Эндэргонические и экзэргонические реакции в живой клетке. Макроэргические соединения. Примеры.
- •4. Структура дыхательной цепи. Митохондрии.
- •14. Образование токсических форм кислорода, механизм их повреждающего действия на клетки
- •15.??? 16..Катаболизм основных пищевых веществ - углеводов, жиров, белков. Понятие о специфических путях катаболизма и общих путях катаболизма.
- •23.Основные углеводы животных, их содержание в тканях, биологическая роль. Основные углеводы пищи. Переваривание углеводов
- •1. Этапы аэробного гликолиза
- •32. Аэробный распад глюкозы можно выразить суммарным уравнением:
- •33Челночные механизмы.
- •37.Обмен галактозы. Галактоземии. Нарушения метаболизма галактозы
- •38. Обмен дисахаридов в норме. Нарушения.??? 39. Обмен фруктозы. Нарушения метаболизма фруктозы
- •Глицеральдегид -3 –фосфат
- •40. Свойства и распространение гликогена как резервного полисахарида.
- •43.Распад гликогена
- •48. Особенности обмена глюкозы в разных органах и клетках: эритроциты, мозг, мышцы, жировая ткань, печень.
33Челночные механизмы.
Глицерофосфатный челночный механизм основан на восстановле-нии образующегося при гликолизе фосфодигидроксиацетона (дигидрокси-ацетонфосфата) цитоплазматической глицерофосфатдегидрогеназой (1), использующей восстановленный НАДН, до α-глицерофосфата, который лег-ко проникает через обе мембраны митохондрии в матрикс и на внутренней мембране окисляется с помощью митохондриальной ФАД-зависимой гли-церофосфатдегидрогеназы (2) до дигидроксиацетонфосфата, легко перехо-дящего через мембраны митохондрии в цитозоль клетки. Образующийся ФАДН2 далее через флавинзависимый транспортирующий электроны фер-мент ЕТФ отдает свои электроны и протоны на коэнзим Q (убихинон) в ми-тохондриальную цепь транспорта электронов, где в результате использова-ния 2 моль электронов в процессе окислительного фосфорилирования гене-рируется до 1,5 моль АТФ.
Этот механизм широко используется различными тканями, особенно
печеночной и мышечной тканью, в процессе интенсивной мышечной работы.
Малат-аспартатный челночный механизм является более сложным,
но и более энергосберегающим. Он использует избыток восстановленного
цитоплазматического НАДН в реакции восстановления оксалоацетата (щаве-
левоуксусной кислоты) до малата (яблочной кислоты) с помощью НАД-
зависимого цитоплазматического фермента малатдегидрогеназы Яб-лочная кислота легко проникает в матрикс через обе мембраны митохондрии,
где окисляется митохондриальной также НАД-зависимой, малатдегидро-
геназой (5) до оксалоацетата. Далее электроны от полученного НАДН посту-
пают в цепь транспорта электронов, где в процессе окислительного фофори-
лирования на 2 моль электронов генерируется до 2,5 моль АТФ. Образую-
щийся оксалоацетат не может покинуть митохондрию, он подвергается реак-
ции переаминирования с участием глутаминовой кислоты (глутамата) под
действием митохондриальной аспартатаминотрансферазы (3). В резуль-
тате образуется аспарагиновая кислота (аспартат), которая с помощью спе-
цифической транспортной системы переходит из митохондрии в цитоплазму,
где под действием цитоплазматической аспартатаминотрансферазы (2)
отдает свою аминогруппу α-кетоглутаровой кислоте (α-кетоглутарат), пре-
вращаясь в оксалоацетат. Следует заметить, что α-кетоглутарат и глутамат
легко проникают через внутреннюю мембрану митохондрии используя спе-
циальную ферментную транспортную систему — глутамат-α-кетоглутарат-
транслоказу (1). Внутренняя мембрана митохондрий содержит целый ряд
переносчиков для ионов и заряженных метаболитов: например, переносчик
дикарбоновых кислот опосредует облегченную обменную диффузию малата,
сукцината, фумарата и Н2РО4
–, а переносчики трикарбоновых кислот обеспе-
чивают обмен ОН– и Н2РО4
–. Из наиболее важных транслоказ – ферментов,
осуществляющих специфический транспорт веществ через внутреннюю
мембрану митохондрий необходимо упомянуть АТФ-АДФ-транслоказу,
осуществляющую транспорт в цитоплазму синтезирующейся в митохондриях
АТФ в обмен на поступающие в митохондрию АДФ и неорганический фос-
фат ион, вносящий в митохондрию дополнительный протон. 34. Аллостерические механизмы регуляции аэробного и анаэробного распада глюкозы.???? 35. Пентозофосфатный путь, называемый также гексомонофосфатным шунтом, служит альтернативным путём окисления глюкозо-6-фосфата. Пентозофосфатный путь состоит из 2 фаз (частей) - окислительной и неокислительной.
В окислительной фазе глюкозо-6-фосфат необратимо окисляется в пентозу - рибулозо-5-фосфат, и образуется восстановленный NADPH.
В неокислительной фазе рибулозо-5-фосфат обратимо превращается в рибозо-5-фосфат и метаболиты гликолиза.
Пентозофосфатный путь обеспечивает клетки рибозой для синтеза пуриновых и пиримидиновых нуклеотидов и гидрированным ко-ферментом NADPH, который используется в восстановительных процессах.
Суммарное уравнение пентозофосфатного пути выражается следующим образом:
3 Глюкозо-6-фосфат + 6 NADP+ → 3 СО2 + 6 (NADPH + Н+) + 2 Фруктозо-6-фосфат + Глицеральдегид- 3 -фосфат.
Ферменты пентозофосфатного пути, так же, как и ферменты гликолиза, локализованы в цитозоле.
Наиболее активно Пентозофосфатный путь протекает в жировой ткани, печени, коре надпочечников, эритроцитах, молочной железе в период лактации, семенниках.
Окислительный этап Суммарное уравнение окислительного этапа пентозофосфатного пути можно представить в виде:
Глюкозо-6-фосфат + 2 NADP+ + Н2О → Рибулозо-5-фосфат + 2 NADPH + Н+ + СО2
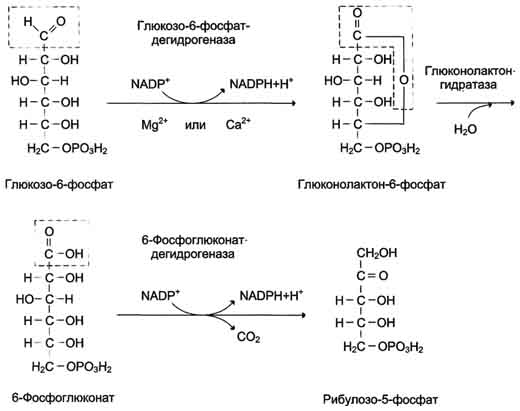 Неокислительный
этап
Неокислительный этап
пентозофосфатного пути включает серию
обратимых реакций, в результате которых
рибулозо-5-фосфат превращается в
рибозо-5-фосфат и ксилулозо-5-фосфат, и
далее за счёт переноса углеродных
фрагментов в метаболиты гликолиза -
фруктозо-6-фосфат и глицеральдегид-3-фосфат.
В этих превращениях принимают участие
ферменты: эпимераза, изомераза,
транскетолаза и трансальдолаза.
Транскетолаза в качестве кофермента
использует тиаминдифосфат. Неокислительный
этап пентозофосфатного пути не включает
реакции дегидрирования
Суммарный
результат метаболизма
3 молекул рибулозо-5-фосфата в неокислительной
фазе пентозофосфатного пути - образование
2 молекул фруктозо-6-фосфата и 1 молекулы
глицеральдегид-3-фосфата. Далее
фруктозо-6-фосфат и глицеральдегид-3-фосфат
могут превратиться в глюкозу. С учётом
стехиометрического коэффициента,
равного 2, для образования 5 молекул
глюкозы (содержащих 30 атомов углерода)
потребуются 4 молекулы фруктозо-6-фосфата
и 2 молекулы глицеральдегид-3-фосфата
(в сумме содержащие также 30 атомов
углерода) или, соответственно, 6 молекул
рибулозо-5-фосфата. Таким образом,
неокислительный путь можно представить
как процесс возвращения пентоз в фонд
гексоз.
36.
Пентозофосфатный цикл
Неокислительный
этап
Неокислительный этап
пентозофосфатного пути включает серию
обратимых реакций, в результате которых
рибулозо-5-фосфат превращается в
рибозо-5-фосфат и ксилулозо-5-фосфат, и
далее за счёт переноса углеродных
фрагментов в метаболиты гликолиза -
фруктозо-6-фосфат и глицеральдегид-3-фосфат.
В этих превращениях принимают участие
ферменты: эпимераза, изомераза,
транскетолаза и трансальдолаза.
Транскетолаза в качестве кофермента
использует тиаминдифосфат. Неокислительный
этап пентозофосфатного пути не включает
реакции дегидрирования
Суммарный
результат метаболизма
3 молекул рибулозо-5-фосфата в неокислительной
фазе пентозофосфатного пути - образование
2 молекул фруктозо-6-фосфата и 1 молекулы
глицеральдегид-3-фосфата. Далее
фруктозо-6-фосфат и глицеральдегид-3-фосфат
могут превратиться в глюкозу. С учётом
стехиометрического коэффициента,
равного 2, для образования 5 молекул
глюкозы (содержащих 30 атомов углерода)
потребуются 4 молекулы фруктозо-6-фосфата
и 2 молекулы глицеральдегид-3-фосфата
(в сумме содержащие также 30 атомов
углерода) или, соответственно, 6 молекул
рибулозо-5-фосфата. Таким образом,
неокислительный путь можно представить
как процесс возвращения пентоз в фонд
гексоз.
36.
Пентозофосфатный цикл
Окислительный этап образования пентоз и неокислительный этап (путь возвращения пентоз в гексозы) составляют вместе циклический процесс.
Такой процесс можно описать общим уравнением:
6 Глюкозо-6-фосфат + 12 NADP+ + 2 Н2О → 5 Глюкозо-6-фосфат + 12 NADPH +12 Н+ + 6 СO2.
Это означает, что из 6 молекул глюкозы образуются 6 молекул рибулозо-5-фосфат (пентозы) и 6 молекул СО2. Ферменты неокислительной
360
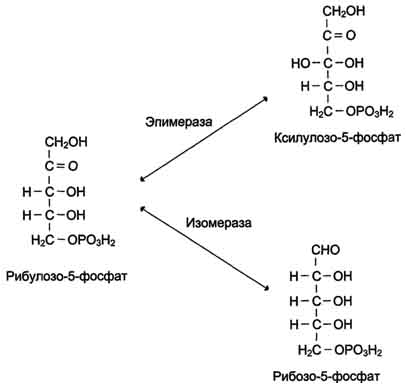
Рис. 7-63. Превращения рибулозо-5-фосфата.
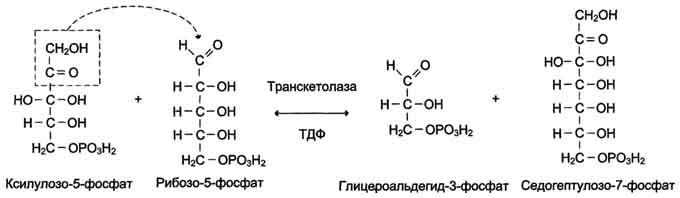
Рис. 7-64. Реакция переноса двухуглеродного фрагмента, катализируемая транскетолазои.
фазы превращают 6 молекул рибулозо-5-фосфат в 5 молекул глюкозы (гексозы). При последовательном проведении этих реакций единственным полезным продуктом является NADPH, образующийся в окислительной фазе пентозофосфатного пути. Такой процесс назьюают пентозофосфатным циклом (рис. 7-67).
Протекание пентозофосфатного цикла позволяет клеткам продуцировать NADPH, необходимый для синтеза жиров, не накапливая пентозы.
Энергия, выделяющаяся при распаде глюкозы, трансформируется в энергию высокоэнергетического донора водорода - NADPH. Гидрированный NADPH служит источником водорода для восстановительных синтезов, а энергия NADPH преобразуется и сохраняется во вновь синтезированных веществах, например
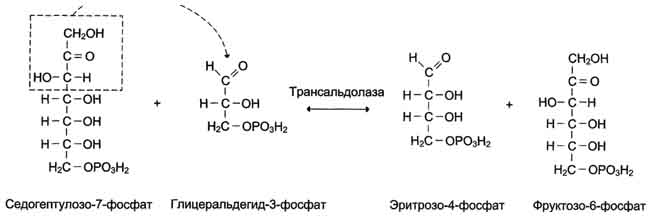
Рис. 7-65. Реакция, катализируемая трансальдолазой.
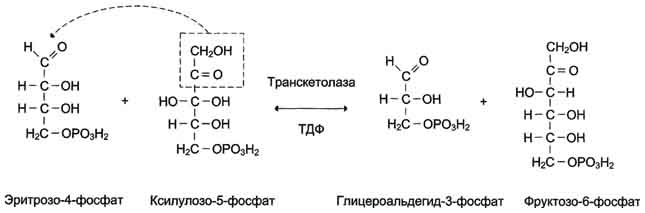
Рис. 7-66. Реакция, катализируемая транскетолазой.
