
- •Кристаллические тела и их особенности;
- •2. Внутренняя энергия идеального газа;
- •Идеальные газы
- •3. Работа в термодинамике;
- •4.Закон кулона;
- •5.Применение первого закона термодинамики к различным процессам;
- •Применение первого закона термодинамики к различным тепловым процессам в идеальном газе
- •6.Электрический ток. Сила тока;
- •Сила и плотность тока
- •7.Потенциал электростатического поля. Разность потенциалов;
- •Разность потенциалов
- •Единица разности потенциалов
- •Связь между напряженностью и напряжением.
- •9.Последовательное соединение ;
- •10.Изобарный процесс;
- •11.Изохорный процесс;
- •12.Параллельные соединения;
- •13.Агрегатные состояния веществ;
- •14.Зависимость сопротивление проводника от температуры;
- •15.Законы Ньютона;
- •16.Первый закон термодинамики;
- •17.Адиабатический процесс;
- •18.Напряженность электрического поля;
- •19.Напряжение;
- •20.Гармонические колебания;
- •21.Вес и невесомость;
- •22.Равноускоренное движение;
- •23.Напряженность электрического поля;
- •24.Закон всемирного тяготения;
- •25.Закон Джоуля - Ленца;
- •26.Закон сохранения энергии;
- •27.Основные положения молекулярно кинетической теории;
- •28.Свойство идеального газа;
- •29.Постоянный электрический ток; Что называют электрическим током?
- •Условия существования постоянного электрического тока.
- •Основные понятия.
- •Законы Ома.
- •Короткое замыкание.
- •Последовательное и параллельное соединение проводников.
- •Правила Кирхгофа.
- •Порядок расчета сложной цепи постоянного тока.
- •Шунты и добавочные сопротивления.
- •30.Уравнение Менделеева – Клапейрона;
- •31.Виды кристаллических структур;
- •32.Механические колебания;
- •33.Работа сил электрического поля;
- •34.Принцып действия тепловой машины;
Кристаллические тела и их особенности;
Кристаллические тела обладают различными свойствами в различных направлениях.
Это явление, называемое анизотропией, объясняется тем, что в кристаллических решетках расстояние между атомами (ионами), а следовательно, и взаимодействие их между собой в различных направлениях неодинаковы; свойства металлов определяются взаимодействием атомов (ионов).
Если взять одиночный кристалл меди (или, как его называют, монокристалл) и вырезать из него образцы в различных направлениях (рис. 4), то свойства таких образцов будут различны.
Прочность может изменяться в 2–2,5 раза, пластичность, т.е. способность деформироваться, — в 5–6 раз, в зависимости от направления, в котором был вырезан образец.
Однако такое различие свойств наблюдается только у монокристаллов.
2. Внутренняя энергия идеального газа;
Вну́тренняя эне́ргия тела (обозначается как E или U) — это сумма энергий молекулярных взаимодействий и тепловых движений молекулы. Внутренняя энергия является однозначной функцией состояния системы. Это означает, что всякий раз, когда система оказывается в данном состоянии, её внутренняя энергия принимает присущее этому состоянию значение, независимо от предыстории системы. Следовательно, изменение внутренней энергии при переходе из одного состояния в другое будет всегда равно разности между ее значениями в конечном и начальном состояниях, независимо от пути, по которому совершался переход.
Внутреннюю энергию тела нельзя измерить напрямую. Можно определить только изменение внутренней энергии:
![]()
где
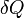 —
подведённое
к телу количество теплоты, измеренное
в джоулях
—
подведённое
к телу количество теплоты, измеренное
в джоулях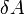 [1] —
работа,
совершаемая телом против внешних сил,
измеренная в джоулях
[1] —
работа,
совершаемая телом против внешних сил,
измеренная в джоулях
Эта формула является математическим выражением первого начала термодинамики
Для квазистатических процессов выполняется следующее соотношение:
![]()
где
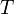 —
температура,
измеренная в кельвинах
—
температура,
измеренная в кельвинах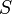 —
энтропия,
измеренная в джоулях/кельвин
—
энтропия,
измеренная в джоулях/кельвин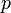 —
давление,
измеренное в паскалях
—
давление,
измеренное в паскалях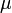 —
химический
потенциал
—
химический
потенциал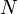 —
количество
частиц в системе
—
количество
частиц в системе
Идеальные газы
Согласно закону
Джоуля, выведенному эмпирически,
внутренняя энергия идеального
газа
не зависит от давления или объёма. Исходя
из этого факта, можно получить выражение
для изменения внутренней энергии
идеального газа. По определению молярной
теплоёмкости
при постоянном объёме,
![]() .
Так как внутренняя энергия идеального
газа является функцией только от
температуры, то
.
Так как внутренняя энергия идеального
газа является функцией только от
температуры, то
![]() .
.
Эта же формула
верна и для вычисления изменения
внутренней энергии любого тела, но
только в процессах при постоянном объёме
(изохорных
процессах);
в общем случае
![]() является
функцией и температуры, и объёма.
является
функцией и температуры, и объёма.
Если пренебречь изменением молярной теплоёмкости при изменении температуры, получим:
![]() ,
,
где
![]() —
количество вещества,
—
количество вещества,
![]() —
изменение температуры.
—
изменение температуры.
3. Работа в термодинамике;
1) одна из форм обмена энергией (наряду с теплотой) термодинамической системы (физического тела) с окружающими телами; 2) количественная характеристика преобразования энергии в физических процессах, зависит от вида процесса; работа системы положительна, если она отдает энергию, и отрицательна, если получает.
