
- •1. Ферменти: визначення; властивості ферментів як біологічних каталізаторів.
- •2. Класифікація та номенклатура ферментів, характеристика окремих класів
- •3. Будова та механізми дії ферментів. Активний та алостеричний (регуляторний) центр.
- •7. Механізми дії та кінетика ферментативних реакцій: залежність швидкості
- •10. Типи інгібування ферментів: зворотнє (конкурентне, неконкурентне) та
- •11. Регуляція ферментативних процесів. Шляхи та механізми регуляції:
- •14. Ензимодіагностика патологічних процесів та захворювань.
- •15. Ензимотерапія – застосування ферментів, їх активаторів та інгібіторів в
- •16. Принципи та методи виявлення ферментів у біооб’єктах. Одиниці виміру
- •Біохімія водо – та жиророзчинних вітамінів
- •2. Вітамін в2: структура, коферментна форма, біологічні властивості, механізм дії, джерела, добова потреба, можливі патології.
- •3. Метаболізм вуглеводів та його регуляція.
- •4. Вітамін в3: структура, кофермента форма, біологічні властивості, механізм
- •5. Вітамін в5: структура, коферментна форма, біологічні властивості, механізм дії, джерела, добова потреба, можливі патології.
- •6. Вітамін в6: структура, коферментна форма, біологічні властивості, механізм дії, джерела, добова потреба, можливі патології.
- •7. Вітамін в12: будова, біологічні властивості, механізм дії, джерела, добова
- •8. Вітамін с: будова, біологічні властивості, механізм дії, джерела, добова
- •9. Вітамін н: будова, біологічні властивості, механізм дії, джерела, добова потреба, можливі патології.
- •10. Вітамін р: будова, біологічні властивості, механізм дії, джерела, добова потреба, можливі патології.
- •13. Вітамін д: будова, біологічні властивості, механізм дії, джерела, добова потреба, можливі патології.
- •14. Вітамін к: будова, біологічні властивості, механізм дії, джерела, добова потреба, можливі патології.
- •Біохімія механізму дії гормонів
- •Основні закономірності обміну речовин. Цикл трикарбонових кислот.
- •1. Обмін речовин (метаболізм) – загальні закономірності протікання катоболічних та анаболічних процесів.
- •5. Субстратне фосфорилювання цтк.
- •Молекулярні основи біоенергетики.
- •1. Реакції біологічного окислення; типи реакцій (дегідрогеназні, оксидазні, оксигеназні) та їх біологічне значення. Тканинне дирхання.
- •2. Флавінзалежні дегідрогенази
- •3. Послідовність компонентів дихального ланцюга мітохондрій. Молекулярні
- •4. Окисне фосфорилювання: пункти спряження транспорту електронів та фосфорилювання, коефіцієнт окисного фосфорилювання.
- •Пункти спряження транспорту електронів та окисного фосфорилювання
- •Ділянки дихального ланцюга мітохондрій, де вивільнення хімічної енергії достатнє для синтезу молекули атф
- •7. Мікросомальне окислення: цитохром р-450; молекулярна організація ланцюга переносу електронів.
- •Обмін вуглеводів
- •3. Аеробне окислення глюкози. Етапи репетворення глюкози до co2 , h2o.
- •4. Окислювальне декарбоксилювання пірувату. Ферменти, коферменти та послідовність реакцій в мультиферментному комплексі.
- •5. Гліколітична оксидоредукція : субстратне фосфорилювання та човникові
- •6. Порівняльна характеристика біоенергетики аеробного та анаеробного окислення глюкози, ефект Пастера.
- •7. Фосфоролітичний шлях розщеплення глікогену в печінці та мязах.
- •8. Біосинтез глікогену: ферментативні реакції, фізіологічне значення.
- •9. Механізми реципрокної регуляції глікогенолізу та глікогенезу за рахунок
- •10. Роль адреналіну, глюкагону та інсуліну в гормональній регуляції обміну
- •11. Генетичні порушення метаболізму глікогену (глікогенози, аглікогенози).
- •12. Глюконеогенез: субстрати , ферменти та фізіологічне значення процесу.
- •13. Глюкозо-лактатний (цикл Корі) та глюкозо-аланіновий цикли.
- •Метаболізм амінокислот. Ензимопатії амінокислотного обміну
- •Амінотрансферазні реакції
- •Окислення біогенних амінів
- •5. Шляхи утворення та знешкодження аміаку в організмі.
- •Генетичні дефекти ферментів синтезу сечовини
- •12. Обмін циклічної амінокислоти триптофану та його спадкові ензимопатії.
7. Механізми дії та кінетика ферментативних реакцій: залежність швидкості
реакції від концентрації субстрату, рН та температури.
Ферментативна кінетика досліджує вплив на швидкість перебігу реакції різних хімічних речовин і фізико-хімічних чинників, які є достатньо численними та різноманітними. До них відносять концентрацію фермента та субстрату, рН і температуру, наявність активаторів або інгібіторів.
Залежність швидкості ферментативної реакції від концентрації субстрату.
Швидкість будь-якої ферментативної реакції залежить від концентрації фермента.
При збільшенні кількості субстрату початкова швидкість зростає і коли фермент повністю насичується субстратом, тобто відбувається максимально можливе утворення фермент-субстратних комплексів, спостерігають найвищу швидкість утворення продукту. Але подальше збільшення концентрації субстрату не призведе до збільшення утворення продукту, оскільки швидкість реакції збільшуватися не буде.
На першій стадії фермент вступає в швидку зворотну взаємодію з субстратом з утворенням фермент-субстратного комплексу (ES), а під час другої стадії, яка відбувається повільніше і лімітує швидкість процесу, комплекс ES розпадається з утворенням продукту реакції (Р) та відновленого стану ферменту
Залежність швидкості ферментативної реакції від температури.
Зростання температури супроводжується прискоренням руху молекул і, відповідно, прискоренням ймовірності взаємодії реагуючих речовин. Крім того, температура може підвищувати енергію реагуючих речовин, що теж прискорює реакцію. Однак, швидкість ферментативної реакції має свій температурний оптимум, перевищення якого супроводжується зниженням ферментативної активності внаслідок термічної денатурації білкових молекул. Зниження температури нижче оптимальної тимчасово сповільнює активність ферменту внаслідок зменшення процесів дифузії молекул.
Залежність швидкості ферментативної реакції від pH середовища.
Відхилення рН від оптимальних величин порушує іонізацію функціональних груп в активному центрі фермента. Зміна рН середовища може також впливати і на просторову організацію субстрату.
8.Кінетика ферментативних реакцій: рівняння Міхаеліса-Ментен.
Константа Міхаеліса – це концентрація субстрату, при якій швидкість дорівнює половині максимальної. Це відношення між сумою констант швидкостей реакцій зворотнього розпаду і розщеплення комплексу з утворенням продуктів реакції та константою швидкості утворення фермент-субстратного комплексу. Вона кількісно визначає спорідненість ферменту із субстратом – чим активніший фермент, тим нижче значення його константи.
Vmax —
максимальна швидкість реакції, яка
спостерігається тоді, коли фермент
повністю насичений субстратом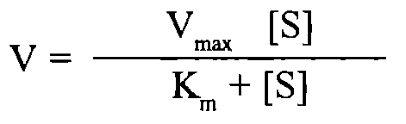
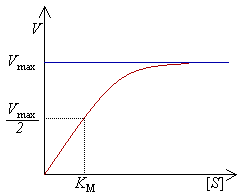
Km — константа Міхаеліса.
Графік залежності початкової швидкості
реакції від концентрації субстрату:
9. Активатори та інгібітори ферментів: приклади та механізми дії.
Активатори - речовини, які підвищують каталітичну активність ферментів. Присутність активатора вкрай важлива для ферменту. До активаторів належать кофактори, іони металів, різноманітні модифікатори тощо.
Активація деяких ферментів може здійснюватися шляхом приєднання до алостеричного центру ферменту якої-небудь специфічної модифікуючої групи, що сприяє змінюванню конформації ферменту і його активного центру. Прикладами можуть бути іони хлору, які є активаторами амілази слини; іони водню, які підвищують активність пепсину; жовчні кислоти, які посилюють дію ліпази підшлункової залози; лужна фосфатаза може активуватися катіонами.
Інгібітори - хімічні сполуки, що зменшують каталітичну активність ферментів. Навідміну від речовин, які інактивують ферменти за рахунок їх денатурації (концентровані кислоти та луги, солі важких металів у високих концентраціях), дія інгібіторів є специфічною стосовно певних ферментів або груп ферментів, вони мають низьку концентрацію.
Наприклад малонова кислота,яка протидіє звязуванню активним центром ферменту сукцинат-дегідрогенази справжнього субстрату-сукцинату.
