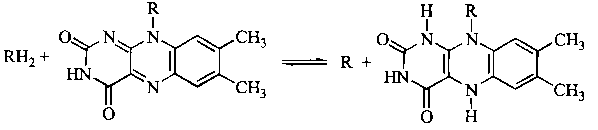- •1. Ферменти: визначення; властивості ферментів як біологічних каталізаторів.
- •2. Класифікація та номенклатура ферментів, характеристика окремих класів
- •3. Будова та механізми дії ферментів. Активний та алостеричний (регуляторний) центр.
- •7. Механізми дії та кінетика ферментативних реакцій: залежність швидкості
- •10. Типи інгібування ферментів: зворотнє (конкурентне, неконкурентне) та
- •11. Регуляція ферментативних процесів. Шляхи та механізми регуляції:
- •14. Ензимодіагностика патологічних процесів та захворювань.
- •15. Ензимотерапія – застосування ферментів, їх активаторів та інгібіторів в
- •16. Принципи та методи виявлення ферментів у біооб’єктах. Одиниці виміру
- •Біохімія водо – та жиророзчинних вітамінів
- •2. Вітамін в2: структура, коферментна форма, біологічні властивості, механізм дії, джерела, добова потреба, можливі патології.
- •3. Метаболізм вуглеводів та його регуляція.
- •4. Вітамін в3: структура, кофермента форма, біологічні властивості, механізм
- •5. Вітамін в5: структура, коферментна форма, біологічні властивості, механізм дії, джерела, добова потреба, можливі патології.
- •6. Вітамін в6: структура, коферментна форма, біологічні властивості, механізм дії, джерела, добова потреба, можливі патології.
- •7. Вітамін в12: будова, біологічні властивості, механізм дії, джерела, добова
- •8. Вітамін с: будова, біологічні властивості, механізм дії, джерела, добова
- •9. Вітамін н: будова, біологічні властивості, механізм дії, джерела, добова потреба, можливі патології.
- •10. Вітамін р: будова, біологічні властивості, механізм дії, джерела, добова потреба, можливі патології.
- •13. Вітамін д: будова, біологічні властивості, механізм дії, джерела, добова потреба, можливі патології.
- •14. Вітамін к: будова, біологічні властивості, механізм дії, джерела, добова потреба, можливі патології.
- •Біохімія механізму дії гормонів
- •Основні закономірності обміну речовин. Цикл трикарбонових кислот.
- •1. Обмін речовин (метаболізм) – загальні закономірності протікання катоболічних та анаболічних процесів.
- •5. Субстратне фосфорилювання цтк.
- •Молекулярні основи біоенергетики.
- •1. Реакції біологічного окислення; типи реакцій (дегідрогеназні, оксидазні, оксигеназні) та їх біологічне значення. Тканинне дирхання.
- •2. Флавінзалежні дегідрогенази
- •3. Послідовність компонентів дихального ланцюга мітохондрій. Молекулярні
- •4. Окисне фосфорилювання: пункти спряження транспорту електронів та фосфорилювання, коефіцієнт окисного фосфорилювання.
- •Пункти спряження транспорту електронів та окисного фосфорилювання
- •Ділянки дихального ланцюга мітохондрій, де вивільнення хімічної енергії достатнє для синтезу молекули атф
- •7. Мікросомальне окислення: цитохром р-450; молекулярна організація ланцюга переносу електронів.
- •Обмін вуглеводів
- •3. Аеробне окислення глюкози. Етапи репетворення глюкози до co2 , h2o.
- •4. Окислювальне декарбоксилювання пірувату. Ферменти, коферменти та послідовність реакцій в мультиферментному комплексі.
- •5. Гліколітична оксидоредукція : субстратне фосфорилювання та човникові
- •6. Порівняльна характеристика біоенергетики аеробного та анаеробного окислення глюкози, ефект Пастера.
- •7. Фосфоролітичний шлях розщеплення глікогену в печінці та мязах.
- •8. Біосинтез глікогену: ферментативні реакції, фізіологічне значення.
- •9. Механізми реципрокної регуляції глікогенолізу та глікогенезу за рахунок
- •10. Роль адреналіну, глюкагону та інсуліну в гормональній регуляції обміну
- •11. Генетичні порушення метаболізму глікогену (глікогенози, аглікогенози).
- •12. Глюконеогенез: субстрати , ферменти та фізіологічне значення процесу.
- •13. Глюкозо-лактатний (цикл Корі) та глюкозо-аланіновий цикли.
- •Метаболізм амінокислот. Ензимопатії амінокислотного обміну
- •Амінотрансферазні реакції
- •Окислення біогенних амінів
- •5. Шляхи утворення та знешкодження аміаку в організмі.
- •Генетичні дефекти ферментів синтезу сечовини
- •12. Обмін циклічної амінокислоти триптофану та його спадкові ензимопатії.
5. Субстратне фосфорилювання цтк.
Субстратне фосфорилювання - процес синтезу АТФ, що в біологічних системах відбувається внаслідок розщеплення субстратів без участі дихального ланцюга мітохондрій. У цьому разі перетворення субстрату в продукт реакції супроводжується фосфорилюванням АДФ з утворенням АТФ.
Реакція, яку каталізує сукцинаттіокіназа (сукциніл-КоА синтеза), є єдиною реакцією циклу, що супроводжується генерацією високоенергетичного фосфатного зв’язку на субстратному рівні
З субстратів ГДФ та Фн відбувається утворення ГТФ, який під дією фосфокінази вступає в реакцію з АДФ з утворенням АТФ:
ГТФ + АДФ → АТФ + ГДФ.
Молекулярні основи біоенергетики.
1. Реакції біологічного окислення; типи реакцій (дегідрогеназні, оксидазні, оксигеназні) та їх біологічне значення. Тканинне дирхання.
В даний час біологічне окислення визначається як сукупність реакцій окислення органічних речовин (субстратів), що виконують функцію енергетичного забезпечення потреб організму. Окислення субстратів в біохімічних системах супроводжується відщепленням електронів від субстратів (донор електронів), які за участю проміжних переносників передаються на кисень - кінцевий (термінальний) акцептор електронів у аеробних організмів. Транспорт високоенергетичних електронів відновлених субстратів відбувається в складній системі, що складається з окислювально-відновних ферментів і коферментів, локалізованих у внутрішній мембрані мітохондрії.
Ферменти, що каталізують окислювально-відновні реакції, називають оксидоредуктазами
1) Оксидази. Справжні оксидази каталізують видалення водню з субстрату, використовуючи при цьому якості акцептора водню тільки кисень. Вони незмінно містять мідь, продуктом реакції є вода (виняток становлять реакції, що каталізуютьсямоноаміноксидазою, в результаті яких утворюється Н2О2).
2) Аеробні дегідрогенази-ферменти, що каталізують видалення водню з субстрату; на відміну від оксидаз вони можуть використовувати в якості акцептора водню не тільки кисень, але і штучні акцептори, такі, як метиленовий синій. Ці дегідрогенази відносяться до флавопротеїнів, і продуктом каталізуючої ними реакції є перекис водню, а не вода.
3) Анаеробні дегідрогенази-ферменти, що каталізують видалення водню з субстрату, але не здатні використовувати кисень в якості акцептора водню. У цей клас входить велика к-ть ферментів. Вони виконують дві головні функції.
-
Перенесення водню з одного субстрату на інший в сполученої окислювально-відновної реакції. Ці дегідрогенази специфічні до субстратів, але часто використовують один і той же кофермент або переносник водню.
-
Функцію компонентів дихального ланцюга, що забезпечують транспорт електронів від субстрату на кисень.
4) оксигенази - ферменти, що каталізують пряме введення кисню в молекулу субстрату.
Окислювальним фосфорилюванням називають поєднання двох клітинних процесів: екзергонічні реакції окислення відновлених молекул (НАДН + Н + або ФАДН2) і ендергонічні реакції фосфорилювання АДФ і утв АТФ.
2. Ферменти біологічного окислення в мітохондріях: піридин-, флавін- залежні дегідрогенази, цитохроми.
1. Дегідрогенази, залежні від нікотинамідних коферментів (НАД(Ф)-залежні дегідрогенази).
Коферментами цих дегідрогеназ є нуклеотиди НАД або НАДФ, у структурі молекул яких міститься похідна піридину - нікотинамід. Зв'язок між НАД (або НАДФ) та білковою частиною ферменту (апоферментом) у складі піридинзалежних дегідрогеназ нестійкий: він утворюється та руйнується в процесі каталітичного циклу, що дозволяє вважати нікотинамідні нуклеотиди скоріше субстратами, ніж простетичними групами.
Активною
структурою в молекулі НАД або НАДФ, що
акцептує відновлювальні еквіваленти
від субстрату, є піридинове кільце
никотинаміду. У ході ферментативної
реакції субстрат відщеплює два атоми
водню (2Н++
2е-),
один з яких у формі гідридіона: Н-
(тобто Н+
+ 2е-)
приєднується до піридинового кільця
НАД(Ф), а другий у вигляді протона (іона
Н+)
надходить у реакційне середовище.
Дегідрогенази, залежні від нікотинамідних
коферментів, дуже поширені в живих
клітинах. Вони виконують функції
анаеробних дегідрогеназ, що відщеплюють
протони та електрони від багатьох
субстратів, відновлюючи НАД або НАДФ,
які передають в подальшому відновлювальні
еквіваленти на інші акцептори. НАД-залежні
дегідрогенази - ці ферменти каталізують
окислювально-відновлювальні реакції,
що містяться на окислювальних шляхах
метаболізму - гліколізу, циклу лимонної
кислоти, β-окислення жирних кислот,
окисного дезамінування амінокислот,
дихального ланцюга мітохондрій.
НАДФ-залежні дегідрогенази - ці ферменти
беруть участь у процесах відновлювального
синтезу, що відбуваються в цитозолі,
зокрема постачають атоми водню при
синтезі жирних кислот та стероїдів.
Головним джерелом відновленого НАДФ є
дегідрогеназні реакції пентозофосфатного
шляху окислення глюкози.