
18.2.6-стом-укр-протокол
.docЗаняття 6 СТОМ. Дослідження біологічного окислення. Тканинне дихання та окисне фосфорилювання.
Цілі заняття:
-
Пояснювати механізми спряження біологічного окислення та окисного фосфорилювання – синтезу АТФ;
-
Аналізувати структурно-функціональні особливості функціонування дихального ланцюга, що забезпечують ефективний синтез – АТФ;
-
Пояснювати основні засади хеміоосмотичної теорії окисного фосфорилювання;
-
Аналізувати дію інгібіторів і роз `єднувачів окисного фосфорилювання природного та синтетичного походження, їх фізіологічне значення.
Теоретичні питання для самопідготовки до заняття:
-
Окисне фосфорилювання і синтез АТФ в мітохондріях:
-
шляхи утворення АТФ в клітинах – субстратне та окисне фосфорилювання;
-
спряження дихання та окисного фосфорилювання;
-
ділянки утворення АТФ в дихальному ланцюзі;
-
коефіцієнт окисного фосфорилювання, його значення при окисленні різних субстратів у мітохондріях;
-
пункти спряження транспорту електронів та окисного фосфорилювання.
-
Хеміосмотична теорія окисного фосфорилювання, її унікальність та спільність принципів генерації енергії в різних живих системах.
-
Структурно-функціональні передумови ефективного спряження транспорту електронів в дихальному ланцюгу та синтезу АТФ:
-
специфічна асиметрична локалізація компонентів ланцюга транспорту електронів у внутрішній мембрані мітохондрій;
-
цілісність спрягаючих мембран мітохондрій;
-
генерація електрохімічного градієнта протонів на мембрані;
-
функціонування протонних помп дихального ланцюга;
-
наявність АТФ-синтетази – ферменту, що використовує енергію електрохімічного градієнта протонів для синтезу АТФ.
-
Схема хеміосмотичного механізму спряження транспорту електронів в дихальному ланцюзі з синтезом АТФ.
-
Молекулярна будова та принцип дії АТФ-синтетази.
-
Інгібітори транспорту електронів в дихальному ланцюгу мітохондрій.
-
Інгібітори окисного фосфорилювання в дихальному ланцюгу мітохондрій.
-
Роз`єднувачі транспорту електронів та окисного фосфорилювання в дихальному ланцюгу мітохондрій.
-
Фізіологічно активні сполуки - роз`єднувачі транспорту електронів та окисного фосфорилювання в дихальному ланцюгу мітохондрій.
-
Роль роз`єднувачів транспорту електронів та окисного фосфорилювання у регуляції термогенезу в організмі людини і тварин.
Зміст теми
Комплекси дихального ланцюга:
I комплекс – НАДН-дегідрогеназа (НАДН-убіхінон оксидоредуктаза) має дві функції: окислює НАДН.Н+ - переносить від нього 2 електрони на убіхінон та транспортує 4Н+ з матриксу у міжмембранний простір.
II комплекс – сукцинатдегідрогеназа (сукцинат-убіхінон оксидоредуктаза) забезпечує додатковий шлях для входу електронів у дихальний ланцюг за рахунок окиснення сукцинату.
III комплекс – цитохром с редуктаза (убіхінон-цитохром с оксидоредуктаза) містить цитохроми b та c1, транспортує 2 електрони з убіхінону на цитохром с та забезпечує викачування 4 протонів з матриксу в міжмембранний простір.
IV комплекс – цитохром с оксидаза містить цитохроми а та а3, транспортує 2 електрони на кисень та одночасно переносить 2 протони в міжмембранний простір.
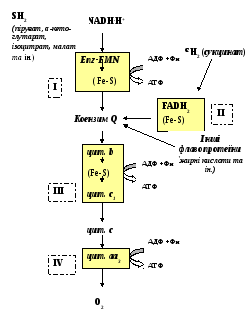
Інгібітори дихального ланцюга. Робота дихального ланцюга може бути інгібована під дією різноманітних клітинних отрут, які взаємодіють з білками-переносниками та порушують транспорт електронів:
-
Інгібітори I комплексу — барбітурати (амітил, секонал), ротенон, пієрицидин А.
-
Інгібітор II комплексу — малонат.
-
Інгібітор III комплексу — антиміцин А.
-
Інгібітори IV комплексу — Н2S, цианіди, СО.
Наявність у клітині вказаних інгібіторів призводить до розвитку гіпоенергетичного стану, що, в свою чергу, в деяких випадках може призвести до загибелі клітини.
Хеміосмотична теорія Мітчелла (теорія окисного фосфорилювання)
Пояснення механізмів спряження роботи дихального ланцюга та синтезу АТФ було запропоноване англійським біохіміком Пітером Мітчеллом у 1961 році.
Основними постулатами теорії Мітчелла є:
-
внутрішня мембрана мітохондрій непроникна для іонів та малих молекул (за винятком молекул води);
-
дихальний ланцюг працює як «помпа», що викачує протони з матриксу в міжмембранний простір – рух 2 електронів від субстрату на кисень призводить до перенесення 8-10 Н+ (протони транспортуються через I, III та IV комплекси) через мембрану;
-
робота дихального ланцюга створює електрохімічний градієнт протонів (∆μН+), оскільки вони вільно через внутрішню мітохондріальну мембрану повернутися в матрикс не можуть і будуть накопичуватись у міжмембранному просторі; ∆μН+ - це проміжна форма зберігання енергії окиснення субстратів;
-
енергію протонного градієнта використовує Н+-АТФ- синтаза (V комплекс) для синтезу АТФ, коли через одну з її субодиниць протони повертаються в матрикс;
-
існують сполуки - роз’єднувачі окисного фосфорилю-вання, які порушують електрохімічний градієнт протонів і знижують ефективність роботи Н+-АТФ-синтази.
Інгібітори та роз’єднувачі окисного фосфорилювання
Крім 2,4-динітрофенолу до синтетичних роз’єднувачів потрібно віднести деякі похідні вітаміну К, анестетики, антибіотики валіноміцин та граміцидин, ацетилсаліцилову кислоту, гербіциди. До природних роз’єднувачів належать продукти перекисного окиснення ліпідів, довголанцюгові жирні кислоти, великі дози тиреоїдних гормонів.
Завдання для самостійної роботи:
Зобразіть у вигляді схеми дихальний ланцюг мітохондрій та укажіть на ньому:
-
Місце розташування та будову АТФ-азного комплексу.
-
Пункти спряження транспорту протонів через мембрану та фосфорилювання
-
Місця ігнібірування дихально ланцюга ротеноном, ціанідами, аміталом та антиміцином.
Завдання для самоконтролю:
-
У чому полягає суть хеміоосмотичної теорії окисного фосфорилювання.
-
Який механізм дії ферментної системи – протонної АТФази.
-
Поясніть, як підтримується температура тіла теплокровних організмів при охолодженні?
-
Яку роль у новонародженних відіграє бурий жир для підтримання температури тіла?
-
Опишіть механізм дії роз`єднувачів окисного фосфорилювання.
-
Який механізм токсичної дії сірководня на організм?
-
Ротенон, механізм його дії на електронний транспорт.
-
В якій формі звільняється енергія при роз`єднанні окисного фосфорилювання?
-
Як зміниться коефіцієнт АДФ/О та дихальний контроль при додаванні до інтактних мітохондрій 2,4-динітрофенолу?
-
Поясніть механізм дії на електронний транспорт монооксиду вуглецю.
Практична робота
Частина 1
Завдання 1. Визначення активності ФАД-залежної сукцинат-дегідрогенази – компонента дихального ланцюга мітохондрій.
Принцип методу. Сукцинатдегідрогеназа каталізує дегідрогенізацію сукцинату (янтарної кислоти), в результаті чого утворюється фумарат (фумарова кислота). Кофактором ферменту є ФАД, який відновлюється в процесі реакції до ФАДН2. Утворений в реакції ФАДН2 відновлює метиленовий синій та перетворює її в безбарвну лейкосполуку.
Хід роботи. Дві пробірки – контрольну та дослідну заповнюють реактивами за таблицею:
|
Вміст пробірок |
Пробірка |
|
|
Контрольна |
Дослідна |
|
|
Фосфатний буфер, рН = 7,4 |
1,0 мл |
1,0 мл |
|
Розчин янтарної кислоти |
1,0 мл |
1,0 мл |
|
Суспензія мітохондрій |
--- |
0,5 мл |
|
Суспензія мітохондрій після кип’ятіння |
0,5 мл |
--- |
|
Метиленовий синій |
0,5 мл |
0,5 мл |
|
Інкубація в термостаті при 37оС |
||
|
Результати: час, протягом якого відбувається знебарвлення розчину |
|
|
За результатами проведеного експерименту зробити висновки.
ВИСНОВОК:
Завдання 2. Визначення активності цитохромоксидази– компонента дихального ланцюга мітохондрій.
Принцип методу. Цитохроми – складні білки гемпротеїни, відносяться до класу ферментів– оксидо-редуктаз, присутні у всіх тваринних та рослинних клітинах. Завдяки тому, що атоми заліза в цитохромах легко змінюють свою валентність, цитохроми є компонентами дихального ланцюга мітохондрій та переносниками електронів від відновленого убіхінону на кисень. В цитохромній системі передавати електрони на кисень може лише цитохром а-а3 – цитохромоксидаза в склад якої входить мідь.
Метод визначення активності цитохромоксидази ґрунтується на здатності диметилпарафенілендіамінхлориду (ДПФД) бути донором електронів для цитохрому с. ДПФД неферментативно відновлює цитохром с, а сам окислюючись, перетворюється на червоний пігмент, кількісне утворення якого є пропорційним активності цитохромоксидази мітохондрій.
Хід роботи. Дві пробірки: контрольну та дослідну заповнюють реактивами за таблицею:
|
Вміст пробірок |
Пробірка |
|
|
Контрольна |
Дослідна |
|
|
Фосфатний буфер, рН = 7,4 |
1,0 мл |
1,0 мл |
|
Розчин цитохрому с |
2 краплі |
2 краплі |
|
Суспензія мітохондрій |
0,5 мл |
0,5 мл |
|
Розчин ДПФД |
0,5 мл |
0,5 мл |
|
Етиловий спирт |
1,0 мл |
--- |
|
Фізіологічний розчин |
--- |
1,0 мл |
|
Інкубація в термостаті 5 хв. при 37оС |
||
|
Результати: поява червоного забарвлення |
|
|
Додавання етилового спирту інактивує цитохромоксидазу та ферментативне перетворення цитохрому с.
Пробірки поміщають в термостат на 5 хвилин при 37оС і спостерігають за появою червоного забарвлення.
За результатами проведеного експерименту зробити висновки.
ВИСНОВОК:
Частина 2
Завдання 1. Вивчення окисного фосфорилювання в мітохондріях та дії роз’єднувача – 2,4-динітрофенолу на цей процес.
Принцип методу. В процесі окислення різних субстратів і передачі електронів в дихальному ланцюгу мітохондрій вивільняється енергія. Частина цієї енергії використовується для синтезу АТФ в процесі окисного фосфорилювання:
АДФ + Фн АТФ
В експерименті, щоб запобігти нагромадженню АТФ (високий вміст АТФ інгібує ферменти дихального ланцюга) в якості кінцевого акцептора неорганічного фосфату використовують глюкозу. Фосфорилювання глюкози за участю АТФ каталізує фермент – гексокіназа:
Глюкоза + АТФ АДФ + глюкозо-6-фосфат
Визначення неорганічного фосфату ґрунтується на здатності молібдату амонію в кислому середовищі приєднувати залишок фосфорної кислоти з утворенням фосфату амонію. Фосфат амонію під дією відновника – аскорбінової кислоти утворює продукти забарвлені в синій колір. В процесі окисного фосфорилювання Фн вилучається з інкубаційного середовища, а тому інтенсивність синього забарвлення розчину зменшується.
Роз’єднувачі – це сполуки які порушують спряженість окислення і фосфорилювання в мітохондріях. В присутності роз’єднувачів спостерігається активне поглинання кисню мітохондріями, однак швидкість генерації АТФ – значно зменшується (або відсутня). Згідно з хеміосмотичною теорією, роз’єднувачі спричиняють втрату мембраною електрохімічного протонного потенціалу – рушійної сили генерації макроергічних зв’язків АТФ.
Хід роботи. Три пробірки– контрольну, дослідну №1 та дослідну №2 заповнюють реактивами за таблицею:
|
Вміст пробірок |
Пробірки |
||
|
Контроль |
Дослід №1 |
Дослід №2 |
|
|
Суміш № 1 (КН2РО4, KCl, MgCl2, КОН - рН = 7,4) |
1,0 мл |
1,0 мл |
1,0 мл |
|
Суміш № 2 (водний розчин глюкози з АТФ) |
0,5 мл |
0,5 мл |
0,5 мл |
|
Гексокіназа |
0,5 мл |
0,5 мл |
0,5 мл |
|
Сукцинат калію |
0,5 мл |
0,5 мл |
0,5 мл |
|
2,4-динітнофенол |
--- |
--- |
2 краплі |
|
Суспензія мітохондрій |
--- |
0,5 мл |
0,5 мл |
|
Суспензія мітохондрій після кип’ятіння |
0,5 мл |
--- |
--- |
|
Розчин оцтової кислоти |
2 краплі |
--- |
--- |
|
Інкубація в термостаті 15 хв. при температурі 37оС |
|||
|
Розчин ТХО |
1,0 мл |
1,0 мл |
1,0 мл |
|
Молібдат амонію |
0,5 мл |
0,5 мл |
0,5 мл |
|
Аскорбінова кислота |
0,5 мл |
0,5 мл |
0,5 мл |
|
Результати: спостерігають за появою синього забарвлення протягом 20 хвилин |
|
|
|
Оцтова кислота додається для повноти денатурації білка в контрольній пробірці. Після інкубації в термостаті протягом 15 хв. при 37оС в кожну пробірку додають по 1,0мл розчину ТХО; по 0,5мл розчину молибдата амонію та по 0,5мл розчину аскорбінової кислоти. Протягом 20 хвилин спостерігають за появою синього забарвлення.
За результатами проведеного експерименту зробити висновки.
ВИСНОВОК:
Клініко-діагностичне та практичне значення.
Коефіцієнт окисного фосфорилювання – відношення кількості зв’язаного (етерифікованого) неорганічного фосфату до кількості поглинутого мітохондріями кисню позначається як Pi/О (Фн/О). Коефіцієнт кількісно дорівнює числу молекул АТФ, що утворюються при перенесенні двох відновлювальних еквівалентів на один атом кисню, тобто АТФ/О. При окисленні субстратів НАД-залежними дегідрогеназами коефіцієнт складає– 3, а для ФАД-залежних дегідрогеназ – 2.
Коефіцієнт окисного фосфорилювання використовується з метою характеристики ефективності процесів енергопродукції в тканинах в нормі та при патології. Порушення синтезу АТФ спостерігається в умовах дії на організм людини і тварин багатьох патогенних факторів хімічного (зокрема, природні та синтетичні токсини, лікарські засоби, тощо), біологічного (гормони, антибіотики, проміжні продукти метаболізму) та фізичного (іонізуюча радіація) походження. Всі вони спричиняють роз’єднання дихання та окисного фосфорилювання за рахунок порушення здатності створювати та підтримувати електрохімічний протонний потенціал на спрягаючи мембранах мітохондрій.
Роз’єднувачами окисного фосфорилювання є сполуки природного та синтетичного походження. Природні роз’єднувачі – вищі жирні кислоти, гормони щитовидної залози (тироксин, трийодтиронін), прогестерон, жовчні кислоти, деякі антибіотики. Синтетичні роз’єднувачі – 2,4-динітрофенол та близькі до нього за хімічною будовою динітрокрезол, пентахлорфенол, а також синтетична сполука– карбоціанід-м-хлорфенілгідразон, що в 100 разів перевищує за специфічною активністю 2,4-динітрофенол.
Українська й англійська термінологія
|
Біологічне окислення це процес окислення біологічних речовин з виділенням енергії. |
Biological oxidation is the process of oxidation of biological substances with the release of energy. |
|
Тканинне дихання - процес поглинання кисню (О2) тканинами при окисленні органічного субстрату з виділенням вуглекислого газу (СО2) і води (Н2О). |
Tissue respiration is the process of absorbing oxygen (O2) by tissues during the oxidation of an organic substrate with the release of carbon dioxide (CO2) and water (H2O). |
|
Окислювальне фосфорилювання це синтез АТФ пов'язаний з тканинним диханням. |
Oxidative phosphorylation is the synthesis of ATP coupled to tissue respiration. |
|
Макроергічні сполуки - це речовини, що містять багаті енергією зв'язку. |
Macroergic compounds are substances containing energy-rich bonds. |
|
Дихальний ланцюг - це система ферментів і коферментів, які беруть участь в транспорті електронів і протонів від окисляемого субстрату до кисню. |
The electron transport chain (ETC) is a system of enzymes and coenzymes that take part in the transport of electrons and protons from the oxidized substrate to oxygen. |
|
Редокс-потенціал (РОП) - це величина електричного заряду, який створюється між платиновими електродами, поміщеними в розчин, що містить окислену і відновлену форму речовини. |
The redox potential (ROP) is the magnitude of the electric charge that is created between the platinum electrodes placed in a solution containing the oxidized and reduced form of the substance. |
|
Коефіцієнт окисного фосфорилювання (Р / О) цей число молекул неорганічного фосфату (Фн), яке перейшло в органічну форму (в форму АТФ) в розрахунку на кожен поглинений атом кисню |
The coefficient of oxidative phosphorylation (P / O) is the number of molecules of inorganic phosphate (FN) that has passed into the organic form (in the form of ATP) per each absorbed oxygen atom |
Рекомендована література.
Основна:
-
Губський Ю.І. Біологічна хімія. – Київ –Тернопіль: Укрмедкнига, 2000. – 508 с.
-
Методичні розробки практичних занять з біологічної хімії. Практикум. За редакцією д. мед. н., професора Ю.В. Хмелевського. – Київ: НМУ. – 1985. – 204 с.
-
Обмін речовин та його показники. Методичні розробки практичних занять з біологічної хімії. – Київ: НМУ. – 1992.– 36 с.
Додаткова:
-
Гонський Я.І., Максимчук Т.П., Калинський М.І., Біохімія людини. Підручник. – Тернопіль: Укрмедкнига, 2002. – 744 с.
-
Ленинджер А. Основы биохимии. В 3 т.– М.: Мир. 1985. – 1056 с.
-
Марри Р., Греннер Д., Мейес П., Родуєлл В. Биохимия человека: В 2 т.– М.: Мир, 1993. т.1. – 381 с.
