
- •Часть 1. Тема 1: Основные положения спектроскопии
- •1.1. Основные квантовые законы (постулаты Бора)
- •1.2. Уровни энергии и переходы между ними.
- •1.2.1. Спектр атома водорода
- •1.3. Спектры поглощения, испускания и рассеивания
- •1.3.1. Оптическое возбуждение
- •1.3.2. Комбинационное рассеивание
- •1.3.3. Электрические способы возбуждения
- •1.4. Деление спектроскопии по свойствам излучения
- •1.4.1. Предмет и задачи спектроскопии
- •1.4.2. Деление спектроскопии по свойствам электромагнитного излучения
- •1.5. Деление спектроскопии по свойствам атомных систем
- •1.6. Типы уровней атомов и молекул
- •Тема 2: Спектроскопические методы анализа
- •2.1. Классификация типов спектрального анализа.
- •2.2. Деление спектроскопии по методам: некоторые особенности проведения анализа
- •2.3. Деление спектрального анализа по решаемым задачам: некоторые особенности проведения
- •2.3.1. Элементный спектральный анализ
- •2.3.2. Изотопный спектральный анализ.
- •2.3.3. Молекулярный спектральный анализ
- •Абсорбционный анализ по спектрам поглощения
- •Эмиссионный молекулярный спектральный анализ
- •2.3.4. Анализ структурных элементов сложных молекулярных соединений
- •1. Структурный анализ в уф и видимой областях
- •2. Спектральный структурный анализ в ик области
- •3. Структурный анализ по спектрам комбинационного рассеивания
- •2.4. Общие схемы проведения спектрального анализа
- •2 .4.1. Эмиссионный спектральный анализ
- •2.4.2. Абсорбционный спектральный анализ
- •2.5. Основные характеристики и области применения спектрального анализа
- •Часть 2: Атомная спектроскопия. Тема 3. Уровни энергии и спектры атома водорода и водородоподобных ионов.
- •3.1. Квантовые числа одноэлектронного атома и степень вырождения его уровней.
- •3.2. Невырожденные и вырожденные уровни энергии. Вырождение уровней одноэлектронного атома.
- •3.3. Правила отбора для одноэлектронных атомов.
- •3.4. Тонкая структура уровней энергии и спектральных линий.
- •3.5. Зависимость спектров одноэлектронных атомов от заряда и массы ядра.
- •3.6. Характеристика стационарных состояний одноэлектронного атома.
- •Тема 4. Электронные оболочки атомов и периодическая система элементов.
- •4.1. Квантовые числа электронов в сложном атоме и принцип Паули.
- •4.2. Электронные слои и оболочки и их заполнение.
- •4.3. Зависимость энергии электронов от орбитального кв. Числа.
- •4.4. Свойства элементов с заполненными и незаполненными оболочками.
- •4.5. Типы спектров различных элементов.
- •Тема 5: Основы общей систематики сложных спектров.
- •5.1. Сложение орбитальных и спиновых моментов и типы связи.
- •5.2. Общая характеристика нормальной связи.
- •Тема 6: Рентгеновские спектры.
- •6.1 Общая характеристика рентгеновских спектров поглощения и испускания.
- •6.2. Внутренняя конверсия рентгеновского излучения.
- •Тема 7: Явление Зеемана и магнитный резонанс.
- •7.1. Расщепление уровней энергии в магнитном поле.
- •7.2. Общая картина зеемановского расщепления спектральных линий.
- •Тема 8. Явление Штарка.
- •8.1. Общая характеристика явления Штарка.
- •8.2. Явление Штарка для атомов в общем случае.
- •Часть 4. Молекулярный спектральный анализ Тема 9: ик-спектрометрия и уф-спектрофотометрия
- •9.1. Строение молекулы
- •9.2. Молекулярные спектры
- •9.3. Вращательные спектры
- •9.4 Колебательные спектры
- •9.5 Электронные спектры
- •9.6 Аппаратура ик-спектроскопии.
- •2) Кюветное отделение.
- •3) Фотометр
- •4) Монохроматор
- •9.7 Аппаратура уф – спектроскопии
- •4)Кюветное отделение
- •Тема 10. Качественный и количественный молекулярный анализ.
- •D зависит только от числа поглощающих частиц на пути светового пучка и от их свойств.
- •5.1. Качественный молекулярный анализ
- •5.2. Количественный молекулярный анализ
- •3 Эмиссионный спектральный анализ.
1.3.1. Оптическое возбуждение
Оптическое возбуждение – возбуждение путём поглощения фотонов.
Условия возбуждения здесь наиболее просты. Его можно получить излучением известного спектрального состава, в частности монохроматическим излучением, то есть сообщая атомной системе определённые порции энергии hv. Оптическое возбуждение может быть прекращено в заданный момент времени, что позволяет исследовать испускание атомных систем после прекращения возбуждения – послесвечение – измерять его длительность и законы затухания.
Испускание, обладающее малой длительностью послесвечения называется флуоресценцией, а обладающее большой продолжительностью послесвечения, называется фосфоресценцией. Оба типа испускания являются частными случаями фотолюминесценции.
Простейшим и очень важным случаем оптического возбуждения является возбуждение одного определённого дискретного верхнего уровня Ei атома газа из основного состояния E1:
![]()
Возбуждённый атом может отдать свою энергию возбуждения двумя способами:
Путём испускания фотона, т.е. при переходе с излучением.
Путём потери Е при столкновении с другой частицей, то есть при безизлучательном переходе.
Если атом возвращается в основное состояние, испуская фотон hv той же частоты v, что и поглощённый фотон, то имеем резонансное испускание, а соответствующее излучение называется резонансным. Линии, для которых наблюдается резонансное испускание, называется резонансными.
Явление резонансного испускания было впервые обнаружено Вудом в 1905 году в парах натрия.
Обычно термин «резонансные линии» применяют к одной или нескольким линиям, наиболее интенсивном при резонансном испускании. Обычно подобные лини соответствуют переходам на основной уровень с первого возбуждённого уровня.
К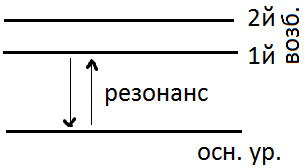 огда
происходит оптическое возбуждение
уровня, с которого возможны переходы
не только обратно на основной уровень,
но и на другие, более низкие по сравнению
с ним возбуждённые уровни, наряду с
резонансным испусканием наблюдается
испускание с частотами, меньшими частоте
резонансной линии. Излучение такого не
резонансного испускания
атомов позволяет проверить правильность
схем уровней энергии.
огда
происходит оптическое возбуждение
уровня, с которого возможны переходы
не только обратно на основной уровень,
но и на другие, более низкие по сравнению
с ним возбуждённые уровни, наряду с
резонансным испусканием наблюдается
испускание с частотами, меньшими частоте
резонансной линии. Излучение такого не
резонансного испускания
атомов позволяет проверить правильность
схем уровней энергии.
Правило
Стокса:
для испускания, наблюдаемого при
оптическом возбуждени атомных систем
с основного уровня, характерно то, что
частота линий испусскания ![]() частоте
линий поглощения:
частоте
линий поглощения:
![]() (1.5)
(1.5)
Испускание, удовлетворяющее правилу Стокса (1.5), называется стоксовым, а линии испускания – стоксовыми линиями.
Ν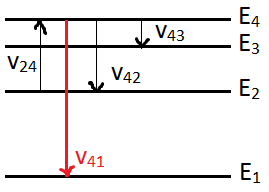 β:
Правило Стокса справедливо лишь для
возбуждения с основного уровня. При
возбуждении с более высоких уровней
может получаться антистоксово испускание,
для которого частота испускаемых фотонов
больше частоты поглощения:
β:
Правило Стокса справедливо лишь для
возбуждения с основного уровня. При
возбуждении с более высоких уровней
может получаться антистоксово испускание,
для которого частота испускаемых фотонов
больше частоты поглощения:
![]() (1.6)
– условие
антистоксового испускания
(1.6)
– условие
антистоксового испускания
Соответствующие линии – антистоксовые. Пример: v41 – антистоксовая линия.
При рассмотрении оптического возбуждения необходимо учитывать, что излучение может не только поглощаться веществом, но и рассеиваться в нём, меняя своё направление распространения.
Различают:
Релеевское рассеивание в однородной среде
Рассеивание в мутной среде (эффект Тиндаля)
Комбинационное рассеивание (эффект Рамана)
В 1-м и 2-м рассеивании частота излучения не меняется, энергия рассеивающих систем – постоянна. В 3-м рассеивании частота излучения при рассеивании меняется, энергия рассеивающих систем меняется.
Рассеивание без изменения частоты является когерентным, фаза рассеянного излучения определяется фазой падающего излучения. Рассеивание с изменением частоты является не когерентным – фаза рассеянного излучения не зависима от фазы падающего излучения.
Лекция № 3 от 14.03.2011
