
- •Вопросы для самостоятельного изучения
- •Часть 4
- •1. Разделение неограниченно смешивающихся жидкостей методом перегонки.
- •Разделение азеотропных смесей
- •2. Диаграмы плавкости
- •Системы с образованием химических соединений, плавящихся конгруэнтно ( с образованием устойчивых химических соединений)
- •2.2 Системы с образованием химических соединений, плавящихся инконгруэнтно (системы с образованием неустойчивых химических соединений)
- •2.3 Системы с неограниченной растворимостью компонентов в жидком состоянии и ограниченной растворимостью в твердом состоянии
- •2.4 Системы с неограниченной растворимостью компонентов и в жидкой и в твердой фазе
- •3. Трёхкомпонентные системы
- •3.1 Графическое изображение состава трехкомпонентных систем
- •3.2 Равновесие жидкость – жидкость в трехкомпонентных системах
- •4. Распределение растворяемого вещества между двумя несмешивающимися жидкостями
- •Отклонения от закона распределения
- •Экстракция
2.3 Системы с неограниченной растворимостью компонентов в жидком состоянии и ограниченной растворимостью в твердом состоянии
Описание диаграммы: Линия аЕb – линия ликвидуса, асЕdb – линия солидуса.
Области:
– расплав.
– равновесие расплава с твердым раствором В в А. В точке М система с общим составом g1 состоит из жидкости с составом g1ж и твердого раствора с составом g1тв . Относительные количества фаз находят по правилу рычага.
– расплав + твердый раствор А в В.
– твердый раствор В в А (фаза одна).
– твердый раствор А в В (фаза одна).
– равновесие твердого раствора В в А и твердого раствора А в В.
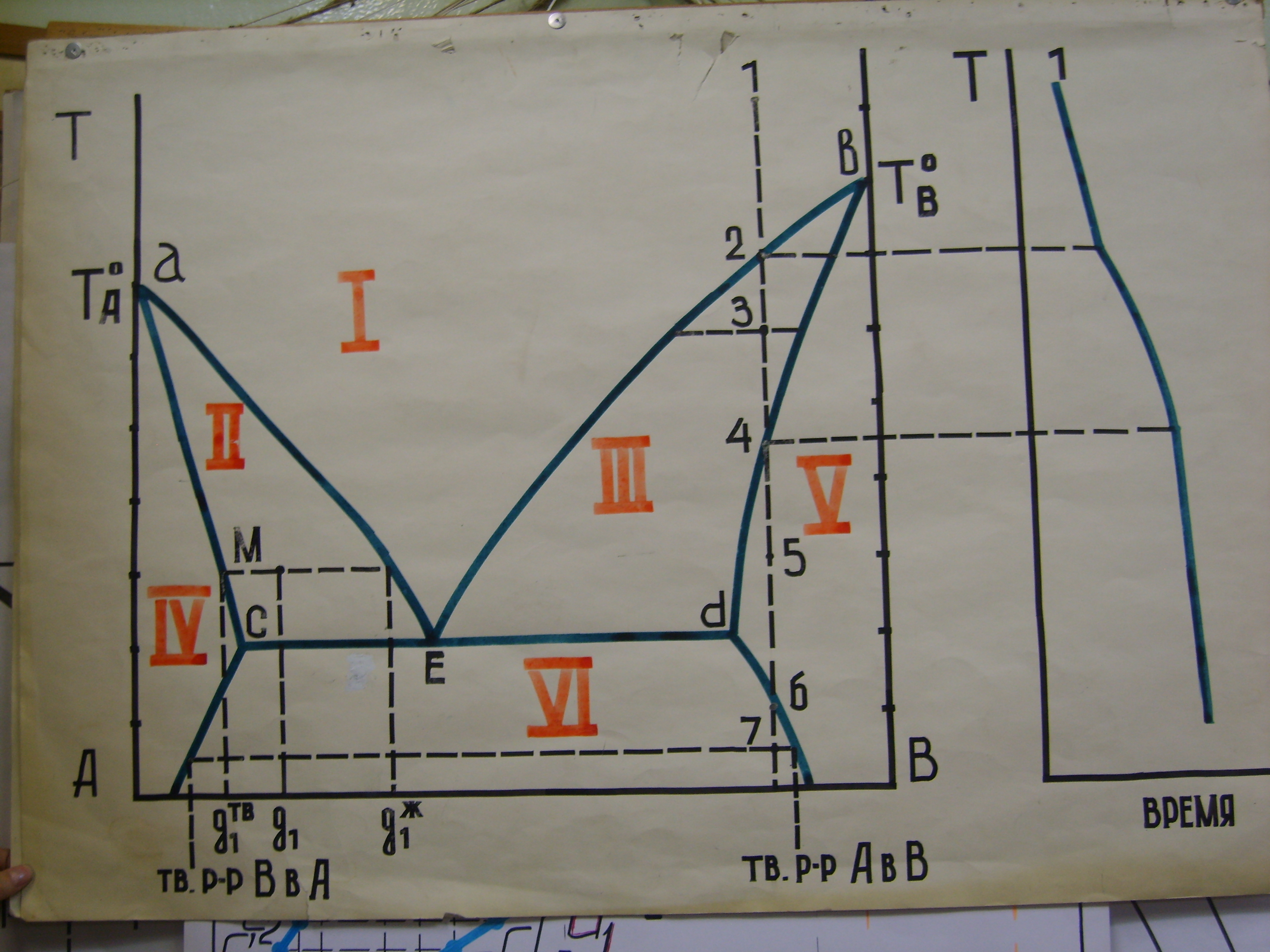
Рассмотрим процесс кристаллизации.
Точка 1: фаза одна – жидкая, С=2 – 1+1=2.
Точка 2: начало кристаллизации – выпадают кристаллы твердого раствора А в В. С=2 – 2+1=1, температура продолжает падать, выделяется теплота.
Точка 3: равновесие твердого раствора А в В и расплава. В ходе кристаллизации состав расплава меняется, меняется и состав твердой фазы (в том числе и состав ранее выпавших кристаллов, если это происходит медленно).
Точка 4: конец кристаллизации, фаза одна (твердый раствор А в В).
Точка 5: фаза одна, состав фазы не изменяется.
Точка 6: начинается уменьшение растворимости А в В в твердой фазе, выделяются кристаллы твердого раствора В в А.
Точка 7: равновесие твердого раствора А в В и твердого раствора В в А.
2.4 Системы с неограниченной растворимостью компонентов и в жидкой и в твердой фазе
Твердые растворы – изоморфные системы (одинаковая форма кристалла). Изоморфизм – свойство атомов или ионов замещать друг друга в кристаллических решетках.
Пример: система Cu – Ni:
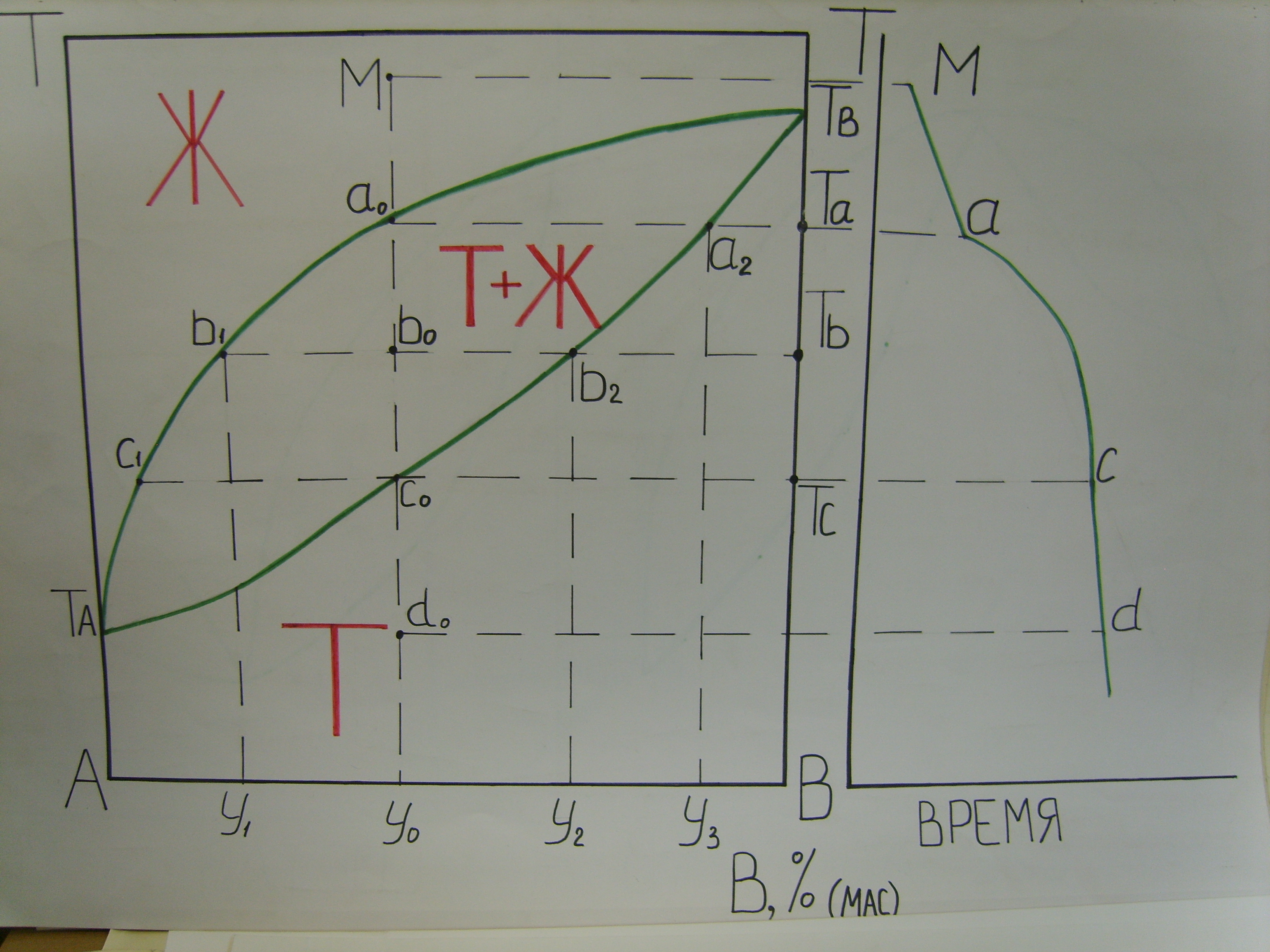
Описание диаграммы: верхняя линия – линия ликвидуса, выше нее система находится в жидком состоянии. Нижняя линия – линия солидуса, ниже нее система находится в твердом состоянии.
Области:
I – расплав,
II – расплав + кристаллы твердого раствора,
III – твердый раствор.
Рассмотрим
процесс кристаллизации из точки М.
Начинается кристаллизация в точке a![]() .
Выпадают кристаллы твердого раствора
с составом, соответствующим точке
a
.
Выпадают кристаллы твердого раствора
с составом, соответствующим точке
a![]() (у
(у![]() ).
В ходе кристаллизации состав расплава
изменяется, изменяется и состав твердой
фазы; заканчивается кристаллизация в
точке с
.
Все кристаллы имеют состав у
.
В твердой фазе можно получить кристаллы
любого состава, поэтому эти компоненты
неограниченно растворимы в твердой
фазе.
).
В ходе кристаллизации состав расплава
изменяется, изменяется и состав твердой
фазы; заканчивается кристаллизация в
точке с
.
Все кристаллы имеют состав у
.
В твердой фазе можно получить кристаллы
любого состава, поэтому эти компоненты
неограниченно растворимы в твердой
фазе.
3. Трёхкомпонентные системы
3.1 Графическое изображение состава трехкомпонентных систем
Для
описания состояния трехкомпонентной
системы нужно задавать 4 параметра: р,
Т, х![]() ,
х
.
Изобразить состояние такой системы
можно в четырехмерном пространстве.
Если рассматривать систему при постоянном
давлении, то задавать нужно 3 параметра.
Изобразить состояние системы можно на
трехмерной диаграмме. Если рассматривать
при постоянных давлении и температуре,
то задавать нужно 2 параметра: х
,
х
,
а изобразить состояние можно на плоской
диаграмме, при этом условное число
степеней свободы: Сусл=3
– Ф. Можно изображать состояние системы
в прямоугольных координатах, чаще
пользуются треугольными диаграммами.
,
х
.
Изобразить состояние такой системы
можно в четырехмерном пространстве.
Если рассматривать систему при постоянном
давлении, то задавать нужно 3 параметра.
Изобразить состояние системы можно на
трехмерной диаграмме. Если рассматривать
при постоянных давлении и температуре,
то задавать нужно 2 параметра: х
,
х
,
а изобразить состояние можно на плоской
диаграмме, при этом условное число
степеней свободы: Сусл=3
– Ф. Можно изображать состояние системы
в прямоугольных координатах, чаще
пользуются треугольными диаграммами.
Треугольник состава
Треугольник
 АВС
- равносторонний.
АВС
- равносторонний.
Точки А, В и С изображают чистые компоненты. Линии АВ, ВС и СА изображают двухкомпонентные системы. Точки внутри треугольника изображают трехкомпонентные системы. Для определения состава используют один из двух методов.
Метод Гиббса. Он основан на свойстве равностороннего треугольника: сумма длин перпендикуляров, опущенных на стороны из любой точки внутри треугольника, равна высоте треугольника:
РНа+ РНв+РНс=Сс.
Чтобы определить концентрацию компонента А в системе, состав которой изображается точкой Р, нужно провести из точки Р перпендикуляр на сторону противолежащую вершине А и определить какую долю его длина состовляет от высоты треугольника. Для удобства можно высоту разделить на 10 частей и нанести шкалу на одной из сторон треугольника.
Например,
в точке Р:
![]() .
.
Метод
Розебума. Он основан на свойстве
равностороннего треугольника: сумма
длин отрезков, проведенных параллельно
каждой стороне треугольника из любой
точки внутри треугольника равна длине
стороны треугольника. Для того, чтобы
определить концентрацию компонента А
в системе, состав которой изображается
точкой Р, нужно из этой точки провести
прямую до пересечения с противолежащей
стороной по отношению к вершине А
параллельно одной из двух других сторон
и определить, какую долю длина полученного
отрезка прямой состовляет от длины
стороны треугольника:
![]() .
.
Свойства треугольника состава

На линии LM: [В]=const. Точки на линии, параллельной стороне треугольника, соответствуют постоянной концентрации компонента, изображаемого противолежащей вершиной треугольника.
На линии BQ:
 .
Точки на линии, проведенной из вершины,
изображающей один из компонентов,
соответствуют постоянному отношению
концентраций двух других компонентов.
.
Точки на линии, проведенной из вершины,
изображающей один из компонентов,
соответствуют постоянному отношению
концентраций двух других компонентов.
