
Второе начало термодинамики
Невозможен процесс, в котором теплота самопроизвольно передаётся от менее нагретого тепла к более нагретому.
Ни в каком процессе энергия не может вновь возникать или исчезать – необратимость процессов.
Аморфные и кристаллические тела
Аморфными называют тела, физические свойства которых одинаковы по всем направлениям (смола, янтарь, стекло)
Аморфные тела – изотропные, т.к. молекулы и атомы располагаются хаотично.
Кристаллы – твердые тела; атомы и молекулы располагаются упорядоченно и образуют периодически повторяющуюся структуру. Физические свойства кристаллов неодинаковы в разных направлениях, но одинаковы в параллельных направлениях. Это свойство называется анизотропностью.
Анизотропия объясняется тем, что расстояние между атомами молекулами неодинаково в разных направлениях и силы взаимодействия между ними различны в разных направлениях.
Монокристаллы имеют периодически повторяющуюся внутреннюю структуру во всём объёме.
Поликристаллы – совокупность сросшихся друг с другом хаотически ориентированных кристаллов.
Кристаллической решёткой называется пространственная сетка, узлы которой совпадают с центрами атомов или молекул в кристалле.
Поликристаллическими телами являются все металлы, камни, соли, песок и т.д.
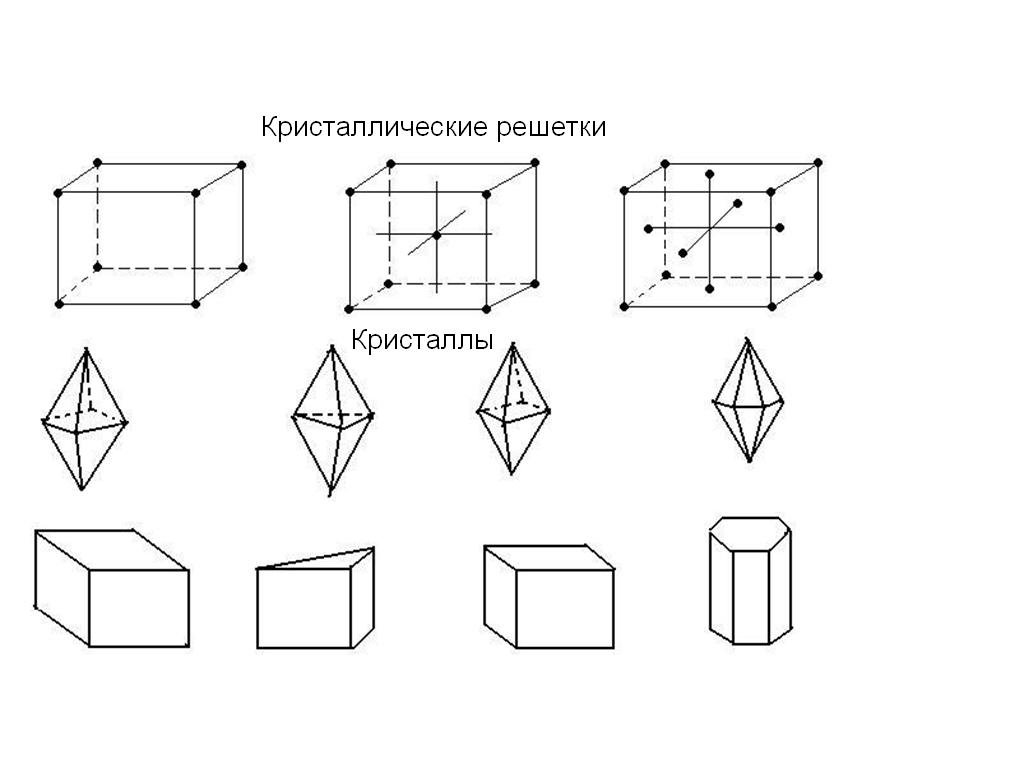
Дефекты кристаллической решётки
1) Дефект дислокация.
Простая дислокация заключается в том, что в какой-либо участок кристалла внедрилась лишняя узловая плоскость, в результате кристалл оказывается разбитым на два блока.
2) Диффузия
При длительном контакте двух твёрдых тел происходит диффузия. В идеальном кристалле, диффузия почти невозможна, т.к. в идеальном кристалле все узловые точки заняты «своими» атомами, поэтому, внедрение «чужеродного» атома в узловую точку должно сопровождаться значительной работой по вырыванию атома из узла, на что обычно энергии не хватает.
3) Дефект замещения.
При достаточно высокой температуре вероятен процесс, при котором чужеродный атом и атом основного вещества меняются местами, что приводит к перемещению чужеродного атома по кристаллу.
Наличие дефектов в кристалле сильно влияет на его свойства. Например, примеси в кристаллической решётке германия, или кремния, составляющие всего лишь 0,1%, практически никак не влияют на структуру кристалла, но очень существенно в 1000 раз меняют его электрическое сопротивление.
Дефекты существенно уменьшают прочность кристаллов.
Кипение
Процесс испарения может происходить не только с поверхности жидкости, но и внутри жидкости. Пузырьки пара внутри жидкости расширяются и всплывают на поверхность, если P0>Pвнеш. Процесс называется кипением.
Точка кипения остается постоянной Tкип воды = 100 оС.
При понижении внешнего давления Ткип жидкости понижается, при повышении давления Ткип повышается.
Критическая температура
Любое вещество, находящееся в газообразном состоянии может превратиться в жидкость при температуре ниже критической. Каждое вещество имеет свою критическую температуру.
Тк – это температура, при которой исчезают различия в физических свойствах между жидкостью и насыщенным паром.
Для сжижения любого газа надо сначала охладить его до температуры ниже критической Тг < Тк, а затем увеличить давление до значения, превышающего давление насыщенного пара.
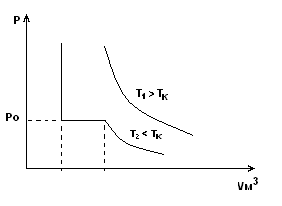
Относительная влажность воздуха
Относительной влажностью воздуха называется отношение давления водяного пара содержащегося в воздухе при данной температуре к давлению насыщенного пара при той же температуре, выраженное в %.
При φ=100% наступает динамическое равновесие между конденсацией и испарением, а количество воды не уменьшается и не увеличивается.
Парциальное давление водяного пара это давление, которое производил бы водяной пар, если бы все остальные газы отсутствовали.
При охлаждении воздуха, находящийся в нем водяной пар, при некоторой температуре становится насыщенным. Эта температура называется точкой росы. По точке росы можно найти давление водяного пара в воздухе P1. Оно равно давлению насыщенного пара при t1 = tр.
φ=P1/P0 х 100%
Свойства жидкостей
Так как молекулы жидкости близко расположены между собой, то объем мало зависит от давления. Жидкость обладает текучестью. Форма жидкости определяется формой сосуда, в который налита жидкость, действием внешних сил и сил поверхностного натяжения. Скорость диффузии в жидкости больше, чем в твердом теле.
Поверхностное натяжение
Силой поверхностного натяжения называют силу, которая действует вдоль поверхности жидкости перпендикулярно к линии, ограничивающей эту поверхность, и стремится сократить ее до минимума.
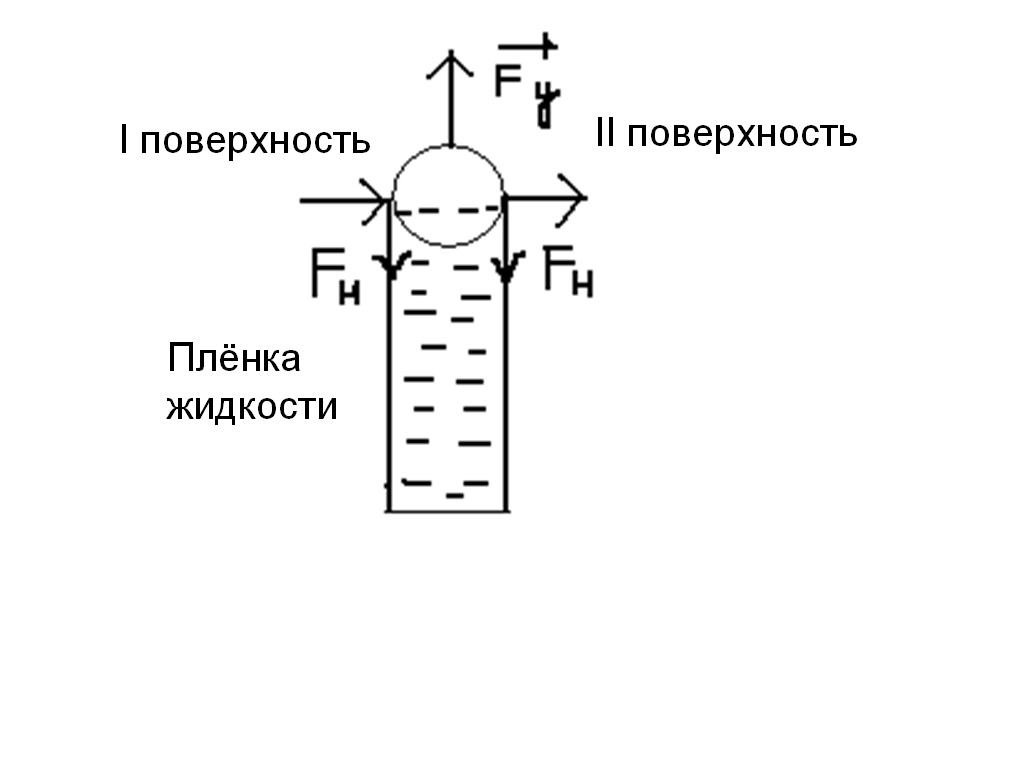
Минимальную поверхность среди тел данного объема имеет шар, поэтому при отсутствии других сил, жидкость под действием поверхностного натяжения принимает форму шара.
Смачивание
Если сила взаимодействия между жидкостью и твердым телом меньше сил взаимодействия между молекулами жидкости, то жидкость не смачивает твердое тело.
Если сила взаимодействия между жидкостью и твердым телом больше сил взаимодействия между молекулами жидкости, то жидкость смачивает твердое тело.
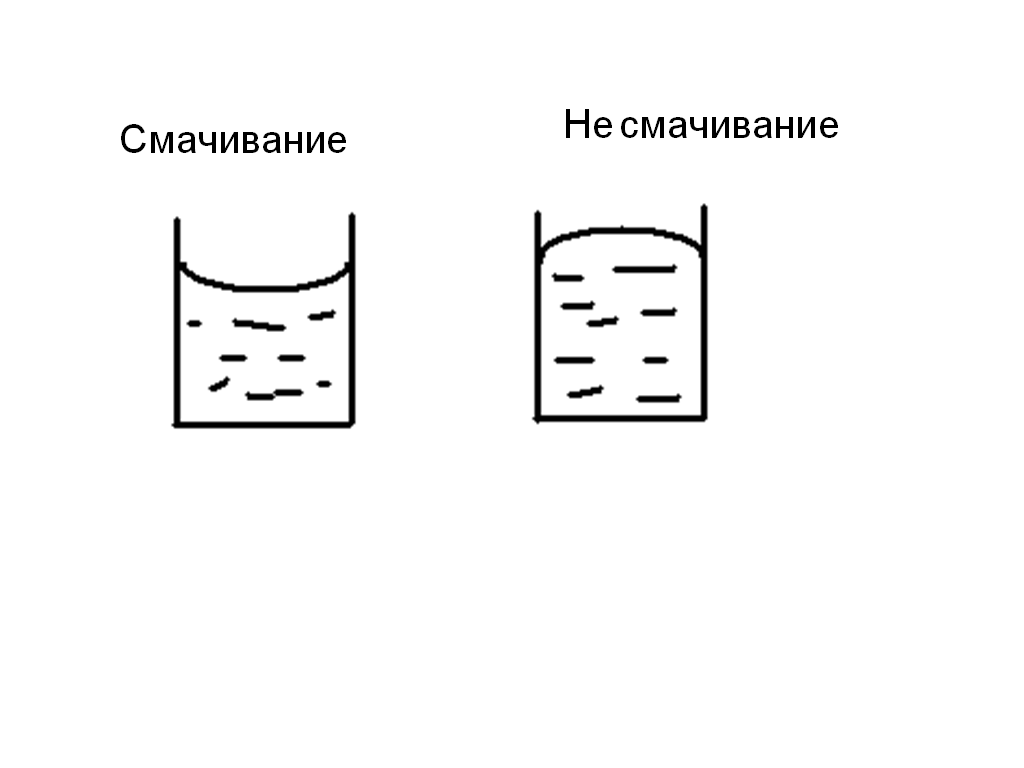
Особенности взаимодействия жидкости со смачиваемыми и не смачиваемыми поверхностями твердых тел служат причиной капиллярных явлений.
Капилляр – это трубка с малым внутренним диаметром.
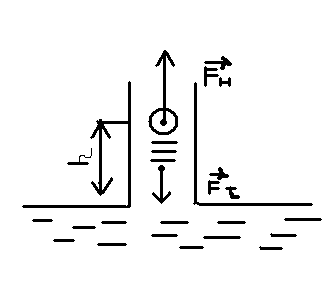
Подъём жидкости вдоль смачивающей поверхности продолжается до тех пор, пока сила тяжести равна силе натяжения (Fj = Fн)
Fj = Fн Fj = mg = ρhπr2g Fн = δl = δ2πr h = (2*δ)/( ρ*g*r) m = ρ*v v = π*r2*h , где h – высота подъёма столба жидкости в капилляре r – радиус капилляра |
