
- •Федеральное агенство по образованию
- •Подготовлено к печати на кафедре
- •Подписано в печать 12.11.04 Сдано в производство 10.11.04
- •Часть 1 Проблемы современного производства
- •Раздел 1.1. Энергетические ресурсы и динамика их
- •Раздел 2.2. Необратимое преобразование химической энергии
- •Раздел 2.3. Энергосбережение в энергосиловых установках…………..63
- •Раздел 2.4. Преобразование химической в работу при
- •Раздел 2.5. Энергосбережение в системах производства
- •Часть 1 Проблемы современного производства
- •Раздел 1.1. Энергетические ресурсы и динамика их
- •1.1.1. Источники энергии, мера их измерения
- •1.1.2. Топливно-энергетический потенциал Земли
- •Доказанные извлекаемые запасы органических топлив
- •1.1.3. Производство и потребление топливно - энергетических
- •1.1.4. Структура топливно – энергетических ресурсов.
- •1.1.5. Динамика потребления энергетических ресурсов.
- •1.1.6. Возобновляемые источники энергии.
- •Отсутствие дешевых преобразователей, низкие плотности потоков и неравномерность освещения сильно сдерживают использование этого вида энергии.
- •1.1.7. Новые источники энергии.
- •Раздел 1.2. Энергетический анализ технологий производства энергетической продукции
- •1.2.1 Топливные циклы.
- •Годовая потребность q в органическом топливе в натуральном
- •Приведем результаты расчетов по формулам (2.1) и (2.2) в виде
- •Количество отпущенной тэц в сеть за год электроэнергии
- •Раздел 1.3. Энергетика и экология
- •1.3.1. Место энергетики в антропогенных загрязнениях
- •До 80% антропогенных загрязнений окружающей среды
- •Выбросы вредных веществ в атмосферу являются наиболее важным
- •Выбросы загрязняющих веществ от предприятий энергетики
- •Тэк обеспечивает около 70% ежегодного нарушения земель
- •1.3.2. Структура вредных выбросов и их влияние на
- •1.3.3. Экологические требования к объектам энергетики
- •Поэтому при строительстве каждого энергообъекта обязательно
- •Невыполнение любого из приведенных ограничений делает
- •Все, рассмотренные выше, факторы негативного воздействия тэк
- •Раздел 1.4. Энергетика и экономика
- •1.4.1. Математические модели экономики
- •Модель обладает рядом недостатков. Например, считается, что
- •1.4.2. Модель экономики, включающая энергетику
- •Роль научно-технического прогресса и
- •Часть 2. Термодинамические основы энергосбережения
- •Раздел 2.1. Основы теории преобразования тепловой
- •2.1.1. Теорема Карно.
- •Энтропия как физическая характеристика преобразования тепла в работу. Неравенство Клаузиуса.
- •2.1.5. Химический потенциал
- •2.1.6. Эксергия
- •Подставляя (2.1.31) в (2.1.30), получим что
- •Раздел 2.2. Горение топлив и преобразование выделяющейся
- •Современное производство энергетической продукции и
- •2.2.2. Тепловые эффекты химических реакций. Закон Гесса.
- •Рассмотрим произвольную химическую реакцию
- •2.2.3. Тепловые эффекты образования веществ.
- •2.2.4. Изменение тепловых эффектов химических реакций
- •Тепловой эффект химической реакции
- •2.2.6. Преобразование энергии, выделяющейся при горении
- •2.2.6. Основные направления совершенствования
- •Раздел 2.3. Энергосбережение в энергосиловых установках
- •2.3.1. Регенерация тепла
- •Рассмотрим в качестве примера следующую задачу: как изменится
- •2.3.2. Изотермический подвод и отвод теплоты.
- •2.3.2. Бинарные циклы. Температуры горения органических топлив достаточно велики, и
- •2.3.3. Парогазовые установки.
- •При работе в базовом режиме используется пту, газотурбинная
- •Раздел 2.4. Преобразование химической в работу при
- •Константы равновесия химических реакций.
- •Максимальная работа при обратимых процессах.
- •2.4.3. Коэффициент использования топлива при
- •Идеальная машина для обратимого окисления
- •Раздел 2.5. Энергосбережение в системах производства
- •2.5.1. Обратимое преобразование работы в теплоту. Цикл
- •Обратимое преобразование теплоты.
- •Из рисунка видно, что при преобразовании тепла от источника с
- •Для холодильной машины
- •2.5.3. Тепловые насосы.
- •2.5.4. Энергосбережение при теплофикации
- •Количество отработанной теплоты, полезно использованной для
- •Сравнительный анализ теплофикации и тепловых
- •Р ис.2.5.7. Схемы двух исследуемых вариантов теплоснабжения
- •2.5.6. Основные направления энергосбережения при
- •Приложение 1. Зависимости средних теплоемкостей газов от температуры.
Часть 2. Термодинамические основы энергосбережения
Раздел 2.1. Основы теории преобразования тепловой
энергии в работу.
2.1.1. Теорема Карно.
Основные теоретические представления о превращении теплоты в работу были сформулированы С. Карно в 1824 году. Карно рассмотрел идеальный тепловой двигатель, работающий по циклу, который впоследствии получил название цикла Карно, и сформулировал основные положения, лежащие в основе работы тепловых двигателей. Для осуществления теплового двигателя необходимо иметь, по крайней мере, два тепловых резервуара с различными температурами T1 и T2 (см. рис. 2.1.1). Сжатие и расширение рабочего тела должно происходить при разных температурах, так как только в этом случае будет совершена положительная (полезная) работа. Рабочее тело двигателя, приведенное в контакт с горячим источником теплоты, начинает расширяться. Чтобы процесс расширения был обратимым, необходимо равенство температур тела и резервуара при расширении, которое имеет место только тогда, когда расширение происходит достаточно медленно. Та же ситуация имеет место и при сжатии. От горячего источника теплоты с температурой Т1 в процессе расширения берется тепло q1. В процессе сжатия холодному источнику теплоты с температурой Т2 отдается тепло q2. Чтобы замкнуть цикл, нужно изолировать на время перехода вещество от обоих резервуаров и заставить менять свое состояние по адиабатам (см. рис. 2.1.1). За цикл рабочее тело совершит работу l=q1-q2. Термический коэффициент полезного действия (КПД) теплового двигателя
![]()
В качестве примера рабочего тела, совершающего цикл Карно, Р. Клаузиус взял идеальный газ и провел расчет КПД цикла. В состоянии 1 температура газа равна температуре Т1 горячего источника теплоты. В процессе изотермического расширения газ переходит в состояние 2 (процесс 1-2 на рис. 2.1.2). Совершаемая газом удельная работа
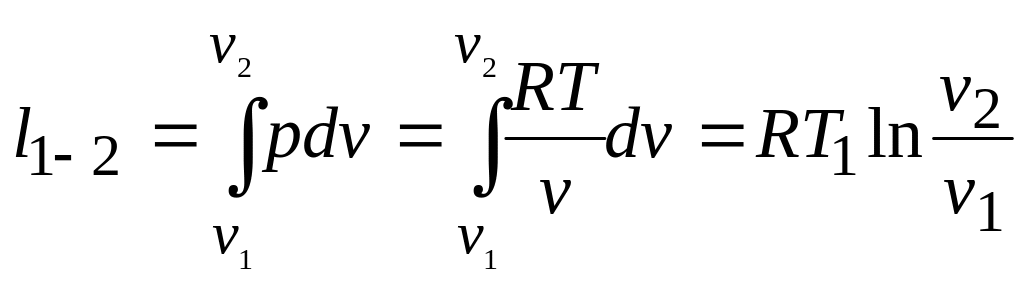 .
(2.1.1) Внутренняя
энергия идеального газа зависит
только
от температуры
и при изотермическом расширении не
изменяется. Следовательно, согласно
первому закону
термодинамики
тепло, полученное от горячего источника
q1
= l1-2.
Из состояния 2 в состояние 3 газ переходит,
расширяясь по адиабате и совершая
работу. Согласно первому закону
термодинамики эта работа равно убыли
его внутренней энергии
.
(2.1.1) Внутренняя
энергия идеального газа зависит
только
от температуры
и при изотермическом расширении не
изменяется. Следовательно, согласно
первому закону
термодинамики
тепло, полученное от горячего источника
q1
= l1-2.
Из состояния 2 в состояние 3 газ переходит,
расширяясь по адиабате и совершая
работу. Согласно первому закону
термодинамики эта работа равно убыли
его внутренней энергии
![]() .
.
В процессе 3-4 изотермического сжатия совершаемая газом работа
![]() ,
(2.1.2)
,
(2.1.2)
т.к. движение поршня происходит против действия силы давления. Сжатие газа требует затрат энергии от внешнего источника, которым служит, используемый в машине, маховик. Отдаваемое газом тепло q2>0 холодному источнику q2=-l3-4. Работа, совершаемая газом при адиабатическом сжатии
![]() .
.
Суммарная работа, совершенная газом за цикл,
l = l1-2 + l2-3 + l3-4 + l4-1 = l1-2 + l3-4 (2.1.3)
Преобразуем полученное выражение, воспользовавшись формулой для адиабаты. Из нее следует, что
![]() .
.
Если теперь разделить по-членно первую формулу на вторую, то получим, что
![]() .
.
Суммарная работа, совершенная газом, как следует из формул (2.1.1) -(2.1.3) оказывается равной
![]() ,
,
а термический КПД
![]() .
(2.1.4)
.
(2.1.4)
Формула (2.1.4) известна как формула Карно.
Приведенный вывод исходил из предположения, что рабочим телом служит идеальный газ. В действительности она справедлива для любого рабочего тела, совершающего обратимый цикл Карно.
Сформулируем положение, известное как теорема Карно. Пусть рабочее тело совершает цикл Карно (см. рис.2.1.2). Отношение количества тепла q1 , полученного от горячего источника тепла, к количеству тепла q2 , отданного холодному источнику тепла, не зависит от природы рабочего тела и определяется только температурой T1 нагревателя и температурой холодильника T 2 :
![]() .
(2.1.5)
.
(2.1.5)
Иными словами, (см. формулу (2.2.1)) термический коэффициент полезного действия любой машины, работающей по обратимому циклу Карно не зависит от природы рабочего тела, а определяется только температурами горячего и холодного источников тепла.
Р.Клаузиус дал доказательство этой теоремы, исходя из следующего положения: теплота не может переходить сама собой от более холодного тела к более горячему.
Отсутствие самопроизвольного перехода тепла вовсе не означает, что нельзя осуществить передачу тепла от холодного тела к горячему. Однако, для того, чтобы это произошло нужно, затратить работу внешних сил по отношению к рассматриваемой термодинамической системе. Без внешнего воздействия такой переход невозможен. Это положение легло в основу одной из формулировок второго начала термодинамики.
Рассмотрим это доказательство. Пусть имеются два рабочих тела C и C'. Предположим, что они берут одинаковое количество тепла q1 = q1 ' из горячего источника К1 тепла и передают разные количества q2 < q2' холодному источнику К2. Заставим первое тело совершить цикл Карно и передать источнику К2 тепло q2. Второе тело заставим проделать круговой процесс в обратном направлении. Оно возьмет тепло q2' из холодного источника К2 и вернет источнику К1 тепло q1, взятое первым телом. Так как первое тело совершило большую работу, чем нужно затратить второму для возвращения тела источнику К1, то есть избыток работы l = l - l' > 0. Таким образом, нам удалось получить работу за счет тепла одного источника. Эту работу всегда можно потратить на передачу тепла от холодного тела к горячему. В результате в системе из двух источников тепла и двух машин осуществился переход тепла от холодного источника тепла к горячему без затрат работы со стороны внешних к системе тел. Остается одно, что q2 = q2'.
Из формулы (2.1.4), найденной для идеального газа, немедленно следует, что для любого тела, совершающего цикл Карно,
![]() ,
,
или
![]() .
(2.1.6)
.
(2.1.6)
Таким образом, второе начало термодинамики позволяет определить вид функции F(T1,T2).
В расчетах удобно говорить только о поглощаемой теплоте и рассматривать отдаваемое количество теплоты как поглощаемое со знаком минус. Принимая такое правило знаков, запишем полученный результат в виде
![]() .
(2.1.7)
.
(2.1.7)
Формулу (2.1.7) легко обобщить на произвольный циклический процесс, представив его как совокупность большого числа циклов Карно, к каждому из которых применимо равенство (2.1.6). В результате получим
![]() .
(2.1.8)
.
(2.1.8)
Формула (2.1.8) позволяет определить энтропию равенством
![]() (2.1.9)
(2.1.9)
для любого тела.
Существуют другие формулировки второго закона термодинамики. Одна из них была дана В. Томсоном в 1851 году: периодически действующая машина, единственным результатом действия которой было бы производство работы за счет получения тепла от одного источника, невозможна. Другая формулировка состоит в невозможности вечного двигателя второго рода, способного совершать работу за счет тепла одного источника. Все эти формулировки второго закона термодинамики эквивалентны и из одной из них немедленно следует другая.
