
- •Диаграммы состояния бинарных систем. Закон Рауля. Диаграммы «давление - состав»,
- •Второй закон Коновалова.
- •Жидкие смеси с неограниченной растворимостью компонентов. Смеси, подчиняющиеся закону Рауля (идеальные смеси): давление и состав пара. Диаграмма «давление – состав».
- •Анализ диаграмм азеотропных смесей.
- •Фракционная перегонка неограниченно смешивающихся жидкостей.
- •Простая перегонка.
- •Взаимно нерастворимые жидкости.
- •Экстракция.
- •Некоторые основные понятия жидкостной экстракции
- •Экстракционное равновесие
- •Использование процессов экстракции в фармацевтическом анализе
- •Диаграммы плавкости.
- •Диаграмма плавкости
- •Применение диаграмм плавкости.
Экстракция.
Взаимно нерастворимые жидкости используют в экстракции. В основе экстракции лежит закон распределения: вещество, добавляемое к системе, состоящей из двух нерастворимых жидкостей, распределяется между обеими фазами в определенном отношении, постоянном при данной температуре.
С помощью водных сред из разных объектов извлекают водо-растворимые компоненты, а с помощью неполярных жидкостей (бензол, масло, ацетон) – соединения углеводородной природы.
Некоторые основные понятия жидкостной экстракции
Экстрагент — органический растворитель в индивидуальном состоянии или содержащий какие-либо реагенты, извлекающий (экстрагирующий) данное вещество из водной фазы.
Так, например, молекулярный иод можно экстрагировать из водной фазы экстрагентом хлороформом, в котором он более растворим, чем в воде. Экстракцию ионов алюминия А13+ из водной фазы можно провести хлороформным раствором 8-оксихинолина. Ионы алюминия образуют с 8-оксихинолином комплексное соединение — оксихинолинат алюминия (оксинат алюминия), который лучше растворяется в хлороформе, чем в воде, и поэтому переходит из водной фазы в хлороформную.
Экстракт — отделенная жидкая органическая фаза, содержащая экстрагированное из водной фазы вещество. В наших примерах экстракт — это хлороформные вытяжки, содержащие экстрагированный молекулярный иод или оксихинолинат алюминия.
Понятие экстракт в жидкостной экстракции и в анализе лекарственного растительного сырья имеет различный смысл. В последнем случае согласно Государственной Фармакопее (1990, XI издание с. 160) «экстракты представляют собой концентрированные извлечения из лекарственного растительного сырья». При этом экстракты могут быть жидкими, густые и сухие. В качестве экстрагентов при экстракции лекарственного растительного сырья чаще всего применяют воду, водные растворы этанола, реже — другие экстрагенты. Сухие экстракты получают после полного удаления жидкой фазы тем или иным способом, обеспечивающим максимальное сохранение в сухом остатке фармакологически активных компонентов жидкого экстракта (высушивание, сублимация и др.)
Экстракционное равновесие
Закон распределения Нернста. Константа распределения Р. Рассмотрим распределение некоторого вещества А между контактирующими несмешивающимися жидкими органической и водной фазами при постоянной температуре (Т = const). Если при достижении состояния истинного равновесия, когда концентрации вещества А в органической и жидкой фазе — равновесные, экстракционное равновесие
А(водн) = А(орг)
рассматривать в качестве химического равновесия, то это равно будет характеризоваться константой равновесия Р, равной
Р=а(орг)/а(водн)
где
а(орг) и а(водн) – равновесные активности вещества
А в органической и водной фазах соответственно.
Величина Р в данном случае называется константой распределения, она постоянна при постоянной температуре для данной системы.
Если химическая природа вещества А одинакова в обеих жидких фазах, тогда формула переходит в:
Р=[А]орг/[А]водн
Константа распределения Р зависит от природы распределяемого вещества и жидких фаз, температуры.
Чем больше константа распределения, тем полнее экстрагируемое вещество извлекается из водного раствора в органическую фазу.
Коэффициент распределения D. Распределяющееся вещество часто находится в несмешивающихся контактирующих жидких органической и водной фазах в неодинаковой химической форме. Например, органические кислоты RCOOH, где R — органический радикал, в водном растворе подвергаются электролитической диссоциации:
RCOOH + H2O = RCOO- + H3O+
т. е. в водном растворе существуют две формы — непродиссоциировавшие молекулы кислоты RCOOH и ее анионы RCOO-. Кроме того, в органической фазе возможна димеризация кислоты RCOOH по схеме
2RCOOH = (RCOOH)2
за счет образования межмолекулярных водородных связей:

 О
…..Н О
О
…..Н О
R С С R
О Н …..О
т. е. в органической фазе присутствуют две химические формы кислоты - мономер RCOOH и димер (RCOOH)2.
Следовательно, межфазное равновесие на границе раздела двух жидких фаз будет более сложным (по сравнению с таким равновесием, когда химическая природа распределяемого вещества в обеих фазах одинакова), что схематически можно представить в виде:
водная фаза {RCOOH+H20 = RCOO-+ H3O+


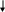
 граница
раздела фаз
граница
раздела фаз
органическая фаза {2RCOOH = (RCOO)2
В подобных случаях (а они встречаются очень часто) суммарное существование различных форм распределяемого вещества учитывается; введением коэффициента распределения D (встречаются и иные буквенные обозначения коэффициента распределения):
D=Σcорг/Σcводн
где Σcорг — сумма равновесных концентраций в органической фазе всех форм распределяемого вещества; Σcводн — сумма равновесных концентраций в водной фазе всех форм распределяемого вещества.
На практике в выражении для коэффициента распределения знаки сумм чаще всего опускают и пишут
D=cорг/cводн
Таким образом, коэффициент распределения D — это отношение суммарной концентрации данного вещества в органической фазе к суммарной концентрации его в водной фазе.
Коэффициент распределения зависит не только от температуры, но и от концентрации распределяемого вещества в обеих жидких фазах, от природы и концентраций других растворенных веществ, рН водной фазы и т. д.
![]()
![]()
 Степень
извлечения (процент экстракции) R.
Под степенью извлечения R понимают
выраженное в процентах отношение
суммарной массы (суммарного количества)
экстрагируемого вещества в органической
фазе к его общей массе (суммарному
количеству) в обеих фазах:
Степень
извлечения (процент экстракции) R.
Под степенью извлечения R понимают
выраженное в процентах отношение
суммарной массы (суммарного количества)
экстрагируемого вещества в органической
фазе к его общей массе (суммарному
количеству) в обеих фазах:
где
nорг и nводн — соответственно количество данного вещества в органической и водной фазах, моль;
cорг и cводн — концентрации данного вещества соответственно в органической и водной фазах, моль/л;
Vорг и Vводн — объем жидкой органической и водной фазы.
Степень извлечения связана с коэффициентом распределения соотношением:

Ч![]() ем
больше величина R,
тем эффективнее процесс экстракции.
Обычно считается, что извлечение
проведено практически полностью (т.е.
количественно), если R≥99,9%.
Если же R<99,9%
, то экстракционное извлечение повторяют.
Влияние на величину R
объёма экстрагента и числа экстракций.
Зависимость степени извлечения R
от объёма исходной водной фазы Vводн,
объёма экстрагента Vорг
и числа n
последовательных экстракций одинаковым
объёмом Vорг
описывается соотношением:
ем
больше величина R,
тем эффективнее процесс экстракции.
Обычно считается, что извлечение
проведено практически полностью (т.е.
количественно), если R≥99,9%.
Если же R<99,9%
, то экстракционное извлечение повторяют.
Влияние на величину R
объёма экстрагента и числа экстракций.
Зависимость степени извлечения R
от объёма исходной водной фазы Vводн,
объёма экстрагента Vорг
и числа n
последовательных экстракций одинаковым
объёмом Vорг
описывается соотношением:
R=[1-1/(1+D ∙Vорг /Vводн )n] ∙100% =
