
- •Тема 1. Твердое тело. Кристаллическая решетка. Симметрия и классификация кристаллов. Дефекты в кристаллах.
- •1.1.Твердое тело (конденсированное состояние).
- •1.2. Типы связей в твердом теле. Природа сил взаимодействия в твердом теле. Кристалл.
- •1.3. Геометрия кристаллической решетки. Трансляция. Элементарная ячейка. Элементы симметрии.
- •1.4. Классы симметрии. Решетка Браве.
- •1 .5. Классификация кристаллов по типу связей.
- •1.6.Символические обозначения плоскостей и направлений в кристаллах. Индексы Миллера.
- •1.7. Дефекты в кристаллах.
- •Вопросы для повторения:
- •Резюме по теме:
- •Тема 2. Элементы зонной теории твердого тела. Цели и задачи изучения темы:
- •2.1. Взгляд на строение атома и твердого тела с позиций квантовой механики. Элементы зонной теории. Энергия ферми.
- •2.2.Четыре типа энергетических (зонных) диаграмм твердого тела.
- •3.2.Собственные и примесные полупроводники. Носители заряда в полупроводниках.
- •3.3. Энергия Ферми.
- •3.4. Генерация и рекомбинация носителей зарядов.
- •3.5. Собственная проводимость полупроводника. Уровень Ферми в собственном полупроводнике. Эффективная масса носителей заряда.
- •3.6. Примесные полупроводники.
- •3.6.1. Примесные уровни.
- •3.6.2. Примесная проводимость полупроводников.
- •3.6.3. Полупроводник р-типа.
- •3.6.4. Сильно легированный полупроводник. Роль беспорядка в кристалле.
- •3.7. Температурная зависимость проводимости примесных полупроводников
- •3.8. Дрейфовый и диффузионный токи в полупроводнике.
- •Вопросы для повторения:
- •Резюме по теме:
- •Тема 4. Свойства электронов. Работа выхода электро-нов. Движение электронов в электрических и магнитных полях.
- •4.1. Свойства электронов.
- •4.2. Работа выхода электронов и влияние адсорбционных слоев на работу выхода.
- •4.2.1. Работа выхода электронов
- •4.2.2. Влияние адсорбционных слоев на работу выхода.
- •4.3. Движение электронов в электрических и магнитных полях.
- •4.3.1. Электрон в электрическом поле.
- •4.3.2. Электрон в магнитном поле.
- •Вопросы для повторения:
- •Резюме:
- •Тема 5. Электронный газ в проводнике. Вырожденный и невырожденный электронный газ. Электропроводность чистых металлов и спла-вов. Электропроводность полупроводников в сильных электрических полях.
- •5.1. Равновесное состояние электронного газа в проводнике в отсутствие электрического поля.
- •5.2. Электропроводность невырожденного и вырожденного газов.
- •5.2.1. Невырожденный газ.
- •5.2.2. Вырожденный газ.
- •5.3. Зависимость подвижности носителей заряда от темпера-туры.
- •5.3.1. Область высоких температур.
- •5.3.2. Область низких температур.
- •5.4. Электропроводность чистых металлов.
- •5.4.1. Проводимость электронных металлов.
- •5.5. Электропроводность металлических сплавов.
- •5.6. Электропроводность полупроводников в сильных электрических полях. Эффект Ганна.
- •Вопросы для повторения:
- •Резюме:
- •Тема 6. Эффект Холла.
- •6.1. Эффект Холла.
- •6.1.1. Эффект Холла в полупроводнике.
- •6.1.2. Эффект Холла в полупроводниках с двумя типами носи-телей заряда.
- •Вопросы для повторения:
- •7.1.2. Толщина двойного электрического слоя, возникающего в месте контакта двух металлов.
- •7.2.Контакт электронного и дырочного полупроводников (p–n переход).
- •Вопросы для повторения:
- •Резюме:
- •Тема 8. Свойства p-n перехода.
- •8.2. Свойства p-n перехода при наличии внешнего напряжения.
- •8.3. Обратное включение p-n перехода.
- •8.4. Вольтамперная характеристика p-n перехода.
- •8.5. Температурные и частотные свойства p-n перехода.
- •8.6. Туннельный эффект.
- •Вопросы для повторения:
- •Резюме:
- •Тема 9. Контакт металл – полупроводник. Гетеропереходы. Поверхностные явления в полупроводнике.
- •9.1. Контакт металл– полупроводник. Переход Шоттки.
- •9.2. Поверхностные явления в полупроводниках.
- •9.3. Гетеропереходы.
- •9.3.1. Идеальный р-n переход
- •9.3.3. Омический переход.
- •Вопросы для повторения:
- •Резюме:
- •Тема 10. Оптические и фотоэлектрические явления в полупроводниках.
- •10.1. Фотопроводимость в полупроводниках.
- •10.2. Фоторезистивный эффект.
- •10.3. Фотоэффект в р-п переходе.
- •10.4.Электромагнитное излучение в полупроводниках.
- •10.5. Лазеры.
- •10.6. Конструкция и изготовление инжекционных лазеров.
- •10.7. Основные характеристики и параметры лазеров.
- •Вопросы для повторения:
- •Резюме:
- •Тема 11. Термоэлектрические явления.
- •11.1. Термоэлектрические явления.
- •11.1.1. Эффект Зеебека.
- •11.1.2. Эффект Пельтье.
- •11.1.3. Эффект Томсона.
- •11.2. Применение термоэлектричества.
- •11.2.1. Применение металлических термобатарей и термопар.
- •11.2.2. Полупроводниковые термоэлектрические приборы.
- •11.2.3. Холодильники и тепловые насосы.
- •11.2.4. Термоэлектрическое охлаждающее устройство (тоу).
- •11.2.5. Использование принципа полупроводникового теплового насоса.
- •Вопросы для повторения:
- •12.1.2. Несамостоятельный разряд.
- •12.1.3. Самостоятельный разряд.
- •12.1.4. Типы самостоятельного разряда.
- •12.2. Понятие о плазме.
- •12.3. Электрический ток в вакууме.
- •12.3.1. Вакуум. Термоэлектронная эмиссия.
- •12.3.2. Электронные лампы.
- •12.4. Электронные пучки. Электронно-лучевая трубка.
- •Вопросы для повторения:
- •Резюме:
- •Приложение Приложение n 1.
- •Приложение n 2.
- •Глоссарий
1 .5. Классификация кристаллов по типу связей.
Расположение атомов или молекул в кристалле зависит от сил взаимодействия между ними. Частицы располагаются таким образом, чтобы энергия взаимодействия между ними была минимальной. Положительная разность между энергией изолированных атомов и атомов в кристаллической решетке называется энергией связи. Значения энергии связи колеблются от 0,1 до 7 эВ на частицу в зависимости от характера взаимодействия. Энергия связи определяет работу, необходимую для удаления частицы из кристалла. Классификация кристаллов по типам связи следующая:
Кристаллы с ван-дер-ваальсовскими связями или молекулярные кристаллы.
Силы взаимодействия в таких кристаллах определяются наличием у молекул естественных или индуцированных электрических моментов. Энергия связи молекулярных решеток обычно имеет порядок 103 ... 104 Дж/моль. Пример таких кристаллов – затвердевшие инертные газы (неон, аргон, криптон, ксенон). Тип решетки этих кристаллов – гранецентрированная кубическая. В ней каждый атом имеет 12 соседей.
Кристаллы с ковалентпной связью. В них взаимодействие между частицами обусловлено тем, что два электрона принадлежат одновременно двум атомам. Такая связь называется также валентной или гомеополярной. Энергия связи таких кристаллов составляет порядка 105… 106 Дж/моль. Примеры - кремний, алмаз и др. Кристаллы с такими связями часто встреча-ются в различных структурных модификациях с почти одинаковыми энергиями связи. Такие модификации называются аллотропными.
Кристаллы с водородной связью, образующейся благодаря электри-ческому взаимодействию атома водорода с другими атомами, обладающими значительной электроотрицательностью. Энергия этой связи достигает 104 Дж/моль. Типичный пример – кристаллы льда, фтороводород HF, синильная кислота HCN и др.
Кристаллы с ионной связью, или просто ионные кристаллы, состоят из ионов противоположных знаков, располагающихся в узлах кристалличес-кой решетки. Энергия связи в таких кристаллах определяется силой кулоновс-кого взаимодействия и достигает величины 105... 106 Дж/моль. Типичный пример NaCl, NH4F и др.
Кристаллы с металлической связью представляют собой совокуп-ность положительных ионов, располагающихся в узлах кристаллической решетки, между которыми квазисвободно движутся валентные электроны, обеспечивая взаимодействие между ионами. Энергия связи в металлических кристаллах составляет 104…105 Дж/моль. Как уже указывалось, кроме вы-шеназванных, между частицами в кристалле возможны смешанные связи.
1.6.Символические обозначения плоскостей и направлений в кристаллах. Индексы Миллера.
Анизотропия кристаллов приводит к необходимости выделять и определенным образом обозначать различные плоскости и направления в кристалле. Для этого пользуются специальной системой координат, связанной с кристаллом так, что координатные оси оказываются параллельными осям симметрии кристалла или перпендикулярными плоскостям симметрии. Координаты в такой системе измеряются в единицах, равных межатомным расстояниям в данном направлении. Эти расстояния называются еще постоянными решетки или параметрами решетки. Положение какой-либо плоскости однозначно определяется координатами любых трех точек этой плоскости, например тех, в которых плоскость пересекается осями координат (рис.1.6.1).
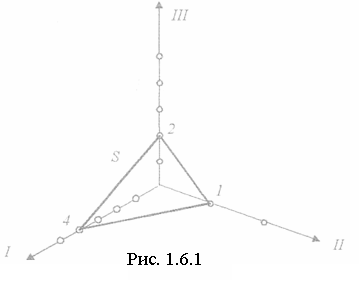
Пусть оси I, II и III являются координатными осями и нуж-но определить плоскость S. Если, например, плоскость пе-ресекает ось I в точке на расстоянии в 4 единицы (т.е. 4 межатомных расстояния), ось II на расстоянии в 1 единицу и ось III на рас-стоянии в 2 единицы, то положение плоскости задается тройкой чисел 4,1,2. Однако в кристаллографии принято пользоваться для обозначения плоскостей не этими числами, а особыми индексами Миллера, которые определяются следующим образом. Берутся обратные значения полученных координат точек пересечения плоскостью координатных осей и эти дроби приводятся к одному знаменателю. Знаменатель отбрасывается, а числители полученных дробей и дают индексы Миллера. Для рассмотренного на чертеже примера координаты равны 4,1,2. Их обратные значения дадут дроби 1/4; 1/1; 1/2. Общий знаменатель дробей – 4. Числители или индексы Миллера оказываются равными 1, 4, 2. Эти индексы записываются в круглых скобках и читаются раздельно (142). Такой набор индексов определяет не одну плоскость, а все семейство параллельных плоскостей. Если рассматриваемая плоскость параллельна одной из осей, т.е. пересекает ее в бесконечности, то соответствующий индекс равен нулю. На рисунке 1.6.2 указаны индексы наиболее важных плоскостей кубического кристалла.
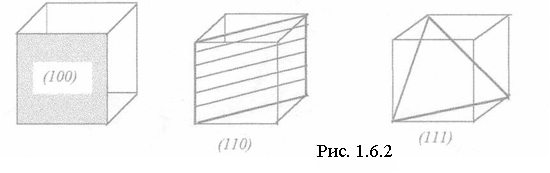
Направления в кристалле также задаются индексами, которые определяются следующим образом. Вдоль определяемого направления выбирают некоторый вектор произвольной длины и определяют величины составляющих вектора по осям координат в единицах постоянной решетки. Тогда индексами этого направления будут три наименьших целых числа, отношения которых между собой равны отношениям составляющих вектора. Если компоненты вектора равны, например 6, 4, 8 единицам, то индексами соответствующего этому вектору направления будут 3,2, и 4. Эти числа заключаются в квадратные скобки [324].
