
- •10 Класс. Зачёт № 4. Опорный конспект № 1
- •10 Класс. Зачёт № 4. Опорный конспект № 3
- •10 Класс. Зачёт № 4. Опорный конспект № 2
- •10 Класс. Зачёт № 3. Опорный конспект № 1
- •10 Класс. Зачёт № 3. Опорный конспект № 2
- •10 Класс. Зачёт № 1. Опорный конспект № 1
- •10 Класс. Зачёт № 2. Опорный конспект № 1
- •10 Класс. Зачёт № 2. Опорный конспект № 2
- •10 Класс. Зачёт № 2. Опорный конспект № 3
10 Класс. Зачёт № 4. Опорный конспект № 2
Тема “ Первый закон термодинамики”
Пусть
в цилиндре под поршнем находится газ.
Это его первое состояние с внутренней
энергией
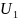 . Внутреннюю энергию этого газа можно
изменить сжатием, т.е. совершая работу
А над газом,
а также передачей газу количества
теплоты Q
. При этом внутренняя энергия газа
изменится и станет
. Внутреннюю энергию этого газа можно
изменить сжатием, т.е. совершая работу
А над газом,
а также передачей газу количества
теплоты Q
. При этом внутренняя энергия газа
изменится и станет
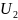 .
Это второе состояние газа.
.
Это второе состояние газа.
 А
А
 газ
газ
газ
газ
Q
Изменение внутренней энергии системы ( газа ) Δ U при переходе из одного состояния в другое равно сумме работы А внешних сил и количества теплоты Q , переданного системе, т. е. Δ U = А + Q
Этот вывод называется первым законом термодинамики.
Следствия из первого закона термодинамики :
- если газ изолирован, то А = 0, Q = 0 , Δ U = 0, т.е. внутренняя энергия не меняется . – если нет теплообмена Q = 0, то Δ U = A, т.е. газ совершает работу за счёт убыли своей внутренней энергии. Это означает, что нельзя создать вечный двигатель. Двигатель перестанет работать, когда запас внутренней энергии закончится.
Применение первого закона термодинамики к изопроцессам.
1. Если над газом осуществляется изохорный процесс, то работа над газом не совершается А = 0 и изменение его внутренней энергии происходит только за счёт передачи газу количества теплоты, т.е. Δ U = Q.
2. Если над газом осуществляется изотермический процесс , то его внутренняя энергия не изменяется Δ U = 0. Полученное количество теплоты газ расходует на совершение работы при расширении 0 = Q + A или Q = - A.
3. Если над газом осуществляется изобарный процесс , то его внутренняя энергия изменяется за счёт полученного количества теплоты и работы, совершённой газом Δ U = Q – A.
4. Если над газом осуществляется адиабатный процесс ( без теплообмена Q=0), то его внутренняя энергия изменяется только за счёт совершения работы Δ U=A. При сжатии газа его внутренняя энергия увеличивается. Если газ сам совершает работу, то его внутренняя энергия уменьшается.
