
- •Прикладная химия
- •Содержание
- •1. Теоретические основы коагуляции коллоидных примесей
- •1.1. Понятие о строении двойного электрического слоя
- •1.2. Устойчивость дисперсных систем
- •1.3. Понятие о гетерокоагуляции и применяемых коагулянтах
- •2. Химические методы очистки сточных вод
- •2.1. Нейтрализация
- •2.1.1. Нейтрализация смешением
- •2.1.2. Реагентная нейтрализация
- •2.1.3. Нейтрализация кислых сточных вод путем их фильтрования через нейтрализующие материалы
- •2.1.4. Нейтрализация щелочных сточных вод кислыми газами
- •2.2. Окислительный метод очистки сточных вод
- •2.2.1. Окисление реагентами, содержащими активный хлор
- •2.2.2. Окисление пероксидом водорода
- •2.2.3. Окисление кислородом воздуха
- •2.2.4. Озонирование
- •2.2.5. Окисление перманганатом калия
- •2.2.6. Радиационное окисление
- •2.3. Очистка восстановлением
- •3. Реагентные методы выделения загрязняющих веществ
- •3.1. Удаление из воды ионов марганца
- •3.2. Удаление ионов железа из поверхностных вод
- •4. Контрольное задание
- •Строение коллоидных частиц
- •Список литературы
2.1.4. Нейтрализация щелочных сточных вод кислыми газами
В процессе нейтрализации щелочных сточных вод используют от-; ходящие газы, содержащие СО2, SO2, N2О3, NО2 и др. При этом происходит нейтрализация сточных вод и одновременная высокоэффективная очистка газов от вредных компонентов, что характерно для ресурсосберегающей (малоотходной) технологии.
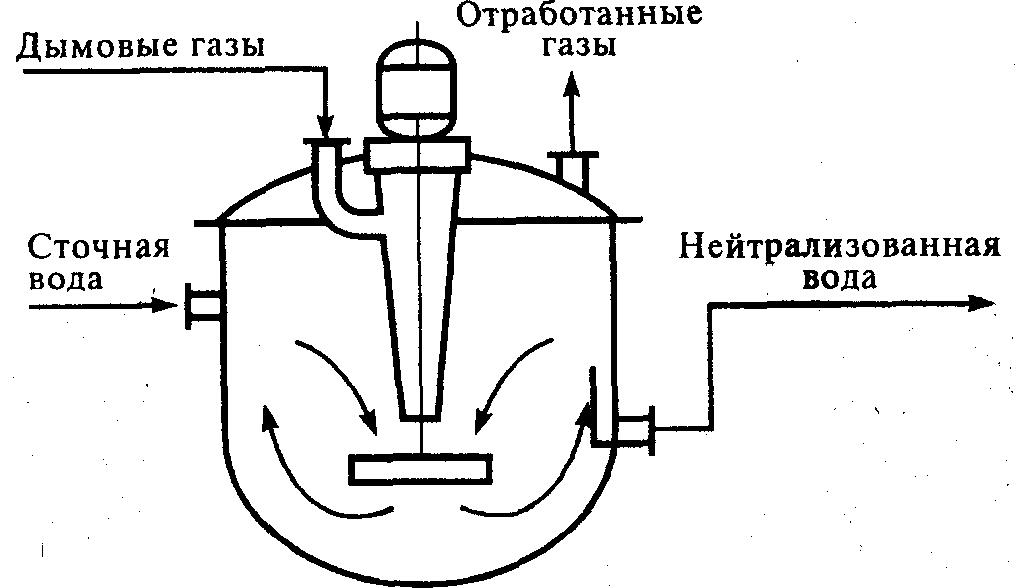
Рис.2. Нейтрализатор щелочных сточных вод дымовыми газами
Преимуществами этой технологии также является исключение использования кислот для нейтрализации, а также возможность создания бессточной схемы водопотребления.
Процесс нейтрализации может быть проведен в реакторах с мешалкой, в распылительных, пленочных и тарельчатых колоннах. Схема реактора с мешалкой для нейтрализации сточных вод дымовыми газами представлена на рис.2.
Нейтрализация щелочных вод дымовыми газами использована в ряде производств, в т. ч. и в асбоцементом производстве.
2.2. Окислительный метод очистки сточных вод
Этот метод очистки используют для обезвреживания производственных сточных вод от цианидов, сероводорода, сульфидов и других веществ. Сточные воды, включающие перечисленные соединения, встречаются в машиностроительной (цехи гальванических покрытий), горнодобывающей (обогатительные фабрики свинцово-цинковых и медных руд), нефтехимической (нефтеперерабатывающие и нефтехимические заводы), целлюлозно-бумажной (цехи варки целлюлозы) и в других отраслях промышленности.
Наиболее часто в практике очистки сточных вод пользуют следующие окислители: хлор, гипохлорит кальция, хлорную известь, диоксид хлора, озон, технический кислород и кислород воздуха. Реже используются пероксид водорода, оксиды марганца, перманганат и бихромат калия.
Для очистки производственных сточных вод возможно также использование процесса радиационного окисления, загрязняющий вещества (обычно органического происхождения) под действием излучений высоких энергий.
2.2.1. Окисление реагентами, содержащими активный хлор
Указанный метод используется для обезвреживания циансодержащих стоков различных объемов и концентраций, а также от таких органических и неорганических соединений, как сероводород, гидросульфид, сульфид, метилмеркаптан и т. д. Следует указать, что сточные воды, содержащие цианиды, образуются при нанесении медных, цинковых и кадмиевых покрытий из цианистых электролитов. Кроме того, циансодержащие стоки образуются при термической закалке стальных изделий в расплавах цианистых солей, а на металлургических предприятиях цианиды попадают в сточные воды из доменных газов (при их промывке и охлаждении). Концентрация простых цианидов (KCN, NaCN) в промывных водах обычно не превышает 200 мг/л. В этих водах также содержатся в небольших количествах комплексные цианиды меди, цинка, кадмия, железа и других веществ.
При введении хлора в воду образуются хлорноватистая и соляная кислоты по реакции
Сl2 + Н2О = НОС1 + НС1
Далее НОС1 диссоциирует, причем степень ее диссоциации зависит от рН. В сильнокислой среде равновесие этой реакции сдвинуто влево, и в воде присутствует Cl2. При рН>4 молекулярный хлор в воде практически отсутствует:
HOCl ↔ H+ + OCI-
Сумма С12 + НОС1 + ОСl- — называется свободным «активным» хлором. Очистка сточных вод от цианидов основана на их окислении в менее токсичные (приблизительно в 1000 раз) цианат — ионы с их последующим гидролизом в нейтральной среде до NH4+ и СО32- по следующим реакциям:
при рН>9- 10 CN- + 2ОH- + Cl2 → CNO- + H2О + 2Cl-
при рН ≈7 СNO- + 2Н2О → NH4+ + СО32-
Образующиеся цианаты можно окислить до элементарного азота и диоксида углерода:
2CNO- + 4OН- + 3Сl → 2СO2↑ + 6Сl- + N2↑ + 2Н2О
При снижении рН возможно протекание реакции прямого хлорирования цианида с образованием токсичного хлорциана.
При использовании в качестве окислителей гипохлоритов реакцию проводят при рН= 10-11
CN- + ОСl- → CNO- + Сl-
Активный хлор окисляет находящиеся в сточных водах соединения аммония, аммиак и органические вещества, содержащие аминогруппы до моно- и дихлораминов, а также до треххлористого азота.
Хлорирование применяется и для дезодорации сточных вод целлюлозно-бумажных комбинатов. Указанные сточные воды содержат сероводород, сульфиды, метилмеркаптан и др.
В щелочной среде хлор окисляет сульфиды до сульфатов. Процесс может быть описан следующим уравнением:
Na2S + 4Сl2 + 8NaOH → Na2SO4 + 8NaCl + 4H2O
Хлораторные установки для очистки сточных вод включают складское хозяйство и устройства для дозирования хлора, в качестве которых чаще всего применяются вакуумные хлораторы.
