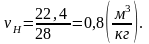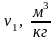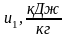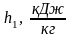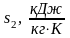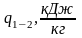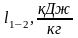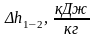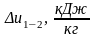- •Техническая термодинамика
- •Газовые процессы
- •1.1.1. Определение недостающих начальных параметров.
- •1.1.2. Определение недостающих конечных параметров.
- •1.1.3. Определение тепла, работы и изменения параметров внутренней энергии, энтальпии и энтропии.
- •1.2.1. Определение недостающих начальных параметров.
- •1.2.2. Определение недостающих конечных параметров.
- •1.2.3. Определение работы и изменения параметров: внутренней энергии, энтальпии и энтропии.
- •Газовые циклы.
- •2.1.1. Определение параметров газа в переходных точках цикла.
- •2.1.2. Определение тепла q, работы l и изменения параметров: внутренней энергии Δu, энтальпии Δh, энтропии Δs, в каждом процессе.
- •2.1.3. Определение полезной работы l, подведённого и отведённого тепла, кпд t (двумя способами).
- •2.2.1. Определение параметров газа в переходных точках цикла.
- •2.2.2. Определение тепла q, работы l и изменения параметров: внутренней энергии Δu, энтальпии Δh, энтропии Δs в каждом процессе.
- •2.2.3 Определение полезной работы l, кпд t (двумя способами).
- •3. Циклы паросиловых установок
- •3.1.6 Расчет термического кпд без промперегрева
- •4. Циклы трансформаторного тепла
- •4.1.1. Расчет удельной холодопроизводительности в цикле.
- •4.1.2. Расчет затраченной работы в цикле.
- •4.1.3. Расчет холодильного коэффициента в цикле.
1.1.2. Определение недостающих конечных параметров.
Определим конечную температуру Т2.
Температуру Т2 найдем из соотношения между параметрами политропного процесса:
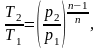 (1.13)
(1.13)
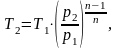 (1.14)
(1.14)
где Т2 – конечная температура, К;
р2 – конечное давление, Па;
n – показатель политропы.
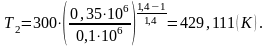
Найдём конечный объем v2.
Из формулы (1.5) для данного случая найдем конечный объем v2:
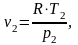 (1.15)
(1.15)
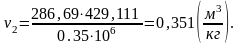
Определим конечную внутреннюю энергию u2.
Аналогично u1 найдем конечную внутреннюю энергию u2 по формуле:
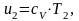 (1.16)
(1.16)
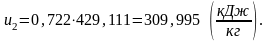
Определим энтальпию h2 в конце процесса.
Аналогично h1 найдем энтальпию h2 в конце процесса по формуле:
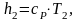 (1.17)
(1.17)
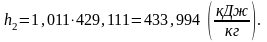
Найдём энтропию s2 в конце процесса.
Аналогично s1 находим энтропию s2 в конце процесса по формуле:
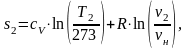 (1.18)
(1.18)
где v2 – конечный объем, м3/кг,
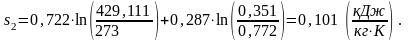
1.1.3. Определение тепла, работы и изменения параметров внутренней энергии, энтальпии и энтропии.
Определим тепло q1-2 в данном процессе.
Количество тепла в политропном процессе рассчитывается по формуле:
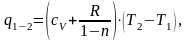 (1.19)
(1.19)
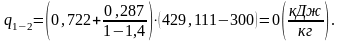
Вычислим работу l1-2 в данном процессе.
Для политропного процесса работа рассчитывается по формуле:
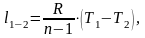 (1.20)
(1.20)
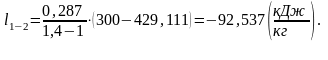
Определим изменение внутренней энергии ∆u1-2 .
Изменение внутренней энергии можно рассчитать по формулам:
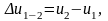 (1.21)
(1.21)
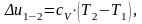 (1.22)
(1.22)
∆u1-2 находим по формуле (1.22):
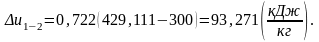
Определим изменение энтальпии ∆h1-2.
Аналогично изменение внутренней энергии ∆u1-2 можно рассчитать изменение энтальпии ∆h1-2 по формулам:
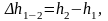 (1.23)
(1.23)
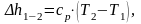 (1.24)
(1.24)
∆h1-2 находим по формуле (1.24):
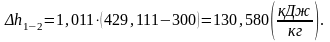
Определим изменение энтропии ∆s1-2.
Как и изменение внутренней энергии, изменение энтропии ∆s1-2 можно расчитать:
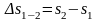 ,
(1.25)
,
(1.25)
или
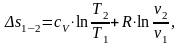 (1.26)
(1.26)
∆s1-2 находим по формуле (1.26):
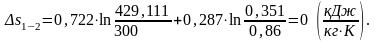
Все ответы приведены в таблице 1.1
Таблица 1.1 – Результаты начальных и конечных параметров, тепло, работа, изменение параметров.
Неизвестные параметры |
Р1, МПа |
Т1, К |
|
|
|
|
Полученный результат |
0,1 |
300 |
0,86 |
216,724 |
303,414 |
0,099 |
Продолжение таблицы 1.1 – Результаты начальных и конечных параметров, тепло работа, изменение параметров.
Неизвестные параметры |
Р2, МПа |
Т2, К |
|
|
|
|
Полученный результат |
0,35 |
429,111 |
0,351 |
309,995 |
433,994 |
0,101 |
Окончание таблицы 1.1 – Результаты начальных и конечных параметров, тепло, работа, изменение параметров.
Неизвестные параметры |
|
|
|
|
|
Полученный результат |
0 |
-92,537 |
130,580 |
93,271 |
0 |
Таблица 1.2 - Промежуточные точки для p,v – диаграммы.
Точки |
Давление р,МПа |
Удельный
объём
|
A |
0,119 |
0,76 |
B |
0,145 |
0,66 |
C |
0,182 |
0,56 |
D |
0,24 |
0,46 |
E |
0,292 |
0,4 |
Т,s – диаграмму строим по двум точкам: 1и 2.
Вывод: Адиабатный процесс носит частный характер, так как здесь накладывается ограничение: изменение количества тепла в процессе равно нулю.
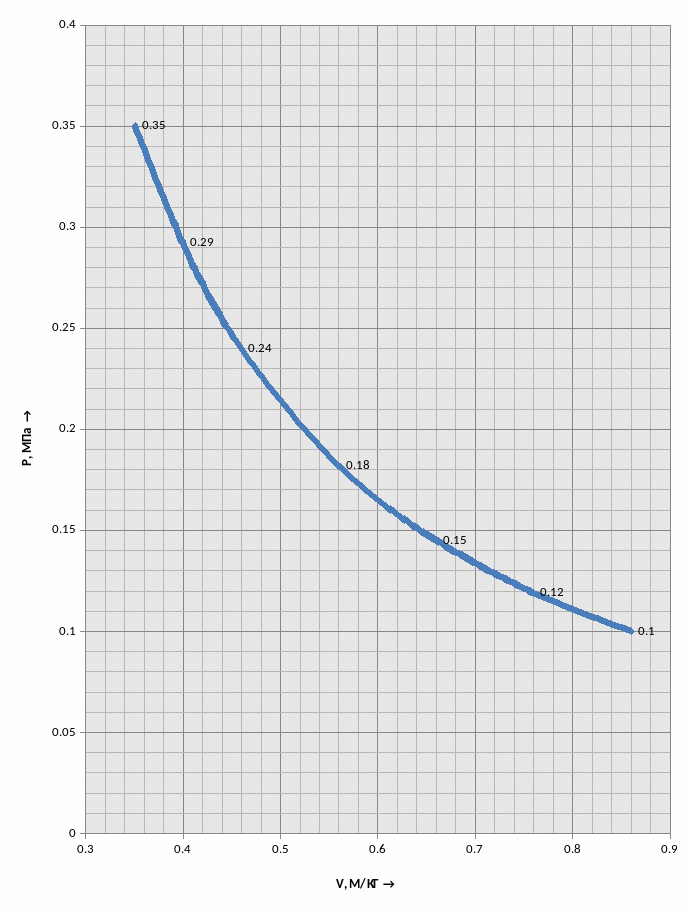
Рисунок 1.1.- Диаграмма в p,v – координатах.

Рисунок 1.2. – Диаграмма в T,S – координатах.
1 .2. Задача 2. В процессе 1-2 с показателем политропы n к 1 кг газа с начальными параметрами р1 = 0,1МПа, Т1 = 300 К подводится тепло q. Определить недостающие начальные параметры v1, u1, h1, s1, конечные параметры р2, Т2, v2, u2, h2, s2, изменение параметров в процессе ∆u1-2, ∆h1-2, ∆s1-2 и работу l1-2. Построить процесс в p, v – и T, s – диаграммах.
Дано: "СИ"
газ СО
процесс
политропный
Т1 = 300 К
р1 = 0.1 МПа .
q
= 600 кДж/кг

n = 4,2
m =1 кг
Найти:
v1, u1, h1, s1, р2,
T2, v2, u2, h2, s2,
l1-2, ∆u1-2, ∆h1-2,
∆s1-2.
Решение:
Для расчетов неизвестных параметров необходимо рассчитать газовую постоянную. Газовая постоянная является индивидуальной для каждого газа, то есть зависит от молекулярной массы газа и рассчитывается по формуле:
(1.27)
где см – это кажущаяся молекулярная масса, она зависит от пропорции компонентов, из которых состоит смесь газа. В данном случае имеется газ СО, и для него газовая постоянная будет равна:
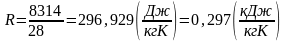 .
.
Так же понадобится для расчетов изобарная (ср) и изохорная (сv) теплоемкости. Так как данный газ - двухатомный, следовательно изобарная теплоемкость равна:
(1.28)
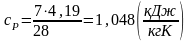
а изохорная теплоемкость равна:
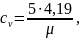 (1.29)
(1.29)
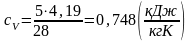 .
.
Объем при нормальных условиях будет равен:
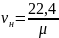 , (1.30)
, (1.30)