
- •Оглавление
- •Программа блока гетерофункциональные углеводороды.
- •Конспект лекций гетерофункциональные углеводороды
- •Углеводы
- •1.1 Моноуглеводы
- •Химическое строение моносахаридов
- •1. Реакции карбонильных форм моносахаридов
- •2.2 Реакции с участием всех гидроксильных групп
- •Олигосахариды
- •1.2.1 Дисахариды
- •1.2.3 Несахароподобные полисахариды
- •1.2.3.1 Гомополисахариды
- •1.2.3.2 Гетерополисахариды
- •2. Аминокислоты
- •Получение α-аминокислот
- •Аминирование эфиров α-галогензамещённых кислот (по Габриэлю) – фталимидный синтез:
- •Кислотно-основные свойства аминокислот
- •Комплексные соли с ионами меди
- •Образование сложных эфиров (этерификация).
- •Действие окислителей.
- •4. Гетероциклические соединения
- •4.1 Пятичленные гетероциклы с одним гетероатомом
- •6. Реакция диенового синтеза с малеиновым ангидридом
- •2. Пиролизом:
- •3. Реакция электрофильного замещения (механизм и ориентация замещения):
- •1. Индол обладает слабоосновными свойствами и в то же время слабокислыми, образует металлические производные – индол-калий, индол-натрий:
- •4.2 Пятичленные гетероциклы с несколькими гетероатомами
- •4.3 Шестичленные гетероциклы с одним гетероатомом
- •4.4 Шестичленные гетероциклы с несколькими гетероатомами
- •1. Основные свойства:
- •2. Свойства, обусловленные функциональными группами, в том числе групповые реакции:
- •4.4 Шестичленные гетероциклы с двумя разными гетероатомами
- •Нобелевские премии по органической химии
- •Список использованной литературы
Кислотно-основные свойства аминокислот
Аминокислоты – амфотерные вещества, которые могут существовать в виде катионов или анионов. Это свойство объясняется наличием как кислотной (–СО2Н), так и основной (–NH2) группы в одной и той же молекуле.

В очень кислых растворах NH2-гpyппa аминокислоты протонируется, и эта кислота становится катионом. В сильнощелочных растворах карбоксильная группа аминокислоты депротонируется и кислота превращается в анион.
В твердом состоянии аминокислоты существуют в виде цвиттер-ионов (известных также под названием диполярных ионов или внутренних солей). В подобных цвиттер-ионах протон переносится от карбоксильной группы к аминогруппе.

Если поместить аминокислоту в среду, обладающую проводимостью, и опустить туда пару электродов, то в кислых растворах аминокислота будет мигрировать к катоду, а в щелочных растворах – к аноду. При некотором значении рН, характерном для данной аминокислоты, она не будет передвигаться ни к катоду, пи к аноду, так как каждая молекула находится в виде цвиттер-иона (иными словами, она несет как положительный, так и отрицательный заряды). Это значение рН называется изоэлектрической точкой (pI) данной аминокислоты (таблица 2). Изоэлектрическая точка аминокислот редко равна 7, так как зависит от кислотности иона алкиламмония, оснoвности карбоксилат-аниона, влияния на них радикала и присутствия любой дополнительной основной или кислотной группы.
При пропускании постоянного тока через раствор, содержащий смесь нескольких аминокислот, каждая из них будет двигаться к катоду или аноду со скоростью, зависящей от природы этой аминокислоты и от рН среды. Разделение и анализ смесей аминокислот, oснованные на этом явлении, называются электрофорезом.
Аминокислоты как биполярные ионы. Хотя аминокислоты обычно изображают как соединения, содержащие амино- и карбоксильную группу H2NCHRCOOH, некоторые их свойства, как физические, так и химические, не согласуются с этой структурой:
в противоположность аминам и карбоновым кислотам аминокислоты представляют собой нелетучие кристаллические вещества, плавящиеся с разложением при довольно высокой температуре;
они не растворимы в неполярных растворителях типа петролейного эфира, бензола или эфира и заметно растворимы в воде;
их водные растворы ведут себя подобно растворам веществ с высоким дипольным моментом;
константы кислотности и основности для групп СООН и NH2 необычайно малы.
Все эти свойства вполне соответствуют структуре диполярного иона для аминокислот H3N+–CHR–COO–. Физические свойства – температура плавления, растворимость, высокие дипольные моменты – отвечают ожидаемым для подобных солей. Кислотно-основные свойства также становятся понятными, если учесть, что измеряемая Ка в действительности относится к кислотности иона аммония RNH3+
![]()
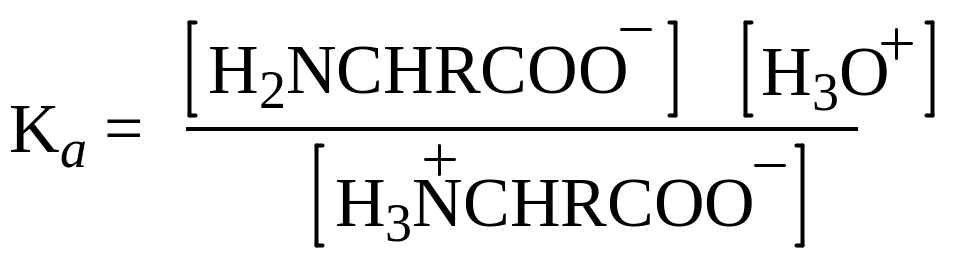
а Кb в действительности относится к основности карбоксилат-иона

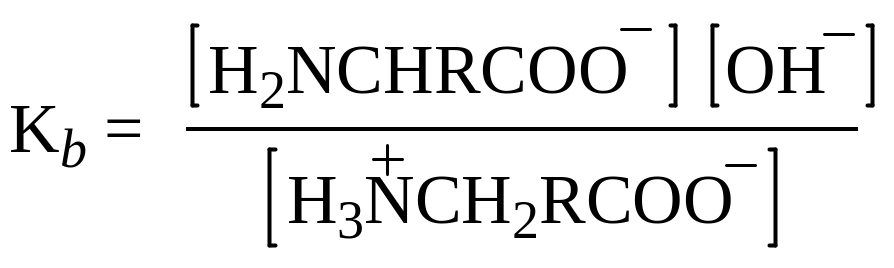
В водном растворе кислотность и основность кислоты и ее сопряженного основания (например, СН3СООН и СН3СОО– или СH3NH3+ и CH3NH2) связаны уравнением Ка·Кb = 10-14. На этом основании можно рассчитать, что Ка = 1,6 ·10–10 для NH3+-группы глицина означает Кb = 6,3 ·10-5для NН2-группы, что кажется вполне приемлемой величиной для алифатического амина. Аналогично Кb = 2,5 ·10–12 для группы СОО– глицина означает, что Ка = 4 ·10–3 для СООН-группы, что кажется вполне приемлемой величиной для карбоновой кислоты, содержащей сильную электроноакцепторную (увеличивающую кислотность) NH3+-гpyппy.
При подщелачивании раствора аминокислоты диполярный ион I превращается в анион II; более сильное основание, гидроксил-ион, отрывает протон от иона аммония и вытесняет более слабое основание — амин

Если подкислить раствор аминокислоты, то диполярный ион I превращается в катион III; более сильная кислота Н3О+ отдает протон карбоксилат-иону и вытесняет более слабую карбоновую кислоту

Итак, кислой группой в простых аминокислотах типа глицина является не СООН–, a NH3-гpyппa, а основной — не NH2-гpyппa, а группа COО–.
Необходимо иметь в виду, что ионы II и III, содержащие свободную NH2- или СООН-группу, находятся в равновесии с диполярным ионом I; поэтому аминокислоты вступают в реакции, характерные для аминов и карбоновых кислот. По мере удаления иона II, например при реакции с бензоилхлоридом, равновесие сдвигается в сторону образования иона II, так что постепенно аминокислота полностью бензоилируется.

В тех случаях, когда это возможно, желаемую реакцию можно ускорить, создавая нужную концентрацию кислоты или основания в растворе так, чтобы увеличить концентрацию реакционноспособной частицы.
Изоэлектрическая точка аминокислот
Если раствор аминокислоты поместить в электрическое поле, то в зависимости от кислотности или основности раствора будет наблюдаться различная картина. В сильнощелочном растворе концентрация анионов II превышает концентрацию катионов III и наблюдается миграция аминокислоты по направлению к аноду.

В сильнокислом растворе имеется значительный избыток катионов III и будет наблюдаться миграция аминокислоты к катоду. Если концентрации ионов II и III равны друг другу, то не будет наблюдаться никакого видимого движения; в этих условиях любая молекула одно и то же время проводит в состоянии и катиона и аниона, поэтому любое незначительное смещение в направлении одного из электродов немедленно компенсируется равным смещением в направлении другого электрода. Концентрация ионов водорода, при которой данная аминокислота не движется под влиянием электрического поля, называется изоэлектрической точкой данной аминокислоты.
Моноаминомонокарбоновая кислота H3N+CHRCOO– имеет несколько большую величину кислотности по сравнению с основностью (например, для глицина Ка — 1,6 · 10–10, а Кь = 2,5 · 10–12). Если кристаллы такой аминокислоты прибавить к воде, то образующийся раствор будет содержать больше анионов II (H2NCHRCOO–), чем катионов III (H3N+CHRCOOH). Эту «избыточную» ионизацию иона аммония в амин (I < = > II + Н+) можно подавить прибавлением кислоты для того, чтобы была достигнута изоэлектрическая точка, которая вследствие этого будет несколько сдвинута в область кислых значений рН. Например, для глицина изоэлектрическая точка лежит при рН 6,1. Аминокислота обычно обнаруживает самую низкую растворимость в растворе при изоэлектрической точке, поскольку при этом концентрация диполярного иона максимальна. Если же раствор будет более щелочным или более кислым, то тем самым увеличивается концентрация одного из более растворимых ионов (II или III).
