
- •Наукова робота з лабораторної роботи №5
- •1.Загальні положення
- •2.Властивості ферментів
- •Вплив рН середовища на активність ферментів.
- •3.Специфічність дії ферментів.
- •3.Будова ферментів
- •4.Класифікація ферментів
- •5.Характеристика окремих класів ферментів та їх промислове використання Оксидоредуктази
- •Трасферази
- •6.Структура і механізм дії ферментів.
- •6. Крохмаль. Склад молекули. Поширення в природі та застосування.
- •8.Фізичні та хімічні властивості амілази
- •9.Значення крохмалю в хлібопекарському виробництві.
- •9. Визначення амілолітичної (декстринуючої) активності.
- •11.Хід роботи
- •13.Графік
- •14. Висновки
- •14. Література.
Трасферази
Найважливішими представниками цього класу є:
1. Фосфортрансферази (кінази) здійснюють перенесення фосфатного залишку від АТФ на різні речовини і, навпаки, від фосфорильованої речовини на АДФ з утворенням АТФ. Ці процеси мають велике значення в енергетичному обміні. Фосфорилювання глюкози за рахунок АТФ є першим і обов’язковим етапом всіх процесів перетворення цього вуглеводу.

Стрептокіназу та урокіназу застосовують для розсмоктування тромбів.
2.Глікозилтрансферази каталізують перенесення залишків вуглеводів.
До цього підкласу належать ферменти фосфорилази, які каталізують перетворення крохмалю чи глікогену у глюкозо-1-фосфат за участі фосфорної кислоти, тобто перенесення глюкозильного залишку на фосфорну кислоту. В результаті відбувається взаємоперетворення вуглеводів. Такий процес розкладу поліцукридів називається фосфоролізом. Він аналогічний гідролізу, але роль води виконує фосфорна кислота. На відміну від гідролаз фосфорилази здійснюють і зворотний процес - синтез складних вуглеводів, переносячи залишки моноцукрів від їх фосфорних ефірів на вуглеводи.
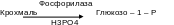
6.Структура і механізм дії ферментів.
Молекулярні процеси, які відбуваються під час біокаталізу, досить детально вивчені і поділяються на три стадії:
1 стадія. Субстрат зближується з активним центром ферменту і орієнтується по відношенню до каталітичної групи. Відбувається зв’язування субстрату в активному центрі. Орієнтуюча група субстрату і зв’язуюча ділянка активного центру мають просторову і хімічну відповідність.
2 стадія. Один з перших дослідників білків Е.Фішер вважав, що фермент «жорстко» відповідає за формулою субстрату, як замок борідці ключа. Але ця модель не пояснює механізму активації субстрату. Сучасна модель відповідності ферменту і субстрату пояснює її так: фермент звязаний з субстратом, деформується і пристосовується до нього, як рукавичка до руки. Виникає індукована відповідність між ферментом і субстратом. Напруження передається від ферменту до субстрату і комплекс переходить в активний стан. Енергія активації субстрату в цьому комплексі значно менша, ніж у відсутності каталізатора.
3 стадія. Відбуваються хімічні взаємодії між активованим субстратом і функціональними групами активного центру. Виділяється два види взаємодії: кислотно-основні і ковалентні. Кислотно-основні взаємодії здійснюють ферменти, в активних центрах яких містяться радикали амінокислот, що можуть виступати акцепторами або донорами протонів.
6. Крохмаль. Склад молекули. Поширення в природі та застосування.
Крохмаль представляє собою суміш двох гомополісахаридів: лінійного – амілози та розгалуженого – амілопектину. Вміст амілози 10 – 30 %, амілопектину 70 – 90 %. Полісахариди крохмалю збудовані із залишків -D-глюкози, що поєднані в амілозі і в лінійних ланцюгах амілопектину -1,4-зв’язками, а в точках розгалуження амілопектину міжланцюговими -1,6-зв’язками. При додаванні йоду амілоза забарвлюється в синій колір, амілопектин – в червоно-фіолетовий. Молекулярна маса крохмалю 105 – 107 Да. Амілоза розчиняється у гарячій воді, амілопектин у воді утворює клейстер. Склад молекули крохмалю виражається формулою (C6H10O5)n. Це природний полімер, що синтезується в рослинах з глюкози:
nC6H12O6 → (C6H10O5)n + nH2O.
Полімерні ланцюги крохмалю неоднорідні. Серед них є лінійні та розгалужені, довгі та короткі. Число ланок у полімері коливається від кількох сотень до п’яти тисяч і більше. Крохмаль поширений у природі. Для різних рослин він запасний поживний матеріал і міститься в них у вигляді крохмальних зерен. Масова частка його у бульбах картоплі становить приблизно 20 %, у зернах пшениці – близько 70 %, рису – близько 80 %. Крохмаль – білий порошок, що не розчиняється в холодній воді. У гарячій воді він набрякає, утворюючи клейстер. Характерною реакцією на крохмаль є утворення синього забарвлення при взаємодії з розчином йоду. Найважливіша хімічна властивість крохмалю – його гідроліз. Кінцевим продуктом гідролізу є глюкоза:
(C6H10O5)n + nH2O → nC6H12O6.
Проміжні продукти гідролізу крохмалю – суміш декстринів і глюкози (патоку) використовують у кондитерській промисловості для виготовлення цукерок, додають у тісто для випікання пряників. Крохмаль є сировиною для виробництва етилового спирту. У текстильній промисловості крохмаль використовують для проклеювання тканин, у паперовій – для склеювання паперу і картону, у медицині – для виготовлення присипок, паст, капсул для лікарських препаратів. Резервний гомополісахарид рослин. Види крохмалю: картопляний, кукурудзяний, амілопектиновий кукурудзяний, пшеничний, рисовий, гороховий, тапіоковий, модифікований і ін.
