
- •Научные методы познания окружающего мира; роль эксперимента и теории в процессе познания природы; моделирование явлений и объектов природы.
- •Электрическая ёмкость: электроёмкость конденсатора; энергия электрического поля.
- •Задача на применение законов сохранения импульса.
- •Билет 2
- •Научные гипотезы; физические законы и теории, границы их применимости.
- •Электрический ток. Последовательное и параллельное соединения проводников. Электродвижущая сила (эдс). Закон Ома для полной электрической цепи.
- •3.Экспериментальное задание: «Измерение длины световой волны с помощью дифракционной решетки».
- •Механическое движение и его относительность; уравнения прямолинейного равноускоренного движения.
- •Электрический ток в газах: несамостоятельный разряд в газах; самостоятельный электрический разряд; виды самостоятельного разряда; плазма.
- •3.Задача на применение уравнения состояния идеального газа
- •Движение по окружности с постоянной по модулю скоростью; период и частота; центростремительное ускорение.
- •2.Электрический ток в растворах и расплавах электролитов: закон Фарадея; определение заряда одновалентного иона; технические применения электролиза.
- •Задача на применение газовых законов.
- •Первый закон Ньютона: инерциальная система отсчёта.
- •Экспериментальное задание: «Измерение влажности воздуха с помощью психрометра».
- •Второй закон Ньютона: понятие о массе и силе, принцип суперпозиции сил; формулировка второго закона Ньютона; классический принцип относительности.
- •Магнитное поле: понятие о магнитном поле; магнитная индукция; линии магнитной индукции, магнитный поток; движение заряженных частиц в однородном магнитном поле.
- •Экспериментальное задание: «Построение графика зависимости температуры от времени остывания воды».
- •Третий закон Ньютона: формулировка; характеристика сил действия и противодействия: модуль, направление, точка приложения, природа.
- •Закон электромагнитной индукция Фарадея; правило Ленца; явление самоиндукции; индуктивность; энергия магнитного поля.
- •Экспериментальное задание: «Исследование зависимости периода и частоты свободных колебаний математического маятника от длинны нити».
- •Колебательный контур. Свободные электромагнитные колебания: затухание свободных колебаний; период электромагнитных колебаний.
- •Экспериментальное задание: «Определение показателя преломления пластмассы».
- •1. Закон всемирного тяготения. Сила тяжести, вес и невесомость.
- •Автоколебания: автоколебательная система; автоколебательный генератор незатухающих электромагнитных колебаний.
- •Силы упругости: природа сил упругости; виды упругих деформаций; закон Гука.
- •3.Задача на применение закона радиоактивного распада
- •Силы трения: природа сил трения; коэффициент трения скольжения; закон сухого трения; трение покоя; учёт и использование трения в быту и технике.
- •Трансформатор: принцип трансформации переменного тока; устройство трансформатора; холостой ход; режим нагрузки; передача электрической энергии.
- •3.Экспериментальное задание: «Исследование последовательного соединения проводников».
- •Равновесие твёрдых тел: момент силы; условия равновесия твёрдого тела; устойчивость тел; виды равновесия; принцип минимума потенциальной энергии.
- •2.Электромагнитное поле. Открытие электромагнитных волн: гипотеза Максвелла; экспериментальное; опыты Герца.
- •Экспериментальное задание: «Измерение эдс и внутреннего сопротивления источника тока2.
- •Механическая работа. Мощность. Энергия: кинетическая энергия; потенциальная энергия тела в однородном поле тяготения и энергия упруго деформированного тела; закон сохранения энергии.
- •Задача на применение закона сохранения энергии.
- •Билет 14
- •.1.Закон Паскаля; закон Архимеда; условия плавания тел.
- •Свет как электромагнитная волна. Скорость света. Интерференция света: опыт Юнга; цвета тонких плёнок.
- •Задача на расчет работы и мощности тока.
- •2. Дифракция света: явление дифракции света; явления, наблюдаемые при пропускании света через отверстия малых размеров; дифракция на малом отверстии и от круглого экрана. Дифракционная решётка.
- •Задача на движение заряженной частицы в магнитном поле
- •Гипотеза Планка о квантах; фотоэффект; опыты а.Г.Столетова; уравнение Эйнштейна для фотоэффекта; фотон.
- •Задача на применение закона электромагнитной индукции
- •Законы отражения и преломления света; полное внутреннее отражение; линзы; формула тонкой линзы; оптические приборы.
- •Задача по теме «Вес движущегося тела».
- •Постулаты специальной теории относительности (сто). Полная энергия. Энергия покоя. Релятивистский импульс.
- •Задача на применение закона всемирного тяготения
- •Билет 19
- •Модель строения жидкостей. Насыщенные и ненасыщенные пары; зависимость давления насыщенного пара от температуры; кипение. Влажность воздуха; точка росы, гигрометр, психрометр.
- •Дисперсия и поглощение света; спектроскоп и спектрограф. Различные виды электромагнитных излучений и их практическое применение. Дисперсия
- •Задача по теме «Кинематика»
- •Билет 20
- •Опыт Резерфорда; ядерная модель атома; квантовые постулаты Бора; гипотеза де Бройля о волновых свойствах частиц; дифракция электронов; лазеры.
- •Экспериментальное задание: «Измерение модуля упругости резины».
- •Модели строения атомного ядра; ядерные силы; нуклонная модель ядра; энергия связи ядра; ядерные спектры; ядерные реакции.
- •1. Тепловые машины: основные части и принципы действия тепловых машин; коэффициент полезного действия тепловой машины и пути его повышения; проблемы энергетики и охрана окружающей среды.
- •2. Радиоактивность; радиоактивные излучения; закон радиоактивного распада.
- •Задача на расчёт параметров колебательного контура
- •Необратимость тепловых процессов; второй закон термодинамики и его статистическое истолкование.
- •3. Экспериментальное задание: «Измерение ускорения свободного падения с помощью математического маятника».
- •Солнечная система. Звёзды и источники их энергии. Современные представления о происхождении и эволюции Солнца и звёзд.
- •Малые тела Солнечной системы.
- •2. Виды звезд.
- •3. Взрывы и эволюция звезд.
- •Задача на применение первого закона термодинамики.
- •Наша Галактика. Другие галактики. Пространственные масштабы наблюдаемой Вселенной. Применимость законов физики для объяснения природы космических объектов.
- •5. Будущее Вселенной.
- •Экспериментальное задание: «Исследование параллельного соединения проводников».
- •«Красное смещение» в спектрах галактик. Современные взгляды на строение и эволюцию Вселенной.
- •3. Задача по теме «Кинематика»
Законы отражения и преломления света; полное внутреннее отражение; линзы; формула тонкой линзы; оптические приборы.
Если
световой пучок падает на поверхность,
разделяющую две прозрачные среды разной
оптической плотности, например воздух
и воду, то часть света отражается от
этой поверхности, а другая часть —
проникает во вторую среду. При переходе
из одной среды в другую луч света изменяет
направление на границе этих сред. Это
явление закреплено в законе отражения
и преломлением света: « Луч падающий,
отраженный и перпендикуляр, восстановленный
в точке падения луча лежат в одной
плоскости. Угол падения равен углу
отражения», и « Луч падающий, преломленный
и перпендикуляр, восстановленный в
точке падания луча, лежат в одной
плоскости. Отношение синуса угла падения
к синусу угла преломления есть величина
постоянная для двух сред и называется
показателем преломления второй среды
относительно первой».
![]() ,
где
,
где![]() -
относительный показатель преломления
(показатель преломления второй среды
относительно первой),
-
относительный показатель преломления
(показатель преломления второй среды
относительно первой), ![]() -угол
падения,
-угол
падения, ![]() -угол
преломления,
-угол
преломления, ![]() -скорость
распространения света в первой среде,
-скорость
распространения света в первой среде, ![]() -
скорость распространения света во
второй среде.
-
скорость распространения света во
второй среде.
При некотором значении угла падения, угол преломления станет равным 900, т.е. наступит полное отражение света.
Линзой называют прозрачное тело, ограниченное сферическими поверхностями. Линзы бывают выпуклые и вогнутые. Выпуклая линза является собирающей, а вогнутая – рассеивающей. Любая линза имеет фокус – точку, в которой собираются все лучи, прошедшие через линзу и оптическую силу – величину обратную фокусному расстоянию. Если перед линзой расположить некоторый предмет, то можно построить его изображение, используя формулу тонкой линзы.
1 / d + 1 / f = 1 /F,где d – расстояние от предмета до линзы, f – расстояние от линзы до изображения, F – фокусное расстояние.
Задача по теме «Вес движущегося тела».
Билет № 18
Связь между давлением идеального газа и средней кинетической энергией теплового движения его молекул. Уравнение состояния идеального газа. Изопроцессы Состояние данной массы газа полностью определено, если известны его давление, температура и объем. Эти величины называют параметрами состояния газа. Уравнение, связывающее параметры состояния, называют уравнением состояния. Для произвольной массы газа состояние газа описывается уравнением Менделеева—Клапейрона: pV = mRT/M, где р — давление, V — объем, m — масса, М — молярная масса, R — универсальная газовая постоянная. Физический смысл универсальной газовой постоянной в том, что она показывает, какую работу совершает один моль идеального газа при изобарном расширении при нагревании на 1 К (R = 8,31 ДжДмоль • К)). Уравнение Менделеева—Клапейрона показывает, что возможно одновременное изменение трех параметров, характеризующих состояние идеального газа. Однако многие процессы в газах, происходящие в природе и осуществляемые в технике, можно рассматривать приближенно как процессы, в которых изменяются лишь два параметра. Особую роль в физике и технике играют три процесса: изотермический, изохорный и изобарный. Изопроцессом называют процесс, происходящий с данной массой газа при одном постоянном параметре — температуре, давлении или объеме. Из уравнения состояния как частные случаи получаются законы для изопроцессов. Изотермическим называют процесс, протекающий при постоянной температуре. Т = const. Он описывается законом Бойля—Мариотта: pV = const. Изохорным называют процесс, протекающий при постоянном объеме. Для него справедлив закон Шарля: V = const, p/T = const. Изобарным называют процесс, протекающий при постоянном давлении. Уравнение этого процесса имеет вид V/T = const прир = const и называется законом Гей-Люссака. Все процессы м
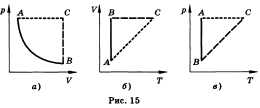 ожно
изобразить графически (рис. 15).
Реальные газы удовлетворяют уравнению
состояния идеального газа при не слишком
высоких давлениях (пока собственный
объем молекул пренебрежительно мал по
сравнению с объемом сосуда, в котором
находится газ) и при не слишком низких
температурах (пока потенциальной
энергией межмолекулярного взаимодействия
можно пренебречь по сравнению с
кинетической энергией теплового
движения молекул), т. е. для реального
газа это уравнение и его следствия
являются хорошим приближением.
ожно
изобразить графически (рис. 15).
Реальные газы удовлетворяют уравнению
состояния идеального газа при не слишком
высоких давлениях (пока собственный
объем молекул пренебрежительно мал по
сравнению с объемом сосуда, в котором
находится газ) и при не слишком низких
температурах (пока потенциальной
энергией межмолекулярного взаимодействия
можно пренебречь по сравнению с
кинетической энергией теплового
движения молекул), т. е. для реального
газа это уравнение и его следствия
являются хорошим приближением.
