
4. Дисперсное состояние вещества
Дисперсные системы. Кристаллы любого вещества, например сахара или хлорида натрия, можно получить разного размера—крупные и мелкие. Каков бы ни был размер кристаллов, все они имеют одинаковую для данного вещества внутреннюю структуру—молекулярную или ионную кристаллическую решетку.
При растворении в воде кристаллов сахара и хлорида натрия Образуются соответственно молекулярные и ионные растворы. Таким образом, одно и то же вещество может находиться в различной степени раздробленности: макроскопически видимые частицы (>0,2—0,1 мм, разрешающая способность глаза), микроскопически видимые частицы (от 0,2—0,1 мм до 400— 300 нм, разрешающая способность микроскопа при освещении белым светом) и в молекулярном (или ионном) состоянии.
Постепенно складывались представления о том, что между миром молекул и микроскопически видимых частиц находится область раздробленности вещества с комплексом новых свойств, присущих этой форме организации вещества.
Представим себе кубик какого-либо вещества, который будем разрезать параллельно одной из его плоскостей, затем полученные пластинки начнем нарезать на палочки, а последние—на кубики. В результате такого диспергирования (дробления) вещества получаются пленочно-, волокнисто- и корпускулярнодис-персные (раздробленные) системы. Если толщина пленок, поперечник волокон или частиц (корпускул) меньше разрешающей способности оптического микроскопа, то они не могут быть обнаружены с его помощью. Такие невидимые в оптический микроскоп частицы называют коллоидными, а раздробленное (диспергированное) состояние веществ с размером частиц от 400—300 нм до 1 нм—коллоидным состоянием вещества.
Дисперсные (раздробленные) системы являются гетерогенными. Они состоят из сплошной непрерывной фазы—дисперсионной среды и находящихся в этой среде раздробленных частиц того или иного размера и формы—дисперсной фазы.
Поскольку дисперсная (прорывная) фаза находится в виде отдельных небольших частиц, то дисперсные системы, в отличие от гетерогенных со сплошными фазами, называют микрогетероген-ными, а коллоидноднсперсные системы называют также ультра-микрогетерогенными, чтобы подчеркнуть, что в этих системах граница раздела фаз не может быть обнаружена в световом микроскопе.
Когда вещество находится в окружающей среде в виде молекул или ионов, то такие растворы называют истинными, т. е. гомогенными однофазными растворами.
Обязательным условием получения дисперсных систем является взаимная нерастворимость диспергируемого вещества и дисперсионной среды. Например, нельзя получить коллоидные растворы сахара или хлорида натрия в воде, но они могут быть получены в керосине или в бензоле, в которых эти вещества практически нерастворимы.
Дисперсные системы классифицируют по дисперсности, агрегатному состоянию дисперсной фазы и дисперсионной среды, интенсивности взаимодействия между ними, отсутствию или образованию структур в дисперсных системах.
Количественной характеристикой дисперсности (раздробленности) вещества является степень дисперсности (степень раздробленности, D)—величина, обратная размеру (а) дисперсных частиц:
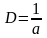
Здесь а равно либо диаметру сферических или волокнистых частиц, либо длине ребра кубических частиц, либо толщине пленок.
Степень дисперсности численно равна числу частиц, которые можно плотно уложить в ряд (или в стопку пленок) на протяжении одного сантиметра.
Если все частицы дисперсной фазы имеют одинаковые размеры, то такие системы называют монодисперсными. Частицы дисперсной фазы неодинакового размера образуют полидисперсные системы. С повышением дисперсности все большее и большее число атомов вещества находится в поверхностном слое, на границе раздела фаз, по сравнению с их числом внутри объема частиц дисперсной фазы. Соотношение между поверхностью и объемом характеризует удельная поверхность: Sуд==S/V, которая для частиц сферической формы равна
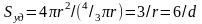
а для частиц кубической формы
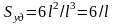
где r—радиус шара; d—его диаметр; l—длина ребра куба.
Так, удельная
поверхность вещества, раздробленного
до микронных кубиков, составляет
6-104
см-1.
При этом из 1 см3
образуется 1012
микронных кубиков с суммарной поверхностью
(S
=Sуд-V),
равной 6-104
см2
(6 м2).
При дальнейшем дроблении 1 см3
вещества до кубиков коллоидной
дисперсности, например с длиной ребра
l = 10-6
см (10 нм), их число достигает 1018
частиц, суммарная поверхность—6*106
см2
(600 м2),
а удельная поверхность—6*106
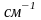 .
.
Следовательно, с повышением дисперсности вещества все большее значение имеют его свойства, определяемые поверхностными явлениями, т. е. совокупностью процессов, происходящих в межфазовой поверхности. Таким образом, своеобразие дисперсных систем определяется большой удельной поверхностью дисперсной фазы и физико-химическим взаимодействием дисперсной фазы и дисперсионной среды на границе раздела фаз.
Дисперсные системы с газообразной дисперсионной средой называют аэрозолями. Туманы представляют собой аэрозоли с жидкой дисперсной фазой (Г1—Ж2), а пыль и дым—аэрозоли с твердой дисперсной фазой (Г1—Т2); пыль образуется при днспергированни веществ, а дым—при конденсации летучих веществ.
Пены—это дисперсия газа в жидкости (Ж1—Г2), причем в пенах жидкость вырождается до тонких пленок, разделяющих отдельные пузырьки газа. Эмульсиями называют дисперсные системы, в которых одна жидкость раздроблена в другой, нерастворяющей ее жидкости (Ж1—Ж2). Низкодисперсиые системы твердых частиц в жидкостях (Ж1—Т2) называют суспензиями, или взвесями, а предсльно-высокодисперсные— коллоидными растворами, или золями, часто лиозолямн, чтобы подчеркнуть, что дисперсионной средой является жидкость (от греч. «лиос»—жидкость). Если дисперсионной средой является вода, то такие золи называют гидрозолями, а если органическая жидкость — органозолями.
В твердой дисперсионной среде могут быть диспергированы гачы, жидкости или 1вердые тела. К системам Ti— Г; (твердые пены) относятся пепопласгы, пенобетон, пемза, шлак, металлы с включением газов. Как своеобразные твердые пены можно рассматривать и хлебобулочные изделия. В твердых пенах газ находится в виде отдельных замкнутых ячеек, разделенных дисперсионной средой. Примером системы Ti — Жэ является натуральный жемчуг, представляющий собой карбонат кальция, в котором коллоидно-диспергирована вода.
Большое практическое значение имеют дисперсные системы типа T1 — Т2. К ним относятся важнейшие строительные материалы (например, бетон), а также металлокерамические композиции и ситаллы.
К дисперсным системам типа T1 — Т2 относятся также некоторые сплавы, цветные стекла, эмали, ряд минералов, в частности некоторые драгоценные и полудрагоценные камни, многие изверженные горные породы, в которых при застывании магмы выделились кристаллы.
Цветные стекла образуются в результате диспергирования в силикатном стекле примесей металлов или их оксидов, придающих стеклу окраску. Например, рубиновое стекло содержит 0,01—0,1'% золота с размером частиц 4—30 мкм. Условия получения ярко-красных рубиновых н других окрашенных стекол изучались еще М. В. Ломоносовым. Эмали—это силикатные стекла с включениями пигментов (SnO2, TiО2, ZrО2), придающих эмалям непрозрачность и окраску. Драгоценные и полудрагоценные камни часто представляют собой оксиды металлов, диспергированные в глиноземе при кварце (например, рубин—это Сг2О3, диспергированный в Al203).
Дисперсные системы могут быть свободнодисперсными и связнодисперсными в зависимости от отсутствия или наличия взаимодействия между частицами Дисперсной фазы. К свободнодисперсным системам относятся аэрозоли, лнозоли, разбавленные суспензии и эмульсии. Они текучи. В этих системах частицы дисперсной фазы не имеют контактов, участвуют в беспорядочном тепловом движении, свободно перемещаются под действием силы тяжести. Спязноднсперсные системы—твердообразны; они возникают при контакте частиц дисперсной фазы, приводящем к образованию структуры в виде каркаса или сетки. Такая структура ограничивает текучесть дисперсной системы и придает ей способность сохранять форму. Подобные структурированные коллоидные системы называют гелями.
