
- •Связь сн в альдегидной группе разрывается в реакциях окисления. Ненасыщенные и ароматические углеводородные радикалы, подвергающиеся атаке электрофильными или нуклеофильными реагентами.
- •Классификация
- •Физические свойства
- •Характерные химические реакции
- •Физические свойства
- •Свойства пептидной связи
- •Описание
- •Классификация липидов
- •Простые липиды
- •Оксилипиды
- •38. Жиры и масла. Особенности структуры. Извлечение из масличного сырья. Жирные кислоты. Эссенциальные жирные кислоты. Жиры и масла, общая характеристика
- •Эссенциальные жирные кислоты свойства и применение
- •Поливалентные углеводородные радикалы
- •41. Химические свойства моносахаридов. Реакции по гидроксильной и карбонильной группе. Химические свойства
- •Классификация гликозидов
- •Классификация полисахаридов
Эссенциальные жирные кислоты свойства и применение
Жирные кислоты - компоненты жиров и масел. Жирные кислоты, необходимые организму и не синтезируемые им, называются эссенциальными жирными кислотами. Их организм получает с пищей.
Эти вещества улучшают состояние волос и ногтей, способствуют нормализации артериального давления, предотвращают развитие артритов, понижают уровень холестерина и триглицеридов, уменьшают вероятность повышения тромбообразования. Эссенциальные жирные кислоты полезны при кандидозе, сердечно-сосудистых заболеваниях, экземе и псориазе. Необходимы для нормальной работы и развития головного мозга.
Эссенциальные жирные кислоты входят в состав практически любой клетки организма. Они необходимы для восстановления старых клеток и образования новых. Помимо этого, они используются при синтезе простагландинов, гормоноподобных веществ, передающих различную химическую информацию в организме, регулируя таким образом многие жизненно важные процессы.
Выделяют две основные категории эссенциальных жирных кислот - омега-3 и омега-6. К омега-3эссенциальным жирным кислотам относятся линолевая и гамма-линоленовая кислоты, встречающиеся в сырых орехах, семечках и бобовых, а также в растительных маслах - масле виноградных косточек, примулы, кунжутном и соевом. Омега-6 - это альфа-линоленовая и эйкозопентатеновая (ЕРА) аминокислоты, которые присутствуют в свежей глубоководной рыбе, рыбном жире и некоторых растительных маслах - льняном, canola и масле из грецких орехов.
Для того, чтобы они служили источником эссенциальных жирных кислот, эти масла следует употреблять в жидком виде или в виде БАПД, не допуская их нагревания. Нагревание уничтожает эссенциальные жирные кислоты и приводит к образованию опасных свободных радикалов. При гидрогенизации масел образуются жиры, которые вредны для организма.
Наиболее важной из этих кислот является линолевая кислота. Суточная потребность в эссенциальных жирных кислотах составляет количество, покрывающее 10-20% от общей калорийности пищевого рациона.
Эссенцильными (незаменимыми) питательными веществами называют те соедине-Ия' к°торое человеческий организм не может синтезировать и должен получить Люди и некоторые животные не способны синтезировать жирные кислоты Двойными связями, расположенными дальше девятого от карбоксильной группы Ма Углерода. Линолевая кислота(С)8 2) с двойными связями в положениях 9 и 12 '"ноленовая кислота (С.,. ..) с двойными связями в положениях 9.12 и 15 относят'езаменимым лля человека соединениям. Эти жирные кислоты, также известные как омега-6 (линолевая) и омега-3 (линоленовая) жирные кислоты, являют важной составной частью рациона питания, выполняя следующие функции: • способствуют предотвращению экземы, псориаза, потери волос, ослабления н.ч мунной системы и неврологической дисфункции; • улучшают состояние кровеносной, репродуктивной систем и кожных покровов- • снижают уровень холестерин ЛИП; • способствуют росту н развитию плода. Биологической активностью обладает только цис-форма, изомеризация этих жирных кислот по положению двойной связи или образование транс-изомеров приводит к потере ими свойств, благоприятных для здоровья человека. 39. Превращения жиров при переработке и хранении. Реакции с участием сложно-эфирных групп и углеводородных радикалов. Реакции окисления. Хранение жиров.
Пищевые жиры вследствие особенностей химического состава легко подвергаются изменениям в процессе хранения и промышленной переработки, которые снижают их качество и биологическую ценность. Поэтому исключение возможности протекания в пищевых жирах процессов, сопровождающихся изменением их органолептических показателей и химического состава, является важной научно-практической проблемой.
Жиры, свободные от влаги и полученные из хорошего сырья, при низкой температуре и без доступа света могут сохраняться продолжительное время. В противном случае они подвергаются различным изменениям, образующиеся вещества ухудшают органолептические показатели жиров и в большей или меньшей степени оказывают вредное действие на организм человека. В основе порчи жиров лежат химические процессы и биохимические превращения. При пищевой порче жиров образуются низкомолекулярные летучие соединения — альдегиды, кетоны и низкомолекулярные кислоты, которые и обусловливают специфический запах прогорклых жиров. С течением времени в жирах образуются также некоторые нелетучие продукты окисления. Жиры, подвергшиеся порче, обычно содержат перекисные вещества, но количество их невелико. Перекисные соединения образуются в результате действия на жиры молекулярного кислорода и оказывают токсичное действие на мелких животных, а также болезнетворное влияние на детей младшего возраста.
Носителями прогорклости являются летучие альдегиды и кетоны, продукты окисления жиров. Они всегда содержатся в прогорклом жире одновременно, но в разных количествах. Альдегиды доминируют в жирах с ненасыщенными кислотами. В жирах с небольшим количеством ненасыщенных кислот (например кокосовое) преобладают кетоны — метилалкилкетоны. При прогоркании жиров кроме указанных соединений образуются вода, оксид и диоксид углерода. В испорченных жирах происходит резкое повышение содержания свободных жирных кислот вследствие гидролиза глицеридов, содержащихся в жирах. Накопление свободных жирных кислот может происходить и в результате воздействия на жиры молекулярного кислорода. Полученные свободные жирные кислоты имеют более низкую молекулярную массу, чем кислоты исходного жира.
Наряду с окислительными процессами при прогоркании жиров происходят также микробиологические и ферментативные процессы. Последние в основном сводятся к гидролизу, т. е. к расщеплению жира. Реакция эта развивается в жирах, содержащих белковые вещества и воду. Часто она бывает обусловлена наличием плесеней.
В растительных маслах на повышение кислотности влияет наличие фермента липазы, содержащегося в нежировом комплексе. При фильтрации осадок, а с ним и большая часть липазы удаляется из масла. В связи с этим профильтрованные масла более устойчивы при хранении.
Существуют и другие причины пищевой порчи жиров. Так, появление в коровьем масле рыбного привкуса и запаха обусловливается расщеплением лецитина и образованием холина. Разложение последнего ведет к образованию триметиламина, имеющего рыбный запах. Появляются иногда и другие неприятные запахи и вкусовые ощущения, связанные с гидролизом некоторых глицеридов под влиянием ферментов и разложения белков плесенями.
Углеводоро́дный радика́л (от лат. radix — «корень»; также — углеводородный остаток) в химии — группа атомов, соединённая с функциональной группой молекулы. Обычно при химических реакциях радикал переходит из одного соединения в другое без изменения. Но радикал и сам может содержать функциональные группы, поэтому с его «неизменностью» нужно быть осторожным: например, аминокислота аспарагиновая кислота содержит в той части молекулы, которая в общем виде рассматривается как остаток аминокислоты, ещё одну карбоксильную группу. Часто углеводородный радикал называют просто радикал, что может вызвать путаницу с таким понятием как свободный радикал. Некоторые углеводородные радикалы могут также являться функциональными группами, например, фенил (−C6H5), винил (−C2H3) и пр. Углеводородными радикалами обычно являются остатки углеводородов, которые входят в состав многих органических соединений. Моновалентные углеводородные радикалы
Название углеводородного радикала образуются от корня названия углеводорода путём прибавления к нему суффикса -ил. Суффиксы «-ен» и «-ин» сохраняются, дабы не потерять представление о насыщенности углеводородного радикала. В более сложных углеводородных радикалах, например, полициклических, суффикс «-ан» сохраняется[1], вероятно, ввиду большей благозвучности. Перед суффиксом «-ил» указывается порядковый номер того атома углерода от начала цепи углеродных атомов радикала, у которого есть свободная валентность — кроме случая, если свободной валентностью обладает первый атом в цепи. Нумерация цепи идёт от конца, ближайшего к свободной валентности. В случае, если в углеродной цепи с одной стороны атома со свободной(-ыми) валентностью(-ями) все атомы водорода замещены, то атом со свободными валентностями считается первым в цепи. Ранее использовался и в тривиальных названиях используется характер атома со свободной валентностью — первичный, вторичный (сек- или втор-), третичный (терц- или трет-) (см. далее). В тривиальных наименованиях используются также корни исторически сложившихся названий веществ или связанных с ними понятий. Например:
−CH3 — метил (метан + -ил)
−C2H5 — этил (этан + -ил)
-CH2-CH=CH-CH3 — бут-2-енил

Вверху изображён спиро[4.5]декан-8-ил.
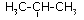 —
проп-2-ил
или
изопропил
—
проп-2-ил
или
изопропил-CH2-CH(CH3)2 — 2-метилбутил или изобутил
-CH(CH3)-CH2-CH3 — бут-2-ил или сек-бутил, или втор-бутил
−C6H5 — фенил (фен[2] + -ил)
-CH=CH2 — винил[3]
