
- •Михайлов с.С. Спортивная биохимия: Учебник для вузов и колледжей физической культуры.
- •Изучение химического состава живого организма, строения и свойств молекул, из которых он состоит.
- •Изучение обмена веществ, т. Е. Химических превращений, кото рым подвергаются входящие в организм молекулы (раздел биохимии, решающий эти задачи, называется «Общая биохимия»).
- •Общая биохимия общая характеристика химического состава организма
- •Классификация белков.
- •Нуклеиновые кислоты
- •Углеводы
- •Общая характеристика обмена веществ
- •Основное назначение метаболизма
- •Строение и биологическая роль атф
- •Ферментативный катализ
- •Строение ферментов
- •Механизм действия ферментов
- •Специфичность ферментов
- •Изоферменты
- •Кинетика ферментативного катализа
- •Зависимость скорости ферментативной реакции от концентрации фермента
- •Зависимость скорости ферментативной реакции от концентрации субстрата
- •Зависимость скорости ферментативной реакции от температуры
- •Зависимость скорости ферментативной реакции от рН
- •Ингибиторы ферментов
- •Активаторы ферментов
- •Регуляция скорости ферментативных реакций
- •Биологическое окисление
- •Тканевое дыхание
- •Анаэробное окисление
- •Окисление
- •Свободнорадикальное окисление
- •Обмен углеводов. Переваривание и всасывание углеводов
- •Синтез гликогена
- •Распад гликогена
- •Метаболизм глюкозы
- •Гексозодифосфатный путь (гдф-путь)
- •Аэробный распад углеводов
- •Сукцинат
- •Обмен липидов.
- •Катаболизм жиров
- •Синтез жиров
- •Обмен нуклеиновых кислот
- •Катаболизм нуклеиновых кислот
- •Олигонуклеотиды
- •Синтез нуклеотидов
- •Аденилоянтарная кислота
- •Ксантиловая кислота
- •Синтез нуклеиновых кислот
- •Цикл образования мочевины
- •Жирные к-ты Глюкоза
- •Водно-минеральный обмен обмен воды
- •Выведение воды из организма
- •Обмен минеральных веществ
- •Распределение минеральных веществ в организме
- •Поступление минеральных веществ в организм
- •Биологическия роль отдельных минеральных элементов
- •Витамины
- •Ацетил-Ко а
- •Цикл кребса
Зависимость скорости ферментативной реакции от рН
Скорость ферментативных реакций значительно зависит от кислотности среды, в которой они протекают.
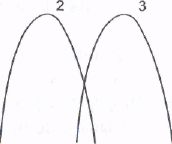
Для каждого фермента имеется определенное значение рН, при котором наблюдается наибольшая скорость реакции - рН-оптимум. При отклонении в любую сторону от этого значения рН резко уменьшается ферментативная активность. Важно подчеркнуть, что величина рН-оптимума у разных ферментов колеблется в большом диапазоне значений рН, в то время как температурный оптимум для большинства ферментов составляет 37-40 °С. В качестве примера можно привести значения рН-оптимума следующих ферментов (рис.):
пепсин желудочного сока - 1,0-2,0
амилаза слюны - 6,8-7,0
щелочная фосфатаза плазмы крови - 9,0-10,0
Влияние кислотности среды на скорость ферментативных реакций обусловлено тем, что при изменении кислотности меняется конформа-ция всей белковой молекулы фермента, в том числе изменяется кон-формация активного центра и его способность осуществлять катализ.
V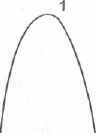


10
рН 1,5 7,0
Рис. Зависимость скорости ферментативной реакции от рН
(1 - пепсин, 2 - амилаза, 3 - щелочная фосфатаза)
При рН-оптимуме фермент находится в оптимальной для проявления каталитических свойств конформации. При небольшом отклонении величины кислотности от рН-оптимума наблюдается незначительное изменение конформации, носящее обратимый характер. При значительном отклонении от рН-оптимума (в сильнокислой и сильнощелочной среде) происходит необратимая денатурация ферментного белка, приводящая к полной утрате каталитической активности.
При работе с ферментами в лабораторных условиях в реакционную среду вводят буферные растворы, рН которых соответствует рН-оптимуму изучаемых ферментов.
Ингибиторы ферментов
Скорость ферментативной реакции существенно зависит от присутствия ингибиторов и активаторов.
Ингибиторы (I) - это химические соединения (обычно низкомолекулярные), которые, находясь в низких концентрациях, избирательно тормозят определенные ферментативные реакции. При этом ингибитор всегда присоединяется к ферменту с образованием фермент-ингибиторного комплекса. Фермент, связанный с ингибитором, теряет свою каталитическую активность.
Если связи между ферментом и ингибитором прочные, то действие ингибитора носит необратимый характер, и торможение нарастает во времени вплоть до полного прекращения ферментативной реакции:
Е + I Е 1
Такие ингибиторы называются необратимыми. Примером необратимых ингибиторов являются фосфорорганические соединения (табун, зарин, дихлофос, карбофос и др.), избирательно и необратимо угнетающие важнейший фермент организма холинэстеразу, участвующую в передаче нервных импульсов.
Если ингибитор присоединяется к ферменту за счет непрочных связей, то торможение фермента является обратимым и не зависит от времени:
Ингибиторы такого типа называются обратимыми.
В свою очередь, обратимые ингибиторы делятся на две разновидности: конкурентные и неконкурентные.
Конкурентные ингибиторы присоединяются к активному центру фермента, т. е. к тому же участку поверхности фермента, что и субстрат. Поэтому между ингибитором и субстратом идет конкуренция за присоединение к активному центру. Занимая активный центр, ингибитор тем самым препятствует образованию фермент-субстратного комплекса - первой стадии ферментативного катализа. Конкурентные ингибиторы обычно по строению похожи на субстрат.
Неконкурентные ингибиторы присоединяются к ферменту вне активного центра. Этот участок поверхности фермента называется алло-стерический центр (т. е. находящийся в другом месте по сравнению с активным центром).
Присоединение неконкурентного ингибитора к аллостерическому центру вызывает неблагоприятное изменение пространственной структуры (конформации) всей молекулы фермента, в том числе и активного центра. В результате каталитические свойства фермента снижаются.
Неконкурентные ингибиторы участвуют в регуляции скорости ферментативных реакций, протекающих в организме. В роли неконкурентных ингибиторов могут быть гормоны, конечные и промежуточные продукты ферментативных реакций, ионы металлов, лекарственные вещества.
