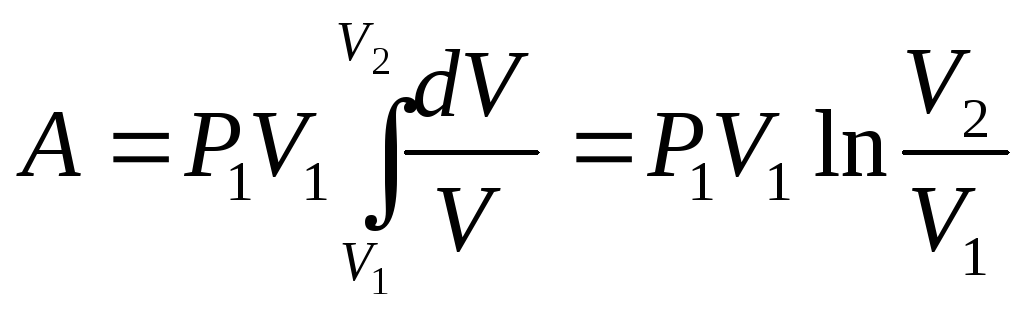лекции, учебные пособия / молекулярная физика, основные формулы, 1-й сем. / МОЛЕКУ~1
.DOC|
PV=const-ур-е Бойля-Мариотта 2. Изобарич.(P=const)
3. Изохорн.(V-const)
P=nkT - Осн.ур-е для давления МКТ P=P1+P2+…-з-н Дальтона
Гипотеза о равнораспределении энергии по степеням свободы
Молярная теплоёмкость.
Показатель адиабаты
Адиабатический процесс
Работа идеального газа
A=P(V2-V1)
Распределение Максвелла
|
Барометрические формулы:
Функции состояния:
S=klnW (W-число микросостояний)
|