
- •Растворы. Способы описания количественного состава растворов. Приготовление растворов.
- •Титрованные растворы. Стандартизация титрованных растворов.
- •Индикаторы. Общая характеристика. Классификация.
- •Индикаторы для кислотно-основного титрования. Теория поведения индикаторов. Ошибки титрования. Кривые титрования.
- •Индикаторы метода осадительного титрования. Кривые осадительного титрования.
- •Индикаторы метода комплексометрического титрования. Кривые титрования.
- •Окислительно-восстановительные индикаторы. Кривые титрования.
- •Растворимость. Условные термины обозначающие растворимость.
- •Кислотно-основные свойства лв.
- •Связь химического строения и спектральных характеристик лв.
- •Хроматографические методы идентификации лв.
- •Определение температуры плавления лв.
- •Определение температуры затвердевания лв.
- •Определение температуры каплепаденияЛв.
- •Определение температуры пределов перегонки лв.
- •Определение температуры кипения лв.
- •Роль Государственной фармакопеи в обеспечении качества лс.
- •Требования общей статьи гф рб к субстанциям для фармацевтического использования.
- •Испытания на содержание примесей
- •Причины попадания летучих в-в и воды в лс.
- •Физические методы определения воды: высушивания и дистилляции.Метод отггонки
- •Химический метод определения воды: акваметрия (метод к.Фишера).
- •Определение обще золы и сульфатной золы.
- •Определение прозрачности и степени мутности растворов лв.
- •Определение бесцветности и окраски растворов лв.
- •Методы определения плотности жидкостей с помощью пикнометра и ареометра.
- •Методы определения плотности твердых жиров и восков.
- •Абсолютный и относительный показатель преломления. Применение показателя преломления в фармакопейном анализе.
- •Удельное оптическое вращение, угол оптического вращения. Применение удельного оптического вращения в фармакопейном анализе.
- •Виды вязкости (динамическая, кинематическая, структурная, удельная, приведенная, характеристическая)
- •Реакции идентификации на мышьяк и ртуть.
- •Испытания на содержание примеси мышьяка в лв.
- •Определение остаточных растворителей в субстанциях.1ч
Растворы. Способы описания количественного состава растворов. Приготовление растворов.
Раствор, концентрация активного вещества в котором известна с высокой точностью, называется стандартным раствором.

Количественный состав раствора можно описывать с помощью безразмерных величин и величин, имеющих размерность. Безразмерные величины иначе называются долями.

Из всех видов долей чаще всего, по крайней мере, в аналитической химии, используется массовая доля.
Доли могут выражаться в процентах. Процент – это не единица измерения, а всего лишь синоним величины «одна сотая».
К размерным величинам, используемым для описания количественного состава растворов, относят концентрации вещества в растворе и моляльность растворённого вещества.
Концентрация – это отношение массы или количества растворённого вещества
к объёму раствора.
Моляльность растворённого вещества представляет собой отношение количества этого вещества, находящегося в растворе, к массе растворителя. Размерность моляльности – моль/кг. Её используют в тех случаях, когда раствор находится в неизотермических условиях.
Для количественной характеристики стандартных растворов обычно используют молярную концентрацию (вещества или эквивалента вещества). Иногда для этой цели пользуются титром раствора.
Если стандартный раствор титранта используется для серийных анализов, то для его количественной характеристики удобно использовать титр соответствия (титр по определяемому веществу), который показывает массу определяемого вещества, взаимодействующего с 1 мл данного титранта.

Титрованные растворы. Стандартизация титрованных растворов.
Титрованные растворы должны готовиться в соответствии с обычными требованиями химического анализа. Проверяют точность используемого оборудования для того, чтобы удостовериться в его пригодности для предполагаемого применения. Титрованными называют растворы точно известной концентрации, предназначенные для целей титриметрического анализа. Концентрацию титрованных растворов выражают их молярностью, титром или титром по определяемому веществу. Молярность выражает количество вещества, растворенного в 1 л раствора, в виде количества молей. Титр по определяемому веществу (титр соответствия) – это выраженная в граммах масса определяемого вещества, эквивалентная 1-му мл данного титранта.
Концентрация титрованных растворов не должна отличаться от указанной более чем на 10%. Молярность титрованных растворов определяют с точностью 0,2%.
Титрованные растворы стандартизуют описанными ниже методами. Если титрованный раствор используют в количественном анализе, в котором конечную точку определяют электрохимическим методом (например, амперометрии или потенциометрии), раствор стандартизуют тем же методом. Состав среды, в которой стандартизуют титрованный раствор, должен быть таким же, как и тот, в котором он будет использован.
Растворы более разведенные, чем описанные ниже, получают разведением последних водой, свободной от углерода диоксида, Р. Поправочные коэффициенты полученных растворов такие же, как у исходных растворов. Растворы с молярностью ниже 0,1 М готовят непосредственно перед использованием. Т.р-ры хранят при комнатной t, защищая от воздействия диоксида углерода, влаги, прямых солнечных лучей.
Стандартным веществом в титриметрии называется реагент, используемый для стандартизации раствора титранта.
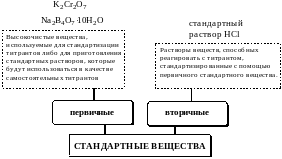
В качестве первичных стандартных веществ используют соединения, обладающие следующими свойствами:
состав строго соответствует химической формуле;
выпускаются промышленностью в чистом виде (квалификация не ниже «ч.д.а.») либо легко подвергаются очистке;
устойчивы при обычных условиях;
нелетучи и, по возможности, не содержат кристаллизационной воды (можно использовать и кристаллогидраты, если они устойчивы).
имеют большую молярную массу (меньше погрешность при измерении массы).
Растворы титрантов можно готовить также из фиксаналов и методом ионного обмена. Фиксаналом (нормадозой, стандарт-титром) называются приготовленные и расфасованные в промышленных условиях порции вещества, содержащие точно известное его количество. Содержимое фиксанала растворяют в указанном объёме растворителя (обычно объём раствора составляет 1 л) и получают раствор с точной концентрацией растворённого вещества.
