
- •1.1.Общий анализ диаграммы состояния железо-цементит и ее практическое значение
- •1.3.Строение и свойства сплавов железо-углерод. Твердые растворы, механические смеси, химические соединения.
- •2.1 Сварка. Классификация способов сварки.
- •3.1 Ручная дуговая сварка. Схема, сущность, параметры режима сварки, область применения, преимущества и недостатки.
- •3.6 Дефекты сварных швов. Внутренние дефекты и их характеристики.
- •3.2 Автоматическая дуговая сварка под слоем флюса. Схема, сущность, параметры режима сварки, область применения, преимущества и недостатки.
- •1.2.Кристалическое строение металлов и сплавов. Типы кристаллических решеток. Их характеристика.
- •1.4.Стали. Маркировка углеродистых сталей обыкновенного качества и качественных. Примеры.
- •2.2.Сварка. Типы сварных соединений. Классификация сварных соединений по пространственному соединению.
- •1.6. Превращения стали при охлаждении. Диффузионное и бездиффузионное превращения.
- •2.6. Свариваемость стали. Группы свариваемости стали.
- •2.11. Сварочные напряжения и деформации. Способы правки деформированных конструкций.
- •3.7. Дефекты сварных швов. Внешние дефекты, их характеристика.
- •2.3 Свариваемость сталей. Основные факторы, влияющие на свариваемость сталей.
- •2.8 Свариваемость сталей. Способы повышения свариваемости сталей.
- •3.4 Контактная сварка. Точечная сварка. Схема, сущность, параметры режима сварки, область применения, преимущества и недостатки.
- •1.8 Термическая обработка стали. Полный отжиг. Режимы. Область применения.
- •1.5. Стали. Маркировка легированных сталей. Обозначение легирующих элементов. Примеры.
- •1.10. Термическая обработка стали. Полная закалка. Режимы.Область применения.
- •2.5. Свариваемость сталей. Влияние легирующих элементов на свариваемость стали.
- •2.10. Сварочные напряжения и деформации. Способы их уменьшения.
- •3.9.Ультразвуковой метод контроля качества сварных соединений. Схема, сущность, применение.
- •1.9. Термическая обработка стали. Неполный отжиг. Режимы. Область применения.
- •2.4. Свариваемость сталей. Влияние содержания углерода на свариваемость сталей.
- •2.9. Сварочные напряжения и деформации. Причины их возникновения.
- •3.5. Контактная сварка. Шовная сварка. Схема, сущность, параметры режима сварки, область применения, преимущества, недостатки.
1.1.Общий анализ диаграммы состояния железо-цементит и ее практическое значение
Диаграмма
состояния-графическое изображение
фазового состояния всех сплавов данной
системы в зависимости от температуры
и концентрации компонентов. Среди
диаграмм состояния металлических
сплавов самое большое значение имеет
диаграмма железо-углерод (цементит).
Диаграмма состояния железо-углерод
необходима: для установления правильных
условий литья деталей, для назначения
оптимальных режимов горячей деформации
металлов , для назначения различных
режимов термической и химико-термической
обработки деталей из стали и чугуна,
при разработке технологий сварки.
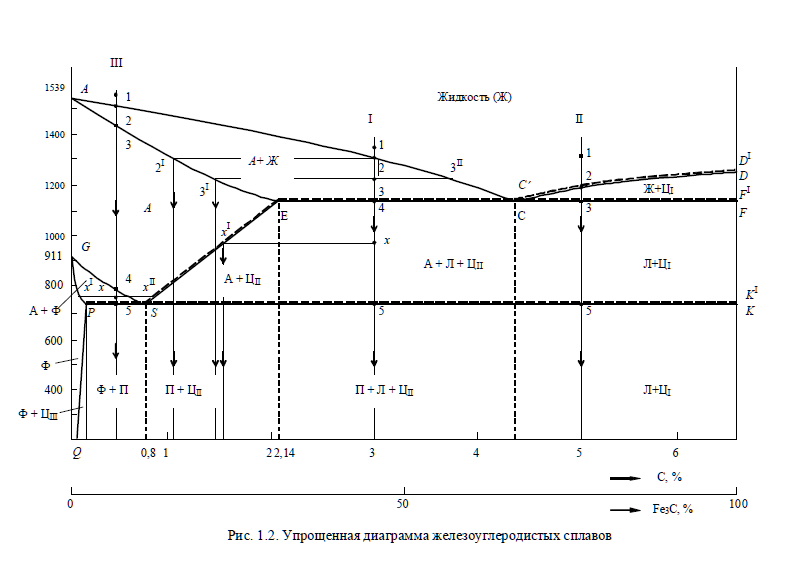
Анализ
диаграммы:
По остановкам или перегибам на кривых
охлаждения можно установить температуры
начала и конца фазовых превращений т.
е. определить критические точки.
Критические точки на кривой охлаждения
железа 1539, 1392, 911, 768 ˚С. Существует два
типа диаграмм: метастабильные-сплошные
линии(железо-карбид) и стабильные-штриховые
линии(железо-графит). ACD-
линия начала первичной кристаллизации
(линия ликвидуса). AECF-линия
конца первичной кристаллизации( линия
солидуса). ECF-линия
эвтектического превращения, по этой
линии происходит реакция
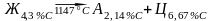 .
GS-
линия начала перехода аустенита в
феррит. SE-линия
предельной растворимости углерода в
ɣ-железе. PSK-линия
эвтектоидного или перлитного превращения,
реакция:
.
GS-
линия начала перехода аустенита в
феррит. SE-линия
предельной растворимости углерода в
ɣ-железе. PSK-линия
эвтектоидного или перлитного превращения,
реакция:
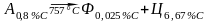 .
.
GP- линия окончания аллотропических превращений в сплавах, по этой линии превращение аустенита в феррит заканчивается. PQ-линия предельной растворимости углерода в α-железе. GS-совокупность верхних критических точек для доэвтектоидной стали.SE- совокупность верхних критических точек для заэвтектоидной стали. PSK- совокупность нижних критических точек для всех сплавов. S- эвтектоидная точка. C-эвтектическая точка.
1.3.Строение и свойства сплавов железо-углерод. Твердые растворы, механические смеси, химические соединения.
А) Жидкий раствор углерода в железе(Ж) . В жидком состоянии железо и углерод неограниченно растворимы друг в друг, в растворе углерод статически равномерно распределен между атомами железа. Атом углерода окружен 6ю атомами железа, образующими октаэдр.
Б) Феррит (Ф) . Твердый раствор внедрения углерода в α-железе. Растворимость углерода в α-железе при нормальной температуре составляет 0,006%. Максимальная растворимость достигается при t=727 ˚С и составляет 0,025%. Твердость 80…100HB
В) Аустенит (А). Твердый раствор внедрения углерода в ɣ-железе. Максимальная растворимость углерода в таком железе при t=1147 ˚С составляет 2,14%. При понижении температуры растворимость уменьшается и при t=727 ˚С составляет 0,8%. Максимальная растворимость углерода в ɣ-железе принята за границу между сталью и чугуном. Сплавы с содержанием углерода менее 2,14% называются сталями, а с большим-чугунами. Пластичность δ=40..50%. Твердость 180..200HB
Г)
Цементит (Ц). Химическое
соединение железа с углеродом (карбид
железа
 ),
содержит 6,67%С. Имеет сложную ромбическую
решетку с плотной упаковкой атомов.
Твердость более 800HB.
Температура плавления точно не
установлена и принимается 1250 ˚С
),
содержит 6,67%С. Имеет сложную ромбическую
решетку с плотной упаковкой атомов.
Твердость более 800HB.
Температура плавления точно не
установлена и принимается 1250 ˚С
При сплавлении железа с углеродом возникают следующие структурные составляющие:
Перлит (П). Механическая смесь пластинок феррита и цементита, содержащая 0,8% С. Образуется при температуре 727 ˚С в результате распада аустенита при его охлаждении. Может быть пластинчатым и зернистым. Твердость 160..200HB.
Ледебурит (Л). Механическая смесь пластинок аустенита и цементита. Образуется в результате кристаллизации жидкого расплава, содержащего 4,3%С при температуре 1147 ˚С. Твердость 600..700HB. Он очень хрупок.
В процессе охлаждения при содержании углерода в сплавах выше предела растворимости он может выделяться в виде графита. Чаще всего он присутствует в высокоуглеродистых сплавах- чугунах.
В твердых растворах и в цементите атомы железа и углерода положительны ионизированны, т. е. углерод ведет себя подобно металлу.
