
МИНОБРНАУКИ РОССИИ
Нижнекамский химико-технологический институт (филиал)
федерального государственного бюджетного образовательного учреждения
Высшего профессионального образования
«Казанский национальный исследовательский технологический университет»
Кафедра химической технологии органических веществ
КОНТРОЛЬНЫЕ ЗАДАНИЯ
ПО ДИСЦИПЛИНЕ
«ОБЩАЯ ХИМИЧЕСКАЯ ТЕХНОЛОГИЯ»
ДЛЯ СТУДЕНТОВ,
ОБУЧАЮЩИХСЯ ЗАОЧНО
ПО СПЕЦИАЛЬНОСТИ
«ХИМИЧЕСКАЯ ТЕХНОЛОГИЯ ОРГАНИЧЕСКИХ ВЕЩЕСТВ»
Разработал ст. преподаватель кафедры ХТОВ Ионова Н. И.
Нижнекамск 2012
Вариант контрольного задания выбирается в соответствии с последней цифрой зачетной книжки студента. Перед тем как приступить к выполнению контрольного задания, студент должен, пользуясь методическими указаниями, проработать рекомендуемую литературу. Контрольная работа выполняется отдельно и представляется на кафедру для рецензирования в намеченные по графику сроки.
Контрольная работа оформляется в тетради. Ответы на вопросы, уравнения реакций записываются полностью. Произвольные сокращения не допускаются, таблицы и рисунки оформляются в соответствии с требованиями, предъявляемыми к оформлению. По всем вариантам должны быть приведены уравнения химических реакций и подробное решение задач. В конце контрольной работы приводится список использованной литературы.
Контрольная работа состоит из четырех заданий. Первые 3 задания являются практическими и отвечают следующим темам: Равновесие химических реакций, Стехиометрия химических превращений и Химические реакторы. Четвертое задание требует ответа на теоретический вопрос.
Стехиометрия химических превращений.
Стехиометрические уравнения показывают, в каких соотношениях вещества вступают в химическое взаимодействие.
Общий вид стехиометрического уравнения:
![]()
Уравнение устанавливает соотношение между количеством превратившихся веществ:
![]()
Степень превращения вещества – отношение количества превращенного вещества к его первоначальному количеству (1):
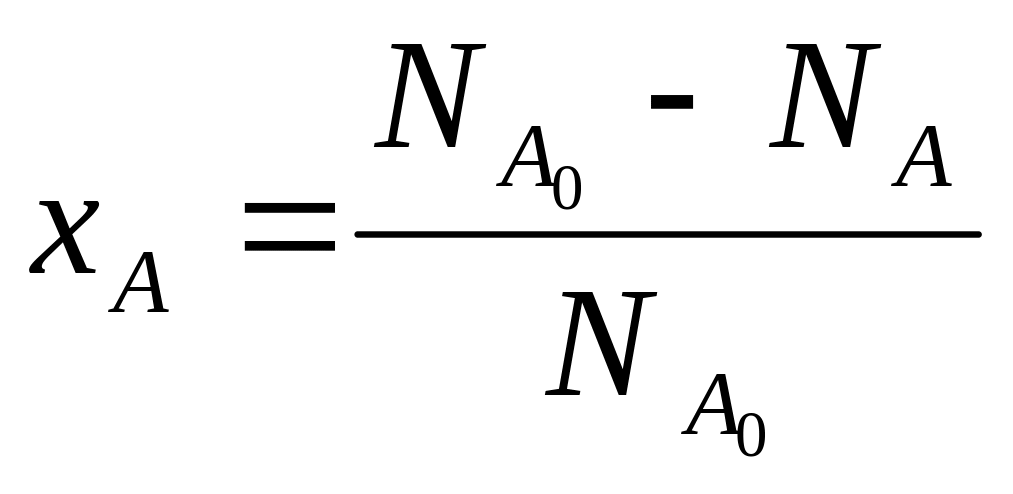
Степень
превращения может быть определена для
любого исходного реагента, например,
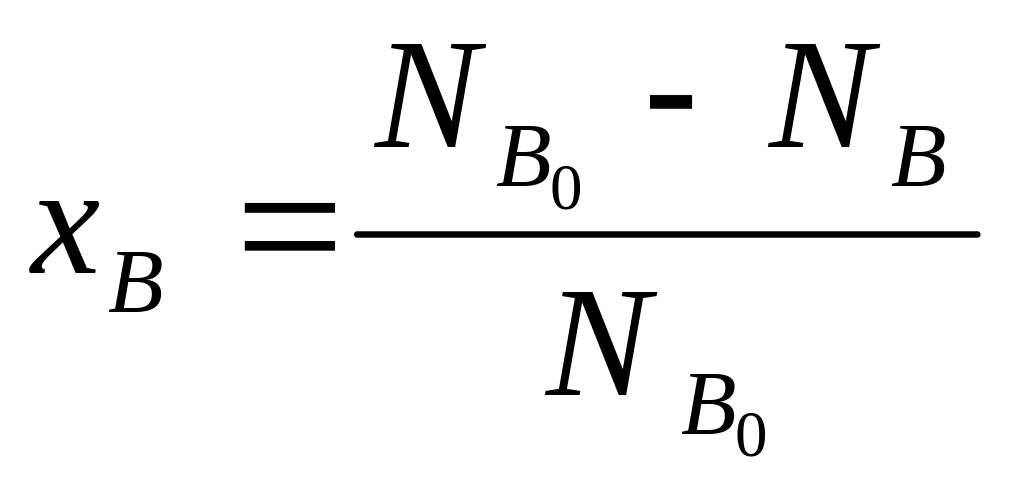
Из соотношения (1) и определений ХА и ХВ, получим связь между степенями превращения двух исходных веществ:
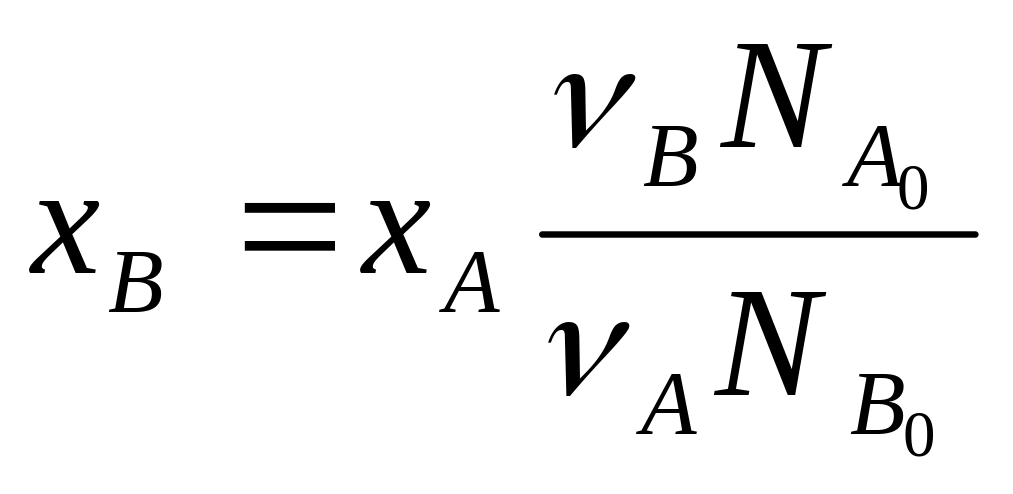
Можно определить количество любого вещества Ni в реагирующей смеси:
![]()
Если реакция протекает без изменения объема реакционной смеси или не происходит изменения общего количества реагирующих веществ, то степень превращения можно выразить через концентрации:
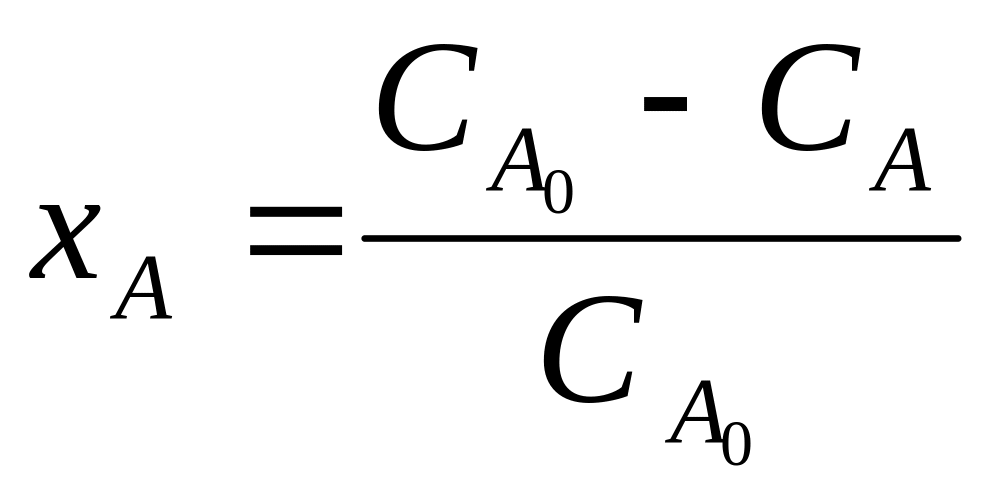
Для сложной реакции кроме степени превращения вводят дополнительные характеристики процесса: селективность процесса и выход продукта.
Селективность – это отношение количества исходного реагента, расходуемого на целевую реакцию, к общему количеству исходного реагента, пошедшего на все реакции.
Для двух параллельных реакций:
![]()
селективность по продукту R
![]()
Для двух последовательных реакций:
![]()
селективность по продукту R
![]()
Выход продукта для продукта R
![]()
Уравнение, связывающее степень превращения исходного вещества, выход продукта и его интегральную селективность, имеет вид
![]()
Смещение химического равновесия.
Сместить химическое равновесие – это значит изменением внешних условий добиться преимущественного протекания прямой или обратной реакций. Общие закономерности этого явления были сформулированы Ле- Шателье в 1887 г.:
Если на систему, находящуюся в равновесии, оказывается воздействие извне, то равновесие смещается в сторону той реакции, протекание которой максимально ослабляет внешнее воздействие.
Чаще всего приходится сталкиваться со смещением равновесия в результате следующих изменений условий:
1)температура
Изменение температуры, в отличие от других внешних воздействий, влияет на значение константы равновесия. Повышение температуры вызывает ускорение той реакции, протекание которой сопровождается поглощением тепла (эндотермическая реакция). Напротив, понижение температуры благоприятствует протеканию экзотермической реакции – реакции, сопровождающейся выделением тепла.
2)давление
Повышение давления ускоряет ту реакцию, в которой происходит уменьшение количеств газообразных веществ, а понижение давления – реакцию, сопровождающуюся увеличением количеств газообразных веществ. Если количество газов в ходе реакции не изменяется, то изменение давления не оказывает влияния на положение химического равновесия.
3)концентрации
Добавление в реакционную систему какого-либо компонента смещает равновесие в сторону той реакции, где тот компонент расходуется. Отвод какого-либо вещества из реакционной системы, напротив, ускоряет реакцию, в которой это вещество образуется.
4)Введение инертного газа в систему при постоянном давлении подобно эффекту уменьшения общего давления. Если реакция протекает с уменьшением числа молей, разбавление инертным газом смещает равновесие реакции в сторону исходных реагентов; при увеличении числа молей равновесие смещается вправо.
