- •Глава 2. Фотосинтез
- •2.1. Сущность и значение фотосинтеза
- •2.2. Структурная организация фотосинтетического аппарата
- •2.3. Пигментная система фотосинтетического аппарата
- •Формы хлорофилла в растениях
- •Распространение основных фотосинтетических пигментов в растениях
- •Некоторые особенности пигментов
- •2.4. Биосинтез пигментов
- •2.5. Роль пигментов в поглощении света
- •2.6. Миграция энергии возбуждения фотосинтетическими пигментами
- •2.7. Световая стадия фотосинтеза
- •Сравнение циклического и нециклического фотофосфорилирования
- •2.8. Темновая фаза
- •2.9. Продукты темновой стадии фотосинтеза
- •2.10. Фотодыхание
- •2.11. Влияние внешних и внутренних факторов на интенсивность фотосинтеза
- •Интенсивность фотосинтеза у растений разных систематических групп
- •2.12. Саморегуляция фотосинтеза
- •2. 13. Фотосинтез и урожай
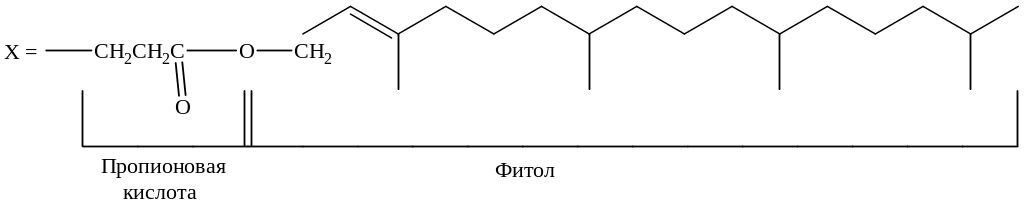
Формы хлорофилла в растениях
Тип хлорофилла |
R1 |
R2 |
R3 |
R4 |
Отсутствие атомов Н между С7 и С8 (двойные связи) |
а |
–СН=СН2– |
–СН3 |
–СН2СН3 |
Х |
Нет |
в |
–СН=СН2– |
–СНО |
–СН2СН3 |
Х |
Нет |
с1 |
–СН=СН2– |
–СН3 |
–СН2СН3 |
–СН=СН·СООН |
Да |
с2 |
–СН=СН2– |
–СН3 |
–СН=СН2 |
–СН=СН·СООН |
Да |
d |
СНО |
–СН3 |
–СН2СН3 |
Х |
Нет |
|
Каротиноиды – жирорастворимые пигменты желтого, оранжевого и красного цветов. Они входят в состав хлоропластов и хромопластов незеленых частей растений (цветов, плодов, корнеплодов). В зеленых листьях их окраска маскируется хлорофиллом.
Каротиноиды являются тетратерпеноидами (8 остатков изопрена) и содержат 40 атомов углерода. Они представляют собой цепи, которые имеют, как и хлорофилл, двойные сопряженные связи. На одном или двух концах цепи находятся иононовые кольца.
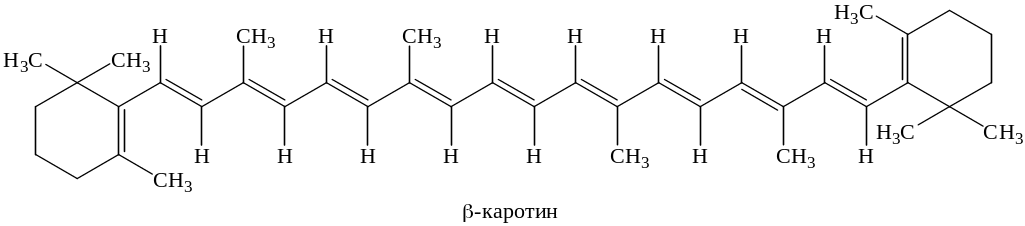
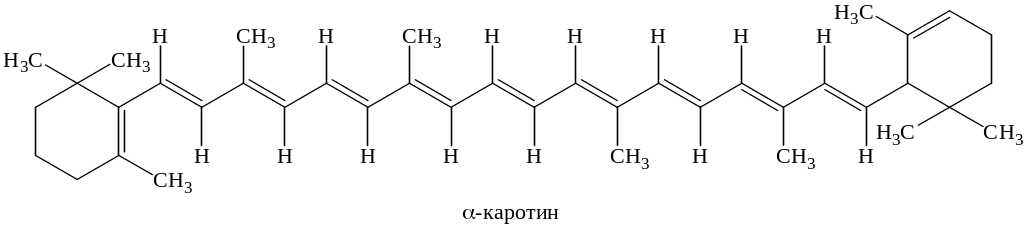
Каротиноиды делят на две группы: каротины и ксантофиллы. Каротины, например α-каротин (С40Н56) представляет собой чистые углеводороды (тетратерпены):
|
|
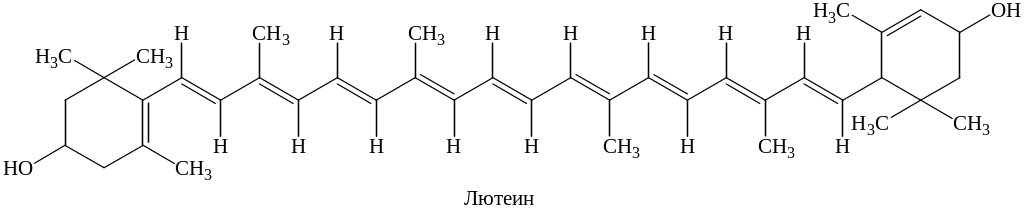
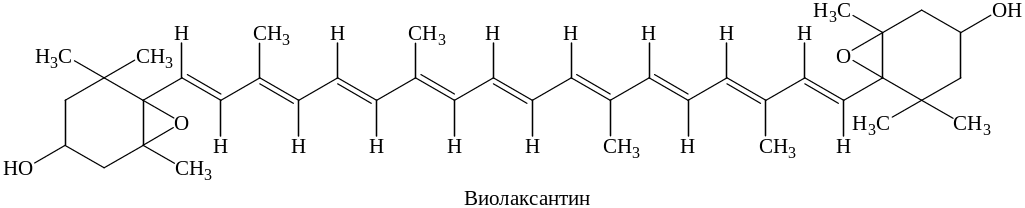
тогда как ксантофиллы: лютеин С40Н56О2 и виолоксантин С40Н56О4 являются окисленными соединениями. Каротины имеют оранжевую или красную окраску, а ксантофиллы – желтую.
|
|
α-Каротин имеет одно β-иононовое кольцо (двойные связи между С5 и С6), а второе – ε-иононовое (двойные связи между С4 и С5). β-Каротин отличается от α- тем, что имеет два β-иононовых кольца.
Ксантофиллы отличаются значительно большим разнообразием, чем каротины, поскольку входящие в их состав кислородосодержащие группы могут быть самыми разнообразными: это может быть гидроксильная группа, кетогруппа, эпоксигруппа и метаксильная группа.
Распределение и типы каротиноидов в растениях имеют глубокий эволюционный смысл; их можно использовать для таксономических целей.
Относительная распространенность хлорофилла и каротиноидов в высших растениях составляет 4,5:1 (квантосомы содержат 230 молекул хлорофилла и 50 молекул каротиноидов). Интересно отметить, что животные обычно не синтезируют каротиноидов. Поэтому желтая и розовая расцветка птиц (например, канареек, фламинго), так же как и многочисленных беспозвоночных, обусловлена каротиноидами, которые они получают, поедая растения.
Молекулы каротиноидов имеют длину около 3 нм; те, которые принимают участие в фотосинтезе обычно имеют 9 или более двойных связей.
Свет, поглощенный хлорофиллом, может вызывать образование возбужденных состояний молекулярного кислорода. Этот высокореакционное состояние может повредить хлорофиллу, но взаимодействие с каротиноидами предотвращает этот процесс. Например, мутант Rhodopseudomonas spheroides, у которого отсутствуют каротиноиды, обычно осуществляет фотосинтез в отсутствии кислорода; когда бактерии освещают в присутствии кислорода, бактериохлорофилл фотоокисляется и бактерии гибнут. У родственных штамов, содержащих каротиноиды, такая чувственность к кислороду не наблюдается. В других случаях, когда синтез каротиноидов подавлен, свет в присутствии кислорода может оказаться для фотосинтезирующих организмов губительным.
У дефектных по каротиноидам мутантов кукурузы и подсолнечника, а также при экспериментально нарушенном образовании каротиноидов наблюдается быстрое фотоокисление хлоропластов. Защитный (фотопротекторный) эффект объясняется способностью каротиноидов взаимодействовать с возбужденными молекулами кислорода и хлорофилла. В этом случае энергия возбужденного триплетного хлорофилла и синглетного кислорода резонансным путем передается на каротиноиды, а затем рассеивается в виде тепла.
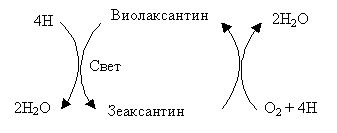
Высказывается мнение о прямом участии каротиноидов в расщеплении воды и кислородном обмене при фотосинтезе. Особое значение придается виолаксантиновому циклу:
|
При освещении в зеленых листьях происходит превращение виолаксантина в зеаксантин. В независимой от света реакции благодаря включению кислорода происходит обратное превращение.
В верхушках побегов растений каротиноиды обеспечивают их ориентацию к световому потоку за счет фототропизма.
Каротиноиды выполняют роль вспомогательных пигментов, которые передают энергию поглощенных квантов хлорофиллу «а» для совершения фотохимической работы. Особенно возрастает их значение как светоулавливающих систем в сине-фиолетовой и синей частях спектра в затененных местах, т. е. когда преобладает рассеянная радиация.
К пигментам, которые участвуют в световой стадии фотосинтеза, относятся и фикобилины. Все фотосинтетические пигменты (хлорофиллы, каротиноиды и фикобилины) входят в состав пигментных систем в виде хромпротеинов, т. е. пигмент – белковых комплексов. Хлорофиллы и каротиноиды связаны с белками относительно слабо, связь между пигментом и белком не ковалентная. Поскольку такие связи легко нарушаются хлорофиллы и каротиноиды можно экстрагировать с помощью органических растворителей таких как ацетон, спирт.
Фикобилины связаны с белком ковалентно, поэтому они находятся в виде молекул – фикобилипротеинов. Фикобилипротеины растворимы в воде и легко вымываются из мацерированных тканей водой или разбавленными растворами солей. Однако, для разрушения молекулы фикобилипротеинов путем расщепления связи между пигментом и белком необходим гидролиз в жестких условиях.
По структуре фикобилины – тоже тетрапироллы, но с открытой цепью, которые имеют систему коньюгированных двойных и одинарных связей. У фикобилинов четыре остатка пиррола вытянуты в открытую цепь таким образом, что замкнутого порфиринового кольца в них не образуется. В своем составе они не содержат атомов Mg, или других металлов, а также фитола. Эти пигменты делят на две основные группы в соответствии с их цветом – красные (фикоэритрины) и синие (фикоцианины).
Название «фикобилины» предложил Лемберг (20-е гг. ХХ века) из-за их подобия с желтыми пигментами.
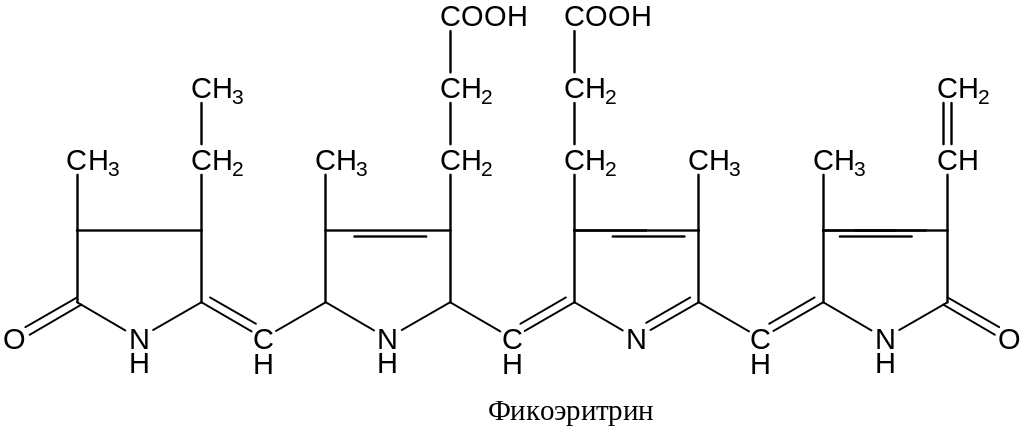
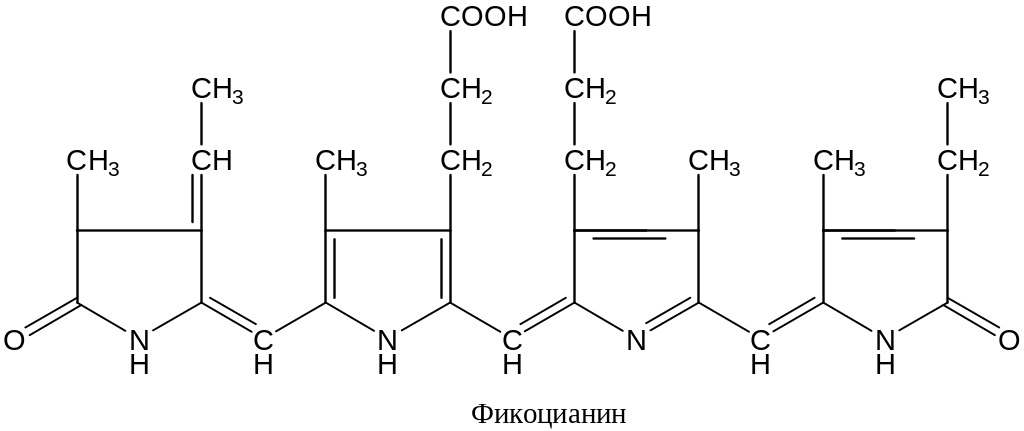
Структурные формулы соответствующих билинов – фикоэритробилина (фикоэритрин) фикоцианобилина (фикоцианин) приведена на рис. 2.5.
|
|
Фикоэритрин и фикоцианин состоят из двух разных белковых субъединиц: α (молекулярная масса ~ 19 000) и β (~ 21 000). Стехиометричные отношения α- и β-субъединиц составляют 1:1. Каждая из белковых субъединиц несет ковалентно связанный с ней фикобилин, при этом субъединицы, выделенные из разных организмов, могут нести разное количество молекул фикобилина – от одной до четырех. Как правило, фикобилины, связанные с одной субъединицей, относятся к одному типу (т. е. к фикоэритробилинам или фикоцианобилинам); в результате получаются красные или синие субъединицы. В некоторых случаях субъединица несет на себе два типа фикобилинов, но тогда один из типов является преобладающим. In vivo белковая субъединица встречается в виде агрегатов (α, β)n, где n равно 3 или 6, что соответствует молекулярным массам около 134 или 268 кД.
К фикобилинам относятся также аллофикацианин. Он назван так потому, что его сначала принимали за одну из форм фикоцианина. Аллофикацианин присутствует в небольших количествах в водорослях семейств красных и сине-зеленых. В отличие от других фикобилипротеинов его молекула состоит только из одного типа белковых субъединиц (молекулярная масса ~ 15 кД), при этом каждая субъединица несет одну молекулу аллофикацианина. In vivo она объединяется в агрегаты с молекулярной массой ~ 10 кД, состоящих из шести субъединиц.
Таблица 2.2