
- •Основные положения теории бутлерова:
- •1. Положение о химическом строении.
- •2. Положение о зависимости свойств от химического строения.
- •3. Положение о взаимном влиянии атомов.
- •Классификация органических соединений
- •Электронные представления о природе химической связи
- •Электронная структура Схема основного электронного состояния
- •Образование ковалентной связи
- •Гибридизация электронов углерода. - и - связи.
- •Основные характеристики ковалентных связей
- •1. Полярность
- •2. Поляризуемость
- •3. Направленность связей
- •4. Длина связи
- •5. Энергия связи
- •6. Классификация органических реакций по механизму
- •Лекция № 2
- •Алифатические соединения (жирные, ациклические)
- •Способы получения предельных углеводородов
- •Лабораторные способы получения алканов
- •Пространственное строение предельных углеводородов
- •Физические свойства предельных углеводородов
- •Химические свойства предельных углеводородов
- •Получение и свойства алифатических радикалов
- •I тип. Реакция замещения
- •II тип. Реакции окисления
- •III тип. Реакции термического расщепления предельных углеводородов
- •IV тип. Изомеризация предельных углеводородов
- •Лекция 3 алкены
- •Номенклатура
- •Способы получения
- •Физические свойства олефинов
- •Химические свойства олефинов
- •1. Реакции присоединения
- •Эффект Караша
- •Свойства карбкатионов
- •2. Реакции окисления
- •3. Реакции полимеризации
- •4. Реакции аллильного замещения
- •Отдельные представители
- •Лекция 4 алкадиены
- •Способы получения
- •Особенности электронного строения диенов с сопряженными связями
- •Физические свойства
- •Химические свойства
- •1. Реакции присоединения
- •2. Реакции окисления
- •3. Реакции полимеризации
- •Натуральный и синтетический каучук
- •Лекция 5 алкины
- •Лабораторные методы получения ацетиленовых углеводородов
- •II. Реакции окисления
- •III. Реакции полимеризации и конденсации
- •Реакции замещения водорода металлом – образование ацетиленидов
- •Изомерия
- •Номенклатура
- •Способы получения
- •Электронное строение
- •Физические свойства
- •Химические свойства
- •I.Реакции нуклеофильного замещения
- •Реакции отщепления галогена
- •III. Реакции отщепления галогеноводорода
- •Лекция 8 спирты (оксисоединения)
- •Свойства
- •Отдельные представители
- •Многоатомные спирты
- •Способы получения (кроме общих)
- •Физические свойства
- •Химические свойства
Основные положения теории бутлерова:
1. Положение о химическом строении.
Молекулы органических соединений имеют определенное химическое строение, под которым понимают последовательность соединения атомов друг с другом в соответствии с их валентностью. Химическое строение вещества можно установить, изучая реакции его разложения или синтеза в мягких условиях и выразить его структурной формулой, например, для этана:

или сокращенной структурной формулой, где черточки ставятся только между атомами углерода: СН3-СН3.
При составлении структурных формул необходимо учитывать основные особенности атома углерода:
углерод, как правило, четырехвалентен;
![]()
атомы углерода могут соединяться друг с другом, образуя цепи: открытые неразветвленные,
![]()
открытые разветвленные

циклические

углерод может затратить на соединение с другим атомом одну, две, три единицы валентности, образуя при этом простую связь:
![]()
двойную связь:
![]()
тройную
связь: -С![]() С-;
С-;
углерод может соединяться как с металлами, так и с неметаллами.
2. Положение о зависимости свойств от химического строения.
Свойства органических веществ зависят не только от количества и природы атомов, входящих в его молекулу, но и от того, в каком порядке они соединяются. Это положение позволило дать объяснение явлению изомерии, когда вещества, имеющие одинаковые эмпирические формулы, но различное химическое строение отличаются по свойствам.
Были выявлены разновидности структурной изомерии:
а) изомерия углеродной цепи СН3-СН2-СН2-СН3
бутан

изобутан
б) изомерия положения (кратных связей или заместителей)
СН2=СН-СН2-СН3 |
-бутилен |
СН3-СН2-СН2-ОН |
бутиловый спирт |
СН3-СН=СН-СН3 |
-бутилен |
|
изобутиловый спирт |
в) метамерия (неуглеродные многовалентные атомы соединены с различными радикалами): СН3-О-СН2-СН2-СН3 метилпропиловый эфир СН3-СН2-О-СН2-СН3 диэтиловый эфир
г) таутомерия – динамическое равновесие двух изомерных форм, способных переходить друг в друга за счет внутримолекулярных перегруппировок:
-
Ацетоуксусный эфир


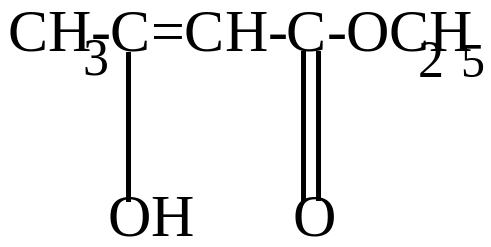
(кетонная форма)
(енольная форма)
3. Положение о взаимном влиянии атомов.
Атомы, связанные в одну молекулу, взаимно влияют друг на друга. Молекулярной формуле С2Н6О соответствуют два метамера:
|
|
этиловый спирт |
диметиловый эфир |
Один из атомов водорода в спирте может замещаться на натрий, в то время как эфир с металлическим натрием не взаимодействует. Причина – в спирте один атом водорода связан с кислородом.
Классификация органических соединений
Развитие теории химического строения позволило Бутлерову провести четкую классификацию органических соединений.
По строению углеродного скелета все органические вещества делятся на три основных вида:
Соединения с открытой цепью углеродных атомов (жирные, алифатические, ациклические).
Соединения с замкнутой цепью углеродных атомов (карбоциклические, изоциклические).
Соединения с замкнутой цепью, состоящей не только из атомов углерода, но и других элементов (гетероатомов), например: N, O, S (гетероциклические соединения).
Внутри каждого раздела проводится более детальная классификация по признаку состава и наличия функциональных групп.
|
|
Состоят из атомов |
Функциональная группа |
1. |
Углеводороды |
С, Н |
- |
2. |
Галогенопроизводные |
С, Н, Гал |
Гал |
3. |
Кислородсодержащие соединения |
С, Н, О |
|
|
а) спирты |
|
-ОН |
|
б) альдегиды и кетоны |
|
С=О |
|
в) карбоновые кислоты |
|
ОН |
4. |
Серосодержащие соединения |
С, Н, S (О) |
|
|
а) тиоспирты |
|
-SH |
|
б) тиоэфиры |
|
-S- |
|
в) сульфокислоты |
|
|
5. |
Азотсодержащие соединения |
С, Н, N (О) |
|
|
а) нитросоединения |
|
-NО2 |
|
б) амины |
|
-NH2 |
6. |
Элементорганические соединения |
С, Н, Э |
|
|
а) металлорганические |
С, Н, Ме |
|
|
б) кремнийорганические |
С, Н, Si (O) |
|
|
в) фосфорорганические и т.д. |
С, Н, Р (О) |
и др. |




 О
О ____С
____С