
- •Каковы основные пути окисления дыхательных субстратов? Как работают оксидоредуктазы?
- •Роль фосфора в процессе дыхания
- •5. Внесение азотных удобрений в жаркий и сухой период лета привело не к повышению, а даже к некоторому снижению урожая опытных участков по сравнению с контрольными участками. Почему?
- •8. Долгодневное двудольное растение выращивалось при коротком ( 10-часовом) дне, короткодневное растение – при долгом (18-часовом) дне. Как будут расти эти растения? Зацветут ли они?
- •Влияние длины дня на цветение фотопериодически чувствительных сортов табака.
- •9. Как объяснить завядание теплолюбивых растений при низких положительных температурах?
- •10. Определите, к каким видам движений относятся следующие явления : …
Каковы основные пути окисления дыхательных субстратов? Как работают оксидоредуктазы?
Окисление дыхательных субстратов в ходе дыхания осуществляется с участием ферментов. Ферменты как белковые катализаторы, помимо свойств, присущим неорганическим катализаторам, обладают рядом особенностей: высокой активностью, высокой спецефичностью по отношению к субстратам и высокой лабильностью. Их пространственная организация и и зависящая от нее активность изменяется под действием внешних и внутренних факторов. Эти свойства обеспечивают возможность тонкой регуляции обмена веществ на уровне ферментов.
Типы окислительно- восстановительных реакций
Существуют четыре способа окисления, и все они связаны с отнятием електронов:
Непосредственная отдача електронов:, напрмер:
Fe 2+---→ Fe 3+
Онятие водорода:

НО____
____ ОН
 О=
=О
О=
=О
Гидрохинон Хинон
Присоеденение кислорода:
2Н2 + О2 → 2Н2О
Образование промежуточного гидратированного соеденения с последующим отнятием двух электронов и протонов:
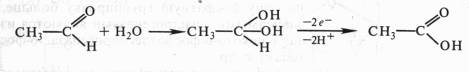
Поскольку окисление одного вещества (донора электронов и протонов) сопряжено с восстановлением другого соеденения (их акцептора), ферменты, катализирующие эти реакции, называют оксидоредуктазами. Все они относятся к I классу ферментов:
Д


 Н2
Е АН2
Д – донор электронов и протонов
Н2
Е АН2
Д – донор электронов и протонов
А - акцептор
Д ЕН2 А Е - энзим
С уществует
3 группы оксидоредуктаз:
уществует
3 группы оксидоредуктаз:
Анаэробные дегидрогеназы (передают электроны различным акцепторам, но не кислороду). В качестве кофермента – NAD+, NADP+. Например: лактатдегидрогеназа, малатдегидрогеназа.
Аэробные дегидрогеназы (передают энергию различным акцепторам, в том числе и кислороду). В качестве простетической группы содержат рибофлавин (витамин В2). Различают два кофермента этой группы: FMN или жёлтый дыхательный фермент Варбурга и FAD.
Пример: сукцинатдегидрогеназа. Доноры электронов для аэробных дегидрогеназ – анаэробные дегидрогеназы, а акцепторы – хиноны, цитохромы, кислород.
Оксидазы (передают электроны только кислороду). При этом образуются вода, перекись водорода и супероксидный анион кислорода – О2-.
 4е
Н2О
(цитохромоксидаза, полифенолоксидаза)
4е
Н2О
(цитохромоксидаза, полифенолоксидаза)
АН2
 +
2е
Н2О2
(оксидазы аминокислот)
+
2е
Н2О2
(оксидазы аминокислот)
 О2
1е
О2
1е
О2- + Н+ (ферменты типа ксантиноксидазы)
Н2О2 и О2 весьма токсичные, поэтому в клетках быстро трансформируются в воду и кислород.
Среди оксидаз очень важную роль играют железосодержащие ферменты и переносчики, относящиеся к цитохромной системе. В неё входят цитохромы и цитохромоксидаза. Именно они передают электроны от флавопротеинов на кислород.
Все компоненты цитохромной системы содержат железопорфири- новую простетическую группу; при переносе электронов железо обратимо восстанавливается и окисляется, приобретая или отдавая электроны и изменяя таким образом свою валентность.
Другие растительные оксидазы (полифенолоксидаза, аскорбатоксидаза) являются медьсодержащими и немитохондриальными (окисляют соответственно фенолы и аскорбиновую кислоту).
К оксидазам относятся также пероксидазы (используют в качестве окислителя перекись водорода) и каталаза (расщепляет перекись водорода на воду и кислород). Простетической группой каталазы и пероксидазы служит гем.
