
- •Методические указания для студентов по выполнению самостоятельных работ
- •Содержание
- •Тема 1.1 Аллотропия и аллотропные модификации
- •Тема 1.2 Радиоактивность элементов и его использование
- •Тема 1.3 Дисперсные системы и их практическое использование в промышленности
- •Тема 1.4 Жесткость воды и способы ее устранения
- •Тема 1.5 Использование неорганических веществ в промышленности
- •Тема 1.7 Коррозия металлов
- •Тема 1.7 Сплавы и их применение
- •Тема 2.1 Классификация реакций в органической химии
- •Тема 2.2 Вулканизация каучука
- •Тема 2.2 Процессы промышленной переработки нефти и газа
- •Тема 2.3 Метанол, этиленгликоль, глицерин –как представители класса спиртов
- •Тема 2.3 Феноло-формальдегидные смолы
- •Тема 2.3 Многообразие карбоновых кислот
- •Тема 2.3 Пленкообразующие масла
- •Тема 2.4 Будущее полимерных материалов
- •Список литературы Учебная основная
- •Учебная дополнительная
Тема 1.4 Жесткость воды и способы ее устранения
Цель, форма работы : углубление знаний о жесткости воды и способов ее устранения ,ответить на вопросы.
Вопросы, рекомендуемые для рассмотрения:
жесткость воды и способы ее устранения. Применение воды в технических целях. Минеральные воды.
Список рекомендуемой литературы:
1.Габриелян О.С. Химия: учеб. для студ. проф. учеб. заведений / О.С. Габриелян, И.Г. Остроумов. – М., 2005.
2.Габриелян О.С. Химия. 10 класс. Базовый уровень: учеб. для общеобразоват. учреждений. – М., 2005.
3. Габриелян О.С. Химия. 11 класс. Базовый уровень: учеб. для общеобразоват. учреждений. – М., 2006.
4. Глинка Н.Л. Общая химия.-Л.:Химия,1988.
5.Потапов В.М.Химия.-М.: Высшая школа, 1985.
6. https://sites.google.com/site/himulacom/repetitor-po-himii
Теоретические основы:
Жесткость воды – это совокупность свойств, обусловленных содержанием в воде катионов кальция и магния. Анионами растворимых солей кальция и магния могут быть гидрокарбонат-ионы, сульфат-ионы и хлорид-ионы. Различают временную (карбонатную) и постоянную жесткость. Временная жесткость обусловлена содержанием в воде гидрокарбонатов кальция и магния. Временная жесткость легко устраняется кипячением:
![]()
Постоянная жесткость обусловлена наличием в воде сульфатов, хлоридов и других солей кальция и магния. Постоянную жесткость можно устранить, используя следующие способы.
а) Известково-содовый способ – к воде добавляют смесь гашеной извести и соды. При этом временная жесткость воды устраняется гашеной известью, а постоянная – содой:
Ca(HCO3)2
+ Ca(OH)2
= 2CaCO3 + 2H2O,
+ 2H2O,
CaCl2 + Na2CO3 = CaCO3 + 2NaCl.
б) Катионитный способ – воду пропускают через колонку, заполненную катионитом (катиониты – твердые вещества, содержащие в своем составе подвижные катионы, способные обмениваться на ионы внешней среды) Na2R, где R – анион. На катионите задерживаются ионы кальция и магния, а в раствор переходят ионы натрия, в результате чего жесткость воды уменьшается:
Na2R
+ Ca2+
 CaR
+ 2Na+,
CaR
+ 2Na+,
Na2R + Mg2+ MgR + 2Na+.
Через определенное время катионит необходимо регенерировать, т.е. восстановить первоначальные свойства. Для этого через катионообменные колонки пропускают насыщенный раствор поваренной соли, при этом происходят обратные процессы:
CaR + 2NaCl Na2R + CaCl2,
MgR + 2NaCl Na2R + MgCl2.
После такой промывки катионит снова можно использовать для умягчения воды.
Сумма временной и постоянной жесткости составляет общую жесткость воды, которая количественно выражается числом ммоль эквивалентов ионов кальция и магния, содержащихся в 1 л воды (таблица).
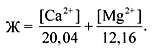
Характеристика воды по степени жесткости
Характеристика воды по жесткости |
Общая жесткость, ммоль экв/л |
Очень мягкая вода |
Не более 1,5 |
Мягкая вода |
От 1,5 до 4
|
Вода средней жесткости |
От 4 до 8 |
Жесткая вода
|
От 8 до 12 |
Очень жесткая вода |
Свыше 12 |
В жесткой воде плохо развариваются продукты, т.к. катионы кальция образуют нерастворимые соединения, взаимодействуя с белками пищи; плохо завариваются чай, кофе; плохо мылится мыло из-за присутствия мало растворимых в воде стеаратов кальция и магния. Постоянное употребление жесткой воды может привести к отложению солей в организме человека. Контрольные вопросы:
Чем обусловлена жёсткость воды?
Какие виды жёсткости воды различают?
Присутствием каких соединений обусловлена временная жёсткость?
Присутствием каких соединений обусловлена постоянная жёсткость воды?
Какими способами устраняют временную жёсткость?
Какими способами устраняют постоянную жёсткость?
Почему жесткость воды следует устранять?
Каким образом может возникнуть в природе жесткость воды?
Почему жесткую воду нельзя употреблять для охлаждения двигателей машин?
Карбонат кальция в воде нерастворим. Однако известняки вымываются водой. Чем это можно объяснить?
Порядок проверки, защиты самостоятельной работы: проверка рабочей тетради.
